Foram encontradas 351 questões.
As células combustíveis despontam como a alternativa mais viável para a obtenção de energia elétrica. A figura I, abaixo, mostra a variação da eficiência na conversão de energia com a potência máxima de saída de várias fontes de energias renováveis.
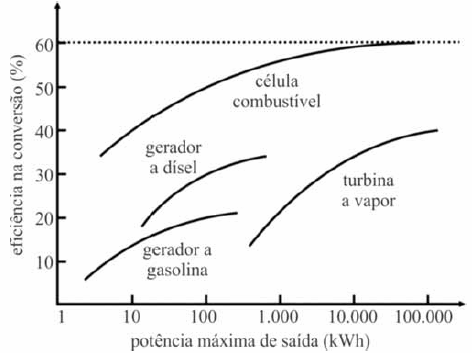
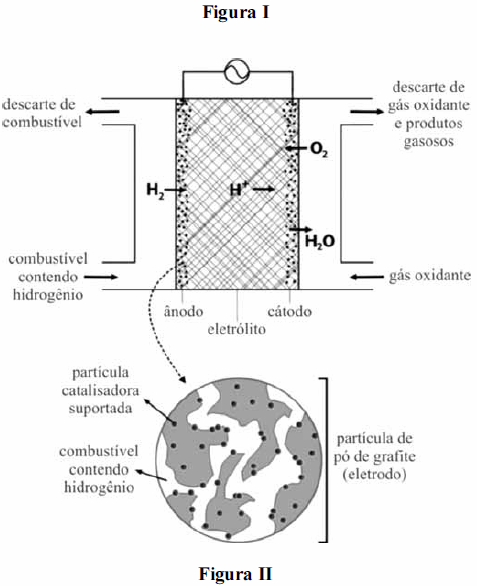
As células combustíveis são, em princípio, baterias que convertem a energia química de uma reação eletroquímica em energia elétrica, como exemplificado na figura II. Na tabela abaixo, são apresentadas semirreações das células e o potencial padrão de redução.

Tendo como referência as informações acima, julgue o item a seguir.
Os geradores a gasolina, dísel e célula combustível com potência de saída de 100 kWh realizam o mesmo trabalho em um mesmo intervalo de tempo.
Provas
O molibdato de amônio, cuja fórmula é (NH4)6Mo7O24A7H2O, é um dos compostos utilizados no processo de fabricação de alvos metálicos para produção de raios X. Nesse processo, o composto em solução aquosa é reduzido a molibdênio metálico, que é prensado e tratado termicamente.
A partir dessas informações, julgue o item a seguir.
Uma solução aquosa de molibdato de amônio de concentração 0,5 mol/L, se for diluída a 0,05 mol/L, sem alteração de temperatura, terá seu pH reduzido em 10 unidades.
Provas
O molibdato de amônio, cuja fórmula é (NH4)6Mo7O24A7H2O, é um dos compostos utilizados no processo de fabricação de alvos metálicos para produção de raios X. Nesse processo, o composto em solução aquosa é reduzido a molibdênio metálico, que é prensado e tratado termicamente.
A partir dessas informações, julgue o item a seguir.
No composto (NH4)6Mo7O24A7H2O, o número de oxidação do molibdênio é +6.
Provas
O molibdato de amônio, cuja fórmula é (NH4)6Mo7O24A7H2O, é um dos compostos utilizados no processo de fabricação de alvos metálicos para produção de raios X. Nesse processo, o composto em solução aquosa é reduzido a molibdênio metálico, que é prensado e tratado termicamente.
A partir dessas informações, julgue o item a seguir.
São necessários mais de 220 mL de uma solução aquosa de (NH4)6Mo7O24A7H2O, de concentração 200,0 g/L, para serem obtidos 25 g de molibdênio metálico, considerando-se a redução de todo o molibdênio contido nessa solução.
Provas
Analise a figura abaixo e assinale a opção correta.
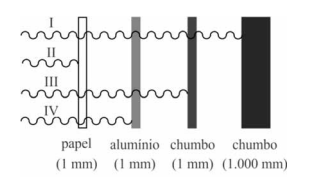
Na figura acima, que ilustra características de emissões radioativas em diferentes materiais, as linhas onduladas I, II, III e IV representam, respectivamente, as radiações
Provas
No século XIX, cientistas observaram que o comportamento e a descrição do átomo de Dalton não se enquadravam no sistema newtoniano de princípios físicos e não explicavam o comportamento elétrico da matéria. Uma das linhas de investigação consistiu em aplicar descargas elétricas em um tubo que continha gás em pequena quantidade e em observar as emissões eletromagnéticas irradiadas, capazes de produzir fluorescência na incidência em certos materiais. Descobriu-se, depois, que a frequência das emissões chamadas de raios X era proporcional ao número atômico (Z) do átomo emissor, segundo a equação de Moseley,\( f = (2,47 \times 10^{15} \times (Z-1)^2 \), em que \( f \) representa a frequência de emissão relativa às transições eletrônicas ocorridas na camada eletrônica K desse átomo, em Hertz. A figura a seguir mostra o espectro de emissão de raios X proveniente do bombardeamento de um feixe de elétrons em determinado alvo metálico.
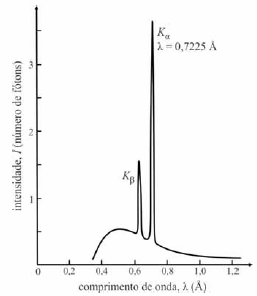
A energia relativa à emissão K\( _\beta \) é maior que a relacionada à emissão \( _\alpha \), ambas mostradas na figura.
Provas
No século XIX, cientistas observaram que o comportamento e a descrição do átomo de Dalton não se enquadravam no sistema newtoniano de princípios físicos e não explicavam o comportamento elétrico da matéria. Uma das linhas de investigação consistiu em aplicar descargas elétricas em um tubo que continha gás em pequena quantidade e em observar as emissões eletromagnéticas irradiadas, capazes de produzir fluorescência na incidência em certos materiais. Descobriu-se, depois, que a frequência das emissões chamadas de raios X era proporcional ao número atômico (Z) do átomo emissor, segundo a equação de Moseley,\( f = (2,47 \times 10^{15} \times (Z-1)^2 \), em que \( f \) representa a frequência de emissão relativa às transições eletrônicas ocorridas na camada eletrônica K desse átomo, em Hertz. A figura a seguir mostra o espectro de emissão de raios X proveniente do bombardeamento de um feixe de elétrons em determinado alvo metálico.

Considerando as informações do texto e tomando I = I(\( \lambda \)) como a intensidade da emissão de raios X em função do comprimento de onda \( \lambda \), julgue o item a seguir.
Sabendo que os picos K" e K$ , observados na figura, decorrem de emissões relacionadas a transições eletrônicas nas camadas mais internas de um átomo, é correto afirmar que essas camadas são mais energéticas que as camadas mais externas do átomo, de onde os elétrons podem ser arrancados mais facilmente.
Provas
No século XIX, cientistas observaram que o comportamento e a descrição do átomo de Dalton não se enquadravam no sistema newtoniano de princípios físicos e não explicavam o comportamento elétrico da matéria. Uma das linhas de investigação consistiu em aplicar descargas elétricas em um tubo que continha gás em pequena quantidade e em observar as emissões eletromagnéticas irradiadas, capazes de produzir fluorescência na incidência em certos materiais. Descobriu-se, depois, que a frequência das emissões chamadas de raios X era proporcional ao número atômico (Z) do átomo emissor, segundo a equação de Moseley,\( f = (2,47 \times 10^{15} \times (Z-1)^2 \), em que \( f \) representa a frequência de emissão relativa às transições eletrônicas ocorridas na camada eletrônica K desse átomo, em Hertz. A figura a seguir mostra o espectro de emissão de raios X proveniente do bombardeamento de um feixe de elétrons em determinado alvo metálico.

Considerando as informações do texto e tomando I = I(\( \lambda \)) como a intensidade da emissão de raios X em função do comprimento de onda \( \lambda \), julgue o item a seguir.
O tecido ósseo pode ser visualizado por meio do exame de raios X.
Provas
No século XIX, cientistas observaram que o comportamento e a descrição do átomo de Dalton não se enquadravam no sistema newtoniano de princípios físicos e não explicavam o comportamento elétrico da matéria. Uma das linhas de investigação consistiu em aplicar descargas elétricas em um tubo que continha gás em pequena quantidade e em observar as emissões eletromagnéticas irradiadas, capazes de produzir fluorescência na incidência em certos materiais. Descobriu-se, depois, que a frequência das emissões chamadas de raios X era proporcional ao número atômico (Z) do átomo emissor, segundo a equação de Moseley,\( f = (2,47 \times 10^{15} \times (Z-1)^2 \), em que \( f \) representa a frequência de emissão relativa às transições eletrônicas ocorridas na camada eletrônica K desse átomo, em Hertz. A figura a seguir mostra o espectro de emissão de raios X proveniente do bombardeamento de um feixe de elétrons em determinado alvo metálico.

Considerando as informações do texto e tomando I = I(\( \lambda \)) como a intensidade da emissão de raios X em função do comprimento de onda \( \lambda \), julgue o item a seguir.
O trabalho de Moseley sobre raios X forneceu subsídios para a construção da Tabela Periódica atual, na qual os elementos químicos estão dispostos em ordem crescente de massa atômica.
Provas
No século XIX, cientistas observaram que o comportamento e a descrição do átomo de Dalton não se enquadravam no sistema newtoniano de princípios físicos e não explicavam o comportamento elétrico da matéria. Uma das linhas de investigação consistiu em aplicar descargas elétricas em um tubo que continha gás em pequena quantidade e em observar as emissões eletromagnéticas irradiadas, capazes de produzir fluorescência na incidência em certos materiais. Descobriu-se, depois, que a frequência das emissões chamadas de raios X era proporcional ao número atômico (Z) do átomo emissor, segundo a equação de Moseley,\( f = (2,47 \times 10^{15} \times (Z-1)^2 \), em que \( f \) representa a frequência de emissão relativa às transições eletrônicas ocorridas na camada eletrônica K desse átomo, em Hertz. A figura a seguir mostra o espectro de emissão de raios X proveniente do bombardeamento de um feixe de elétrons em determinado alvo metálico.

Considerando as informações do texto e tomando I = I(\( \lambda \)) como a intensidade da emissão de raios X em função do comprimento de onda \( \lambda \), julgue o item a seguir.
Ao contrário do estabelecido no modelo atômico proposto por Dalton, em que o átomo é considerado uma partícula maciça, indivisível e sem cargas, experimentos em que foi utilizado um tubo similar ao descrito no texto permitiram a Thomson demonstrar a existência de partículas subatômicas eletricamente carregadas.
Provas
Caderno Container