Foram encontradas 135 questões.
Quantos estereoisômeros são possíveis para o seguinte composto?
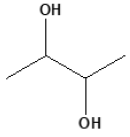
Provas
Uma amostra de 0,728 g de cloreto de hidrogênio gasoso é dissolvida em água pura para 200 mL de solução. Marque a única opção que mostra as concentrações aproximadas, em mol/L, de íons hidrônio e hidróxido, respectivamente.
Provas
Determinado composto orgânico X é submetido a reação de hidratação em catálise ácida, produzindo um álcool, que é sequencialmente oxidado com ácido crômico formando a cetona Y. Outro percurso que também pode levar a formação da cetona Y é por meio de uma ozonólise, seguida de hidratação, do composto orgânico Z. Marque a opção que corresponde aos compostos X, Y e Z, respectivamente.
Provas
Marque a opção que correlaciona corretamente o nome do composto químico com a respectiva fórmula molecular:
Provas
Em uma aula de química experimental, um aluno, utilizou uma capela para misturar cuidadosamente pequena quantidade de açúcar comum (sacarose, C12H22O11) com ácido sulfúrico concentrado. A mistura gerou mudança de cor no açúcar (escurecendo) e provocou liberação de gases, indicativo de que ocorreu reação química. Com base no relato acima assinale a informação verdadeira:
Provas
Uma importante reação química que efetivamente está relacionada com a transformação de óleos ou gorduras de origem vegetal ou animal é conhecida como reação de transesterificação. Devido a sua versatilidade essa reação é utilizada em muitos processos industriais, por exemplo, os processos de obtenção do tereftalato de polietileno (PET) para produção de garrafas de refrigerantes; obtenção de resinas alquídicas, usadas na composição das conhecidas tintas "a óleo"; e ainda na produção de biodiesel usado como combustível em veículos automotores. Marque a opção correta que, de forma geral, resume o processo da transesterificação:
Provas
Aproximadamente, quantos mililitros de H2SO4 0,5 molar são necessários para dissolver 0,5 g de carbonato de cobre (II)? Considere as massas molares (g/mol): H=1; C=12; O=16; S=32; Cu=63,5.
Provas
O valor de H para a equação abaixo é -126kJ. Quanto calor (em kJ) é liberado quando 2,0 mol de NaOH são formados na referida equação química?
2Na2O2(s) + 2H2O(l) !$ \rightarrow !$ 4NaOH(s) + O2(g)
Provas
O alumínio reage com o ácido sulfúrico para formar sulfato de alumínio e hidrogênio. Qual é o volume de gás hidrogênio em litros (L) produzido a 300 K e pressão de 1,0 atm, quando 5,4 g de alumínio e 50,0 mL de ácido sulfúrico 5,0 M são misturados para a reação? Considere: massa molar do alumínio = 27; 0g=mol; R = 0; 082atm:L:mol-1K-1.
Provas
Uma solução aquosa incolor contém nitratos de dois metais, X e Y. Quando foi adicionada a uma solução aquosa de NaCl, formou-se um precipitado branco. Verificou-se que este precipitado era parcialmente solúvel em água quente para dar um resíduo P e uma solução Q. O resíduo P era solúvel em NH3 aquosa e em excesso de tiossulfato de sódio (Na2S2O3). A solução quente Q deu um precipitado amarelo com KI. Os metais X e Y, respectivamente, são:
Provas
Caderno Container