Foram encontradas 40 questões.
O estimulante cardíaco e respiratório metamivam possui a fórmula estrutural a seguir:
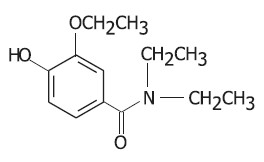
Considerando esse composto, é correto afirmar que ele apresenta os seguintes grupos funcionais:
Provas
Considere certa quantidade da mistura de água e suco de limão, contida em um copo de béquer, a 25°C. Analise as afirmativas abaixo, concernentes a esse sistema:
I) O sistema é ácido.
II) O pH do sistema é maior que 7.
III) No sistema, a concentração dos íons H+ é maior que a dos íons OH–.
A partir dessa análise, está(ão) correta(s):
Provas
Um comprimido efervescente de vitamina C intacto, pesando 5 gramas, quando colocado em um copo contendo água a 25 °C, será dissolvido em dois minutos. Considerando essa informação, assinale como verdadeira (V) ou falsa (F) cada uma das proposições.
( ) Se o comprimido efervescente estiver em pequenos pedaços, o tempo de dissolução também será de dois minutos.
( ) O tempo de dissolução do comprimido efervescente intacto mantém-se quando o comprimido for dissolvido em água a 40 °C, pois a área de contato é a mesma.
( ) Quanto maior a superfície de contato do comprimido efervescente com a água, maior o número de colisões favoráveis, portanto maior a velocidade de dissolução.
( ) O aumento da temperatura diminui a energia de ativação, diminuindo, portanto, o tempo de dissolução.
Assinale a alternativa que apresenta a sequência correta.
Provas
Um elemento químico possui massa atômica igual a 39,1 u e número atômico igual a 19. Acerca desse elemento, considere as seguintes afirmativas:
I) A substância pura desse elemento apresenta-se na forma de um metal em condições ambientais.
II) O íon mais estável desse elemento apresenta carga +2.
III) Esse elemento formará compostos iônicos com os elementos do grupo 17.
IV) A substância pura desse elemento deve ser inerte (não reage) com água.
É(são) verdadeira(s):
Provas
Uma solução aquosa de um eletrólito forte consiste de íons hidratados que estão livres para mover-se em um solvente. Os solutos em soluções não eletrolíticas estão presentes como moléculas. Somente uma fração pequena de moléculas do soluto em soluções eletrolíticas fracas está presentes como íons. Quanto aos eletrólitos, pode-se afirmar que:
I) as soluções aquosas de cloreto de sódio e do nitrato de sódio são exemplos de soluções que conduzem bem corrente elétrica, ou seja, são eletrólitos fortes.
II) os íons não são formados quando um sólido iônico se dissolve. Eles existem como íons ligados no sólido, mas tornam-se livres e podem mover-se na presença de água.
III) as soluções do hidróxido de magnésio e hidróxido de cálcio são exemplos de soluções que conduzem bem a corrente elétrica, ou seja, são eletrólitos fortes.
IV) soluções não eletrolíticas só contém íons.
V) não existem compostos moleculares que sejam eletrólitos fortes.
É(são) verdadeira(s):
Provas
Em um experimento de laboratório, coloca-se um prego de aço dentro de um copo de béquer, contendo ácido clorídrico concentrado, e verifica-se uma efervescência ao redor do prego. É correto afirmar que:
Provas
Analise as proposições em relação a um experimento de eletroquímica.
I) Em uma reação de óxidorredução que ocorre espontaneamente, os elétrons são transferidos de uma espécie química com maior potencial de redução para outra com menor potencial de redução. Portanto, ao calcularmos a diferença de potencial da célula, chega-se a um valor positivo.
II) Uma medida de potencial eletroquímico considera o uso de um eletrodo padrão de hidrogênio (EPH). Se a semicela H+/H2 atuar como ânodo, a semirreação será a de oxidação de H2 a H+ e, se atuar como cátodo, será a de redução de H+ a H2.
III) Uma das formas de evitar o acúmulo de cargas elétricas nas soluções catódicas e anódicas é o uso de uma ponte salina. O excesso de ânions ou cátions gerados nas reações eletroquímicas é compensado pela migração de íons provenientes da ponte salina.
Está(ão) correta(s):
Provas
O tricloreto de fósforo (P!$ Cl !$3) é um líquido incolor bastante tóxico com larga aplicação industrial, principalmente na fabricação de defensivos agrícolas.
Dados: Números atômicos: P = 15; !$ Cl !$ = 17.
A respeito desse composto, é correto afirmar que:
Provas
Assinale a alternativa correta.
A pirita, de fórmula FeS2, foi uma das primeiras estruturas cristalinas resolvidas por métodos de difração de raios X, e os cristais cúbicos simples mostram claramente a ligação enxofre-enxofre [S-S], com carga total –2, dentro das unidades. Assim, FeS2 poderia ser chamado de persulfeto de ferro, ao invés de dissulfeto de ferro, como é usualmente denominado.
O nome persulfeto de ferro seria adequado, pois:
Provas
Os potenciais padrão de redução, determinados mediante processos eletroquímicos, podem ser empregados para prever a espontaneidade de reações, mesmo quando essas não constituem pilhas ou baterias.
Observe a tabela a seguir.
|
Ag+ (aq) + e–!$ \rightleftharpoons !$ Ag(s) |
E0 = 0,80 V |
|
Co2+ (aq) + 2e–!$ \rightleftharpoons !$ Co(s) |
E0 = –0,28 V |
|
Al3+ (aq) + 3e–!$ \rightleftharpoons !$ Al(s) |
E0 = –1,66 V |
|
Ba2+ (aq) + 2e–!$ \rightleftharpoons !$ Ba(s) |
E0 = –2,90 V |
Com base na tabela, considere as reações abaixo.
I) Ba(NO3)2 + 2 Ag !$ → !$ 2 AgNO3 + Ba
II) 2 Al(NO3)3 + 3 Co !$ → !$ 3 Co(NO3)2 + 2 Al
III) 3AgNO3 + Al !$ → !$ Al(NO3)3 + 3 Ag
Ocorre reação espontânea em:
Provas
Caderno Container