Foram encontradas 13.259 questões.
O arranjo experimental mostrado na imagem representa uma célula eletroquímica (pilha) usada na obtenção do potencial padrão de redução (Eº) de semirreações, adotando-se Eº = 0 V para o eletrodo de hidrogênio. Atribui-se Eº positivo para o metal que reduz frente ao H e Eº negativo para o metal ou espécie que oxida.
A substituição do cobre por outro metal (metal M) no arranjo experimental gera um potencial de 0,44 V e o fluxo de elétrons inverte-se de M para o eletrodo de hidrogênio.
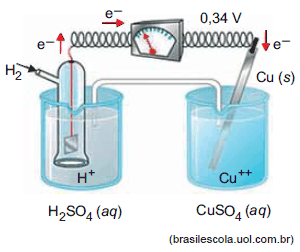
De acordo com as informações, uma pilha formada pelo metal M e pelo metal cobre produz um potencial de
Provas
Um médico prescreve para seu paciente a infusão de 30 mL de uma solução preparada pela diluição de 400 mg de determinado medicamento em 240 mL de soro glicosado a 5% (m/v).
As massas do medicamento e de glicose administradas ao paciente são, respectivamente, de
Provas
Analise o primeiro verso do poema “Psicologia de um Vencido”, de Augusto dos Anjos, que faz alusão à composição química dos seres humanos restringindo-a ao elemento químico carbono e ao composto amônia (NH3).
Eu, filho do carbono e do amoníaco,
Monstro de escuridão e rutilância,
Sofro, desde a epigênesis da infância,
A influência má dos signos do zodíaco.
Todos os elementos químicos identificados no poema podem ser encontrados nas moléculas de
Provas
O lítio é um metal alcalino economicamente importante e bastante versátil. A forma iônica desse elemento químico combinada ao íon carbonato (CO3 2–) forma o carbonato de lítio, composto iônico empregado como medicamento no tratamento do transtorno bipolar.
A fórmula do composto iônico de lítio mencionado no texto e a distribuição eletrônica em níveis e subníveis de energia do íon lítio são:
Provas
O gás ozônio é uma substância química ambígua do ponto de vista ambiental. Na troposfera, o ozônio é tóxico devido ao caráter oxidante. Na estratosfera, absorve radiação ultravioleta nociva ao ser humano por meio de um processo natural que leva à contínua formação e fragmentação da molécula, como representado na imagem.
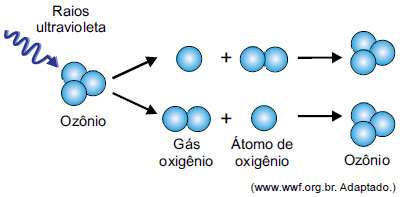
O processo ilustrado na imagem envolve a participação de
Provas
A imagem mostra a formação de água líquida por meio de duas mudanças de estado físico distintas:
Mudança 1 – água formada na superfície externa de um copo.
Mudança 2 – água proveniente do derretimento de gelo.

De acordo com as informações fornecidas, afirma-se que nas mudanças citadas ocorre
Provas
Apesar de a África ser considerada o berço das civilizações e existirem indícios de conhecimentos elementares de Química no sul do continente cerca de 100.000 anos atrás, os conhecimentos químicos ensinados são eurocentristas. Entretanto, uma das grandes contribuições para o estudo de reatividade química é atribuída ao químico egípcio Ahmed Hassan Zewail, agraciado com o prêmio Nobel em 1999 por seus estudos de reações químicas usando uma técnica conhecida como espectroscopia de femtossegundos. Essa técnica possibilita identificar espécies com tempo de vida curto utilizando pulsos de laser com duração de 10−15 s.
Essa contribuição é relevante para o estudo de reações químicas, pois
Provas
No processo de compra e venda de artigos de ouro, é comum testar os objetos para verificar se eles realmente são feitos de ouro ou se são alguma falsificação feita com metais menos nobres. Esse teste pode ser feito adicionando um pequeno volume de ácido forte concentrado às raspas do objeto a ser testado, conforme figura a seguir. Caso o objeto seja feito com ouro, as raspas permanecem visíveis, enquanto as raspas de falsificações são dissolvidas.

Considerando apenas o potencial de redução padrão, qual das alternativas apresenta um material que poderia gerar um falso positivo para o objeto de ouro no teste descrito?
Provas
Um tema de grande interesse na química é a ativação seletiva de ligações C-H. Essa ativação permite a substituição de H nessas ligações por outros átomos, como O ou N. A relevância desse tema pode ser verificada em um estudo recentemente publicado no prestigioso periódico Science, que conta com uma egressa da USP dentre seus autores.
A baixa diferença de eletronegatividade entre C e H é um dos motivos que dificulta a ativação da ligação C-H, pois torna a ligação pouco polar e diminui sua reatividade.
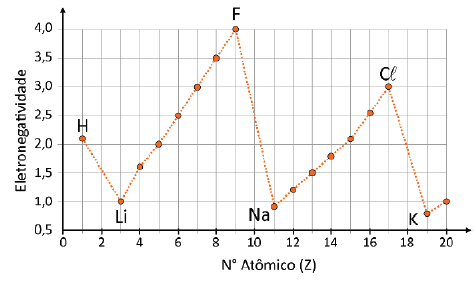
Considerando apenas a eletronegatividade, representada no gráfico, qual das alternativas apresenta uma ligação ainda menos reativa do que a ligação C-H?
Provas
Para gerar hidrogênio, foi utilizado o aparato ilustrado na figura.
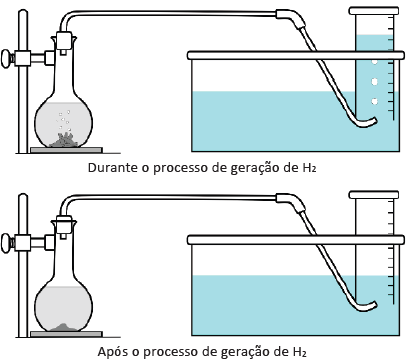
Ao frasco à esquerda adicionou-se uma quantidade prédeterminada de raspas de zinco metálico e ácido clorídrico. Em seguida, o frasco foi fechado com uma rolha conectada a uma tubulação. À medida que o hidrogênio é produzido pela reação Zn0(s) + 2H+(aq) → Zn2+(aq) + H2(g), o gás se acumula em uma proveta previamente cheia de água. Dado que a solubilidade do hidrogênio na água é desprezível, o volume ocupado pelo gás na proveta corresponde ao volume de hidrogênio produzido durante a reação.
Considerando que, nas condições do experimento, foram gerados 49,8 mL de hidrogênio, qual a quantidade de Zn metálico, em gramas, que de fato reagiu?
Provas
Caderno Container