Foram encontradas 13.399 questões.
O Naproxeno é um anti-inflamatório com atividade analgésica. É utilizado principalmente no tratamento de inflamação, dor e edema, como também nas osteoartrites e artrite reumatoide. A sua estrutura é descrita a seguir.
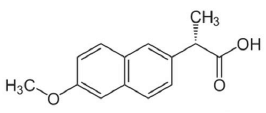
Sobre o Naproxeno, um químico fez as seguintes argumentações:
I. Apresenta as funções orgânicas ácido carboxílico e éter.
II. Contém núcleos benzênicos isolados.
III. Contém carbono quiral.
Estão corretas as argumentações
Provas
Na espectroscopia atômica, geralmente se aplica uma alta temperatura para converter os íons e as moléculas da amostra em átomos para análise. Após a formação desses átomos, alguns podem receber energia adicional da fonte de calor, levando à sua excitação.
A etapa de excitação atômica será útil se o objetivo for, posteriormente, medir a
Provas
Considere que, em uma aula prática de Química, o professor fez dois experimentos de reações entre ácidos e base.
• Experimento 1: misturou 100 mL de HCl 0,02 mol/L com 150 mL de hidróxido de sódio 0,01 mol/L.
• Experimento 2: misturou 150 mL de HCl 0,02 mol/L com 100 mL de hidróxido de sódio 0,05 mol/L.
Ao final dos experimentos, o professor transferiu as duas misturas para um único recipiente e solicitou ao técnico que neutralizasse as soluções para descarte.
Nesse contexto, o técnico precisa adicionar, para neutralização e descarte da mistura, 100 mL de
Provas
O acetileno com 99,8% de pureza é utilizado como gás para instrumentos de Espectrometria de Absorção Atômica com chama (AAS). A combustão do gás acetileno pode ser representada pela equação química a seguir.
Considere os dados apresentados no quadro a seguir.
C2H2 (g) + 5/2 O2 (g) → 2 CO2 (g) + H2O (L)
|
Composto |
!$ \Delta !$H0(formação) (kJ mol-1) |
|
C2H2 (g) |
+ 226,7 |
|
CO2 (g) |
- 393,5 |
|
H2O (L) |
- 285,8 |
Fonte: https://www.fq.pt/images/tabelas/entalpiasdeformacao.pdf.
Qual o valor mais próximo do calor de combustão (!$ \Delta !$H) de 52 g do gás acetileno?
Provas
Os instrumentos para as regiões ultravioleta (UV), visível (VIS) e de infravermelho (IR) apresentam tantas características em comum que, com frequência, são denominados instrumentos ópticos, mesmo o olho humano não sendo sensível aos comprimentos de onda no ultravioleta e no infravermelho. Os instrumentos espectroscópicos típicos possuem cinco componentes.
Sobre os componentes dos instrumentos espectroscópicos, numere a COLUNA II de acordo com a COLUNA I, relacionando seus nomes às suas respectivas características.
COLUNA I
1. Fonte
2. Seletor de comprimento de onda
3. Detector
4. Processador
COLUNA II
( ) Em termos de construção mecânica, empregam-se fendas, lentes, espelhos e prismas.
( ) Transforma o sinal elétrico em um sinal de resposta que precisa ser comparado com uma amostra de referência.
( ) Gera um feixe com potência radiante suficiente para facilitar a detecção e as medidas.
( ) Transdutores que convertem energia radiante em sinais elétricos.
Assinale a sequência correta.
Provas
Considere que um químico recebeu como instrução o preparo de uma solução de hidróxido de sódio a partir de um reagente analítico sólido grau PA.
A vidraria essencial para o preparo dessa solução é o(a)
Provas
As reações de obtenção de sabão ocorrem entre ésteres e bases (sodas ou hidróxidos). As gorduras e óleos são exemplos de ésteres usados nas reações de saponificação. A equação química a seguir representa a reação simplificada de saponificação.

Considere que nesse processo reacional misturou-se 445 g da estearina com 1 litro da solução de hidróxido de sódio.
Tendo em vista que não ocorrem perdas ou excesso de reagentes no processo reacional, qual concentração em mol/L de hidróxido de sódio seria necessária para o total consumo da estearina?
Provas
Os métodos espectroquímicos de análises são baseados na quantidade de radiação transmitida ou absorvida. Cada molécula tem capacidade de absorver radiação eletromagnética. A radiação que uma molécula ou átomo absorvem pode estabelecer uma relação linear entre a absorvância e a concentração da amostra.
Esse processo de absorção de radiação recebe o nome de
Provas
Considere que um grupo de estudante montou um sistema de eletrólise com dois eletrodos conectados em um gerador. Os eletrodos foram submersos em uma solução aquosa de um sal.
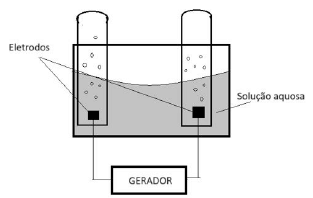
Sabe-se que, durante o funcionamento do processo eletrolítico nas duas células, ocorre a liberação de um gás, como apresentado na figura. De acordo com o fenômeno químico ocorrido, a solução aquosa pode ser constituída por um sal de
Provas
Considere que, em uma aula prática de Química, derramou-se um pouco de ácido sulfúrico (H2SO4) em uma bancada do laboratório. O técnico decidiu neutralizá-lo, espalhando bicarbonato de sódio (NaHCO3) sobre ele e, em seguida, enxugou a solução resultante. Sabe-se que o bicarbonato de sódio é adicionado até que a efervescência causada pelo gás carbônico liberado na reação pare de se formar. Nesse incidente, sabe-se que 50 mL do ácido sulfúrico, 5,0 mol/L, foi derramado.
Nesse contexto, qual a massa mínima do sal, em gramas, foi necessária para neutralizar completamente o ácido sulfúrico?
Provas
Caderno Container