Foram encontradas 13.241 questões.
Os valores associados às regiões vermelha e azul nos diagramas desses três materiais são, respectivamente:
Provas
Provas
Provas
Provas
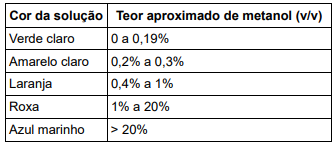
Para simular uma contaminação, um investigador usou uma garrafa de vidro vazia e seca, de 750 mL, com massa de 348,0 g. Essa garrafa foi enxaguada por dentro com etanol combustível adulterado com 50% de metanol. Após verter o conteúdo do enxágue, a massa da garrafa molhada foi de 350,4 g. A garrafa foi então preenchida com etanol de laboratório padrão para análise até completar 750 mL. Por fim, uma alíquota do conteúdo da garrafa foi submetida ao teste.
Dados: Densidade etanol = densidade metanol = 0,79 g mol–1.
Considerando a simulação descrita no texto, o teste de análise deve resultar em qual cor?
Provas
Provas
Nas atividades laboratoriais e em processos industriais, as operações unitárias constituem etapas fundamentais para o controle, a separação e o beneficiamento de substâncias químicas. Considerando essa informação, julgue o item seguinte, acerca dos procedimentos e das aplicações práticas dessas operações.
A liofilização é uma operação unitária de secagem conduzida a 180 °C e 1,8 atm, sob atmosfera inerte de argônio, assegurando a desidratação completa da amostra.
Provas
Nas atividades laboratoriais e em processos industriais, as operações unitárias constituem etapas fundamentais para o controle, a separação e o beneficiamento de substâncias químicas. Considerando essa informação, julgue o item seguinte, acerca dos procedimentos e das aplicações práticas dessas operações.
O sistema de filtração que utiliza o funil de Büchner acoplado a um kitassato opera sob altas pressões, permitindo acelerar a separação dos componentes sólidos por compressão forçada do líquido por meio do filtro.
Provas
Nas atividades laboratoriais e em processos industriais, as operações unitárias constituem etapas fundamentais para o controle, a separação e o beneficiamento de substâncias químicas. Considerando essa informação, julgue o item seguinte, acerca dos procedimentos e das aplicações práticas dessas operações.
A série Tyler é um sistema de peneiras padronizadas empregadas em laboratórios e indústrias para a análise granulométrica de materiais sólidos.
Provas
Nas atividades laboratoriais e em processos industriais, as operações unitárias constituem etapas fundamentais para o controle, a separação e o beneficiamento de substâncias químicas. Considerando essa informação, julgue o item seguinte, acerca dos procedimentos e das aplicações práticas dessas operações.
O Soxhlet é um sistema amplamente utilizado na operação unitária de extração sólido-líquido contínua, processo fundamentado nos princípios de transferência de massa entre a fase sólida e o solvente.
Provas
Caderno Container