Foram encontradas 13.431 questões.
Pesquisa realizada em dosagem de contaminantes em esgoto doméstico revelou a presença de hormônios e antibióticos decorrentes de urina e fezes de indivíduos que fazem uso dessa medicação.
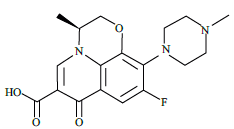
Na molécula de levofloxacin, são encontrados grupos funcionais característicos de
Provas
Um estudo cinético envolvendo a reação
2 A + B + C !$ \rightarrow !$ 2D + E
foi realizado com três experimentos de medida de velocidade de reação sob a mesma temperatura e condições de agitação.
|
Experimento |
A mol L–1 |
B mol L–1 |
C mol L–1 |
Velocidade |
| 1 | 0,1 | 0,1 | 0,1 | 3,0 x 10-4 |
| 2 | 0,05 | 0,1 | 0,1 | 3,0 x 10-4 |
| 3 | 0,05 | 0,3 | 0,1 | 9,0 x 10-4 |
Sabe-se que a reação tem ordem global igual a quatro. Com base nos resultados experimentais, é correto afirmar que os valores de ordem de reação para o consumo das substâncias A, B e C são, respectivamente,
Provas
O estanho é usado no revestimento de embalagens metálicas de alimentos. Sua obtenção pode ser feita por processo eletrolítico em soluções aquosas contendo cloreto de estanho (II).
A reação global do processo eletrolítico é Sn2+(aq) + 2 Cl–(aq) !$ \rightarrow !$ Sn (s) + Cl2 (g)
Dados:
Cl2 (g) + 2e– !$ \rightarrow !$ 2 Cl– (aq) Eº = + 1,36 V
Sn2+ (aq) + 2e– !$ \rightarrow !$ Sn (s) Eº = – 0,14 V
É correto afirmar que, na eletrólise de uma solução aquosa 1,0 mol. L–1 de cloreto de estanho (II) a 25 ºC, o produto formado no catodo, o potencial teórico aplicado e a polaridade do anodo são, respectivamente,
Provas
A determinação de monóxido de carbono em amostras gasosas pode ser feita por meio da passagem da mistura gasosa contendo CO por um absorvedor sólido aquecido a 150 ºC contendo I2O5. Forma-se iodo elementar e dióxido de carbono (reação I). O iodo é destilado e absorvido em uma solução aquosa de tiossulfato de sódio com concentração conhecida.
I2(g) + 2 S2O3 2–(aq) !$ \rightarrow !$ 2I–(aq) + S4O6 2–(aq) (reação II)
O excesso de tiossulfato é retrotitulado e, dessa forma, a quantidade de monóxido de carbono é indiretamente determinada.
A soma dos menores valores inteiros dos coeficientes estequiométricos da equação de reação I e o agente oxidante da reação II são, respectivamente,
Provas
Para a preparação de uma solução em um balão volumétrico com capacidade de 250 mL adicionaram-se 50 mL de uma solução de nitrato de alumínio, 0,10 mol.L–1 e 25 mL de uma solução de ácido nítrico 0,10 mol.L–1. Completou-se o volume até o traço de aferição com água destilada.
As concentrações, em mol.L–1, dos íons alumínio e nitrato na solução preparada são, respectivamente,
Provas
Dissolveu-se 23,25 g de anilina (C6H5NH2) em água (pH = 7,0) purificada por processo de destilação e deionização. Transferiu-se essa solução quantitativamente para um balão volumétrico de capacidade 1 000 mL e completou-se o volume até o traço de aferição a 25 ºC. O pH da solução final é igual a
Dado:
Constante de Basicidade da anilina a 25 ºC Kb !$ \cong !$ 4 x 10–10
Provas
Preparou-se uma mistura reacional adicionando-se um mol de cloreto de amônio e um mol de carbonato de sódio a um litro de água destilada. Após a solubilização completa dos sais foi atingido o equilíbrio reacional.
Considerando-se as espécies que interagem com a água, após atingido o equilíbrio químico, obteve-se na solução a preponderância da concentração de
Provas
Em um acidente envolvendo incêndio em um laboratório químico ocorreu o vazamento de um frasco de mercúrio, e sua vaporização resultou em uma pressão parcial de mercúrio estimada em 10–1 atm. Considerando-se que a temperatura no momento do acidente atingiu 1200 K, o total de átomos de mercúrio, por litro (átomos . L–1) no ambiente do acidente, era de aproximadamente
Dados:
R = 0,082 atm . L . mol–1 . K–1
Constante de Avogadro 6,0 x 10+23 mol–1
Provas
A teoria dos orbitais moleculares foi a ferramenta teórica que esclareceu o que era observado experimentalmente, quanto ao caráter magnético da molécula de oxigênio. Por meio dessa teoria, pode-se também determinar a ordem de ligação de espécies.
Considerando-se as moléculas de O2, CO e NO, a que apresenta caráter magnético diferente das demais e a que apresenta menor valor de ordem de ligação são, respectivamente,
Provas
Uma indústria gera efluente líquido industrial com características orgânicas biodegradáveis. Essa indústria lança seus efluentes líquidos sem tratamento em um corpo hídrico receptor classe 2. A montante do lançamento está a zona de águas limpas. As zonas de autodepuração de matéria orgânica biodegradável no corpo hídrico ocorrem de acordo com o tempo do lançamento e ao longo do corpo hídrico receptor.
Considere as afirmações seguintes:
I. A zona de degradação ocorre logo após o lançamento do efluente líquido. A concentração de matéria orgânica é alta.
II. Na zona de recuperação, a matéria orgânica que foi intensamente consumida na fase anterior já está estabilizada. O consumo de oxigênio está mais reduzido que na fase de decomposição ativa.
III. A zona de decomposição ativa é caracterizada pela elevada atividade bacteriana que atua na decomposição aeróbia da matéria orgânica e por concentração de oxigênio próxima da saturação.
Está correto apenas o contido em
Provas
Caderno Container