Foram encontradas 13.431 questões.
Na busca de novos métodos de análise para aplicação em triagem de amostras de águas, um técnico de laboratório estudou a reatividade de nitratos metálicos em meio ácido e básico. Em tubos de ensaio contendo soluções aquosas de nitratos metálicos, relacionados na tabelas a seguir, foram adicionadas, gota a gota, cerca de 2 mL de soluções dos reagentes HCl, H2SO4 e NH4OH 30%, separadamente.
|
Sal (solução aquosa 0,2 mol/L) |
|
AgNO3 |
|
Sr(NO3)2 |
|
Mg(NO3)2 |
|
Al(NO3)3 |
|
Pb(NO3)2 |
Considere o gráfico a seguir, que mostra a variação de solubilidade do Al(NO3)3 em função do pH, a 25 ºC.
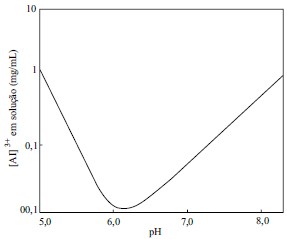
De acordo com o gráfico, para se obter o máximo rendimento na obtenção de Al(OH)3 a partir de uma solução que contém Al(NO3)3, será necessário manter o pH do meio reacional
Provas
Na busca de novos métodos de análise para aplicação em triagem de amostras de águas, um técnico de laboratório estudou a reatividade de nitratos metálicos em meio ácido e básico. Em tubos de ensaio contendo soluções aquosas de nitratos metálicos, relacionados na tabelas a seguir, foram adicionadas, gota a gota, cerca de 2 mL de soluções dos reagentes HCl, H2SO4 e NH4OH 30%, separadamente.
|
Sal (solução aquosa 0,2 mol/L) |
|
AgNO3 |
|
Sr(NO3)2 |
|
Mg(NO3)2 |
|
Al(NO3)3 |
|
Pb(NO3)2 |
Assinale a alternativa que contém, entre as equações apresentadas a seguir, aquela que descreve corretamente a reação que ocorre entre o nitrato de alumínio e o ácido sulfúrico.
Provas
Na busca de novos métodos de análise para aplicação em triagem de amostras de águas, um técnico de laboratório estudou a reatividade de nitratos metálicos em meio ácido e básico. Em tubos de ensaio contendo soluções aquosas de nitratos metálicos, relacionados na tabelas a seguir, foram adicionadas, gota a gota, cerca de 2 mL de soluções dos reagentes HCl, H2SO4 e NH4OH 30%, separadamente.
|
Sal (solução aquosa 0,2 mol/L) |
|
AgNO3 |
|
Sr(NO3)2 |
|
Mg(NO3)2 |
|
Al(NO3)3 |
|
Pb(NO3)2 |
Nas reações realizadas, é correto afirmar que ocorreu formação de precipitado quando o ácido clorídrico foi adicionado aos tubos de ensaio contendo
Provas
Em um laboratório de química, um estagiário localiza em uma parede um sinal como o que está representado a seguir.

Esse sinal indica
Provas
Um técnico de laboratório precisa preparar sulfato de manganês (II) anidro. Para isso, ele vai utilizar sulfato de manganês (II) monoidratado e proceder às seguintes etapas:
1. colocar um cadinho limpo para aquecer sobre a chama de um bico de Bunsen, ajustando o sistema de modo que o cadinho fique posicionado sobre a região mais quente da chama;
2. aquecer por 5 minutos e, em seguida, usando pinças, colocar o cadinho para esfriar sobre a bancada;
3. depois que o cadinho tiver esfriado (temperatura ambiente), pesar e registrar sua massa em milésimos de grama;
4. colocar 1,0 – 1,2 g de sulfato de manganês monoidratado no cadinho, pesar e registrar a massa em milésimos de grama;
5. aquecer por 5 minutos, interromper o aquecimento e repetir os processos descritos nas etapas 2 e 3;
6. repetir a etapa 5 até obter massa constante;
7. tampar o cadinho e, usando pinças e luvas, colocá-lo em um dessecador, até o momento de uso do sulfato de manganês anidro.
Sabendo que foram utilizados 0,165 g de sulfato de manganês monoidratado e que o processo de desidratação foi completo, a massa de sal anidro obtida é igual a
Provas
Um técnico de laboratório precisa preparar sulfato de manganês (II) anidro. Para isso, ele vai utilizar sulfato de manganês (II) monoidratado e proceder às seguintes etapas:
1. colocar um cadinho limpo para aquecer sobre a chama de um bico de Bunsen, ajustando o sistema de modo que o cadinho fique posicionado sobre a região mais quente da chama;
2. aquecer por 5 minutos e, em seguida, usando pinças, colocar o cadinho para esfriar sobre a bancada;
3. depois que o cadinho tiver esfriado (temperatura ambiente), pesar e registrar sua massa em milésimos de grama;
4. colocar 1,0 – 1,2 g de sulfato de manganês monoidratado no cadinho, pesar e registrar a massa em milésimos de grama;
5. aquecer por 5 minutos, interromper o aquecimento e repetir os processos descritos nas etapas 2 e 3;
6. repetir a etapa 5 até obter massa constante;
7. tampar o cadinho e, usando pinças e luvas, colocá-lo em um dessecador, até o momento de uso do sulfato de manganês anidro.
Na figura a seguir, estão representados alguns materiais de uso em laboratórios químicos.
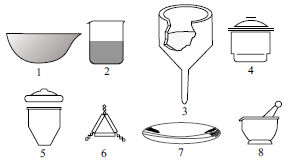
Entre os materiais apresentados na figura, para realizar a prática de acordo com o processo descrito, o técnico utilizará aqueles indicados pelos números
Provas
Quanto ao controle e prevenção da poluição do ar, aplicam-se diversas técnicas de coleta e análise dos poluentes.
Com relação a essas técnicas, pode-se afirmar corretamente que
Provas
Em relação ao controle e à prevenção da poluição ambiental, é correto afirmar que
Provas
Na classificação de produtos químicos, distingue-se entre 9 classes (e respectivas subclasses), nomeadamente as
CLASSE 1 – EXPLOSIVOS
CLASSE 2 – GASES
CLASSE 3 – LÍQUIDOS INFLAMÁVEIS
CLASSE 4 – SÓLIDOS INFLAMÁVEIS
CLASSE 5 – PERÓXIDOS ORGÂNICOS E OXIDANTES
CLASSE 6 – SUBSTÂNCIAS TÓXICAS E INFECTANTES
CLASSE 7 – MATERIAIS RADIOATIVOS
CLASSE 8 – CORROSIVOS
CLASSE 9 – SUBSTÂNCIAS PERIGOSAS DIVERSAS
As substâncias carbureto de cálcio, acetileno, nitrocelulose, peróxido de hidrogênio e acetona são classificadas, respectivamente, como produtos químicos das classes
Provas
Existe uma incompatibilidade entre produtos químicos que demandam atenção especial no seu manuseio ou transporte. Analise a tabela a seguir, em que são apresentadas substâncias e os seus respectivos produtos incompatíveis, classificando cada uma das informações como (V) verdadeira ou (F) falsa.
|
Substâncias |
Produtos Incompatíveis |
|
Amônia |
prata, sais de mercúrio |
|
Cianetos |
ácidos |
|
Cloratos |
sais de amônio, ácidos, metais em pó, enxofre |
|
Metais Alcalinos |
ácidos, oxidantes e peróxidos |
A classificação correta das informações, de cima para baixo, é:
Provas
Caderno Container