Foram encontradas 13.431 questões.
Provas
Abaixo são mostrados diferentes métodos de separação e as respectivas bases destes métodos.
Método de Separação:
1) Precipitação e filtração.
2) Destilação.
3) Extração.
4) Troca iônica.
5) Cromatografia.
6) Eletroforese.
7) Fracionamento por campo e fluxo.
Base do Método:
a) Diferenças na solubilidade dos compostos formados.
b) Diferenças na velocidade de migração de espécies com carga em um campo elétrico.
c) Diferenças na interação de reagentes com uma resina de troca iônica.
d) Diferenças na solubilidade em dois líquidos imiscíveis.
e) Diferenças na interação com um campo ou gradiente aplicado perpendicularmente à direção de transporte.
f) Diferenças na volatilidade dos compostos.
g) Diferenças na velocidade de movimentação de solutos, passando por uma fase estacionária.
Associe o método de separação à sua base e indique a alternativa CORRETA.
Provas
Provas
A vanilina, 4-hidroxi-3-metoxibenzaldeído, fórmula C8H8O3, é responsável pelo aroma e sabor de baunilha, muito apreciados no mundo inteiro. É obtida tradicionalmente das vagens, também chamadas de favas, de uma orquídea tropical, a Vanilla planifolia.
A figura mostra um processo de extração da vanilina a partir de vagens de orquídea espalhadas sobre bandejas perfuradas, em tanques de aço, usando etanol (60% v/v) como solvente. Em geral, a extração dura duas semanas.
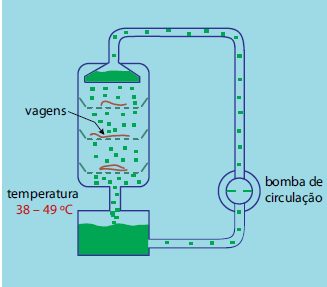
(www.greener-industry.org.uk. Adaptado.)
De acordo com o que mostra a figura, a extração da vanilina a partir de fontes naturais se dá por
Provas
No escoamento sobre uma superfície, os perfis de velocidade (u) e de temperatura (T) possuem as seguintes formas: u y = Ay + By2 + Cy3 – Dy4 e T y = E + Fy + Gy2 – Hy3.
Sabendo-se que os coeficientes de A até H são constantes, determine as expressões do coeficiente de atrito Cf e do coeficiente de convecção h em termos de u∞, de T∞, dos coeficientes apropriados dos perfis e das propriedades do fluido. Os coeficientes de atrito Cf e o de convecção h, em termos de u∞ e de T∞ são, respectivamente,
Provas
Provas
Provas
Provas
- Os métodos gravimétricos são quantitativos e se baseiam na determinação da massa de um composto puro ao qual o analito está quimicamente relacionado.
- A peptização é o processo no qual um coloide coagulado é lavado e permanece no seu estado coloidal.
- A coprecipitação é um processo no qual um precipitado é formado pela geração lenta de um reagente precipitante de forma homogênea em toda a solução.
- O tamanho das partículas do precipitado é influenciado por variáveis como a solubilidade do precipitado, a temperatura, as concentrações dos reagentes e a velocidade com que os reagentes são misturados.
Provas
Provas
Caderno Container