Foram encontradas 13.249 questões.
A figura a seguir representa um espectrofotômetro de feixe único com seus componentes principais (A-G).
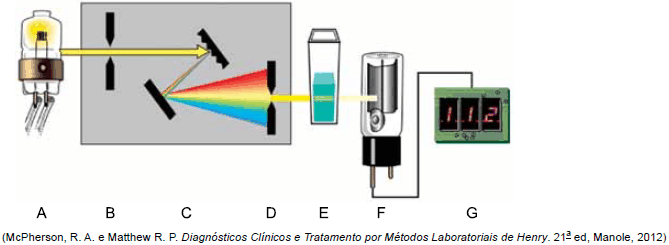
Assinale a alternativa que relaciona corretamente a letra ao componente do espectrofotômetro.
Provas
A velocidade de uma reação química é influenciada por diversos fatores como a superfície de contato, a temperatura do meio, a presença de catalisadores e a concentração de reagentes. A respeito do uso dos catalisadores nas reações químicas, assinale a opção INCORRETA.
Provas
Sobre a tabela periódica e as propriedades dos elementos, analise as afirmativas abaixo e assinale a opção correta.
I- Elementos com o peso atômico maior que 83 são considerados radioativos.
II- O césio (Cs) é um metal alcalino.
III- O elemento que tem a distribuição eletrônica [Ar] 3d10 4s2 4p2 pertence à família dos calcogênios.
IV- O mercúrio (Hg) é um metal líquido em condição ambiente (25ºC e 1atm).
V- O hélio (He) é o elemento da tabela periódica que possui o menor raio atômico e maior eletropositividade.
Provas
Com o objetivo de se evitarem erros na comunicação dos nomes das substâncias, foram padronizadas regras para que ocorra a correta identificação. Assim, assinale a opção que apresenta a nomenclatura correta associada à sua respectiva fórmula química.
Provas
A corrosão é uma reação química comum, presente nos navios pelo fato de se ter materiais metálicos expostos à água do mar. Esse processo resulta na deterioração dos materiais metálicos, como o ferro (Fe), com a formação de ferrugem. A reação do ferro (Fe) com o oxigênio (O2) forma óxido de ferro (Fe2O3). Essa reação é representada pela equação não-balanceada a seguir:
Fe(s) + O2(g) → Fe2O3
Considerando que foram gastos 140g de Fe(s) na reação completa, qual será a massa de Fe2O3 formada?
Dados: massa molar do O2: 32 g/mol, massa molar do Fe: 56 g/mol.
Provas
Examine a representação abaixo.
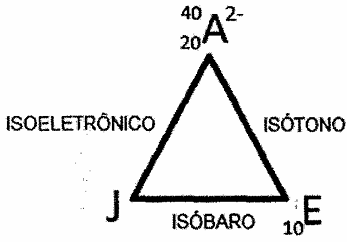
Considere a representação acima e as relações entre os átomos hipotéticos A, E e J. Sabe-se que A e E são isótonos, E. e J são isóbaros, J e A são isoeletrônicos e que os átomos J e E são eletricamente neutros. Sendo assim, determine o número de nêutrons (n) do átomo J e assinale a opção correta.
Provas
Um cientista misturou água e cloreto de prata em um recipiente. Após algum tempo em repouso, ele percebeu que a mistura resultante era heterogênea: uma fase liquida, predominantemente de água, e uma fase sólida, predominantemente de cloreto de prata. Para a separação dessa mistura, qual é o processo mais indicado?
Provas
Disciplina: Engenharia Química
Banca: MS CONCURSOS
Orgão: SAAE-São Carlos-SP
O monitoramento constante da concentração de nitratos, (NO3-), na água, é fundamental para garantir a qualidade de acordo com as normas ambientais. Qual dos equipamentos seria o mais adequado para realizar a quantificação precisa dessas espécies?
Provas
A reação do antibiótico sulfanilamida com halogênios leva à reação de substituição com o halogênio em duas posições distintas do anel aromático, como representado na equação não balanceada a seguir.
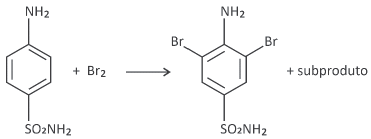
Em um experimento, 1 L de uma solução de sulfanilamida de pH 5 reagiu com Br2 em excesso, obtendo-se pH 4 após reação total. Considerando que o volume se manteve inalterado após a adição do halogênio, quantos mols de sulfanilamida reagiram com bromo?
Provas
A toxicidade do Pb e o risco de sua ingestão ganharam notoriedade na mídia devido à presença desse elemento em copos térmicos amplamente comercializados. A exposição ao Pb, no entanto, pode ocorrer também por fontes naturais, como a ingestão de água em contato prolongado com minérios como a anglesita, rico em PbSO4 (Kps = 1,0 × 10-8). Sabendo que a legislação estabelece a concentração máxima de Pb de 0,01 mg/L para água potável, assinale a alternativa correta em relação à ingestão de água que tenha contato prolongado com a anglesita.
Provas
Caderno Container