Foram encontradas 13.259 questões.
As reações mais características de alcenos e alcinos são as reações de adição, nas quais um reagente é adicionado aos dois átomos que formam a ligação múltipla. Considere as diferentes reações de adição, para a molécula de etileno, descritas a seguir:
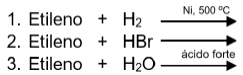
Considerando essas reações de adição, assinale a alternativa que apresenta, respectivamente, as substâncias formadas a partir das reações descritas em 1, 2 e 3.
Provas
A teoria da repulsão de pares de elétrons na camada de valência (VSEPR, do inglês "valence shell electron-pair repulsion") permite prever a geometria de moléculas. Acerca desse assunto, assinale a alternativa que apresenta a correta descrição da geometria molecular das seguintes moléculas: CH4, NH3 e SeCl4, respectivamente.
Provas
Dentre os combustíveis mais utilizados nos automóveis está a gasolina, cujo componente majoritário é o octano (C8H18). A equação química de combustão completa do octano (não balanceada) é representada a seguir:
C8H18(l) + O2(g) → CO2(g) + H2O(g)
Considerando a reação de combustão completa de 5,0 g de C8H18, assinale a alternativa que apresenta todos os coeficientes estequiométricos (na ordem da reação apresentada), como números inteiros, e a massa (gramas) de O2, respectivamente.
Provas
Em relação às normas de biossegurança em laboratórios, envolvendo a manipulação de substâncias tóxicas (gases, líquidos e sólidos) e o conhecimento acerca destas, analise as assertivas e assinale a alternativa que aponta a(s) correta(s).
I. Solventes orgânicos, como etanol, metanol, hexano, tetracloreto de carbono e diclorometano, são líquidos inflamáveis.
II. O formaldeído, à temperatura ambiente, é um gás inflamável, tóxico por ingestão, por contato com a pele e por inalação e é um agente comprovadamente cancerígeno aos seres humanos.
III. Os ácidos concentrados: ácido nítrico, ácido clorídrico e ácido sulfúrico devem ser manipulados dentro da capela de exaustão, pois seus vapores são tóxicos para o sistema respiratório e possuem ação corrosiva quando em contato com a pele.
Provas
Uma amostra de plasma foi analisada por volumetria de precipitação para se determinar o teor de íons cloretos. Após o tratamento adequado dessa amostra, uma alíquota de 10 ml foi titulada com nitrato de prata 0,050 mol/L consumindo 15,00 ml do titulante até atingir o ponto final. Considerando essas informações, assinale a alternativa que apresenta a porcentagem (%, m/v), aproximada, de íon cloreto nessa amostra.
Dado: massa molar do cloro (Cl) = 35 g/mol.
Provas
Considere as seguintes substâncias no estado gasoso: gás cloro, gás amônia, gás cloreto de hidrogênio, gás flúor e gás propano, as quais estão contidas em diferentes frascos fechados, de mesma capacidade, sob as mesmas condições de pressão e temperatura (1 atm e 25 °C). Ao abrir todos os frascos simultaneamente, os gases irão se difundir para o ambiente atmosférico, sob as mesmas condições iniciais. Tendo em vista essas informações e considerando que essas substâncias se comportam como gases ideais, assinale a alternativa que apresenta o gás que se difundirá mais rapidamente.
Dados de massas atômicas: H (1 u); C (12 u); N (14 u); F (19 u); Cl (35 u).
Provas
Para o procedimento de assepsia de materiais cirúrgicos, foi preparada uma solução de etanol 77% (v/v). Diante dessa informação e sabendo que essa solução possui densidade igual a 0,79 g/ml, assinale a alternativa correta.
Provas
Foram preparados 100 ml de uma solução de ácido clorídrico a partir da solução do ácido concentrado. Para isso, foram transferidos 2,0 ml do HCl concentrado para um balão volumétrico (100 ml), avolumando-o com água destilada. O rótulo do ácido clorídrico concentrado apresenta as seguintes informações:
• massa molar = 36 g/mol;
• pureza = 37% (m/m);
• densidade = 1,2 g/ml.
Considerando essas informações, assinale a alternativa que apresenta a concentração (mol/L), aproximada, da solução de HCl que foi preparada.
Provas
Joaquim, estudante do 9º ano do Ensino Fundamental, aprendeu que a densidade é uma propriedade dos corpos. À densidade é determinada pela equação \( d = { \large m \over V} \) , onde \( m \) é a massa de um corpo e \( V \) é o volume ocupado por este. O quadro abaixo apresenta os valores de densidade de alguns metais:
| Metal | Densidade (g/mL) |
| Alumínio | 2,7 |
| Titânio | 4,5 |
| Estanho | 7,2 |
| Prata | 10,5 |
| Mercúrio | 13,5 |
Desejando saber de que material era feito um determinado objeto metálico, Joaquim mediu sua massa, obtendo o valor de 90 g. O volume foi medido utilizando uma proveta contendo inicialmente 50 mL de água, sendo que o volume aumentou para 70 mL quando o objeto foi mergulhado nela. Portanto, Joaquim concluiu corretamente que o objeto é feito de:
Provas
Dado o contexto de Hemograma, associe as colunas relacionando Índices hematimétricos com suas respectivas características e definições:
Coluna 1:
A.Volume corpuscular médio.
B.Hemoglobina corpuscular média.
C.Concentração de hemoglobina corpuscular média.
Coluna 2:
(__)É a percentagem de hemoglobina em 100ml de hemácias.
(__)Representa o quociente de conteúdo de hemoglobina em um determinado volume de hemácias pelo nº de células contidas no mesmo volume.
(__)Representa o quociente de um determinado volume de hemácias pelo número de células contidas no mesmo volume.
Assinale a alternativa cuja a sequência da associação, de cima para baixo, esteja CORRETA:
Provas
Caderno Container