Foram encontradas 13.259 questões.
Um compressor trabalhando adiabaticamente e com uma eficiência de 80%, comprime vapor saturado de 100 kPa a 300 kPa e necessita de 650 kJ para comprimir 10 kg deste vapor. Se a compressão for conduzida agora de forma adiabática e isentrópica, o trabalho necessário para comprimir a mesma quantidade de vapor saturado, em kJ, é de
Provas
Questão presente nas seguintes provas
Um gás ideal, com capacidades caloríficas constantes, passa pela seguinte sequência de processos mecanicamente reversíveis em um sistema fechado:
1. de um estado inicial a 100 ºC e 1 bar, é comprimido adiabaticamente até 150 ºC;
2. em seguida, é resfriado de 150 ºC a 100 ºC, a pressão constante;
3. finalmente, é expandido isotermicamente até o seu estado original.
Para o ciclo completo, as variações de energia interna (!$ Delta U !$) e entalpia (!$ Delta H !$) são
Provas
Questão presente nas seguintes provas
Um tanque, inicialmente sob vácuo, é preenchido com um gás proveniente de uma linha com pressão constante. Desprezando-se a transferência de calor entre o gás e o tanque e as variações de energia cinética e potencial, a relação entre a entalpia específica do gás na linha de entrada (HE) e a energia interna específica do gás no interior do tanque, após o enchimento (U), é
Provas
Questão presente nas seguintes provas
A utlização do eletrodo de Ag/AgCl pode ser tanto como eletrodo de referência quanto como eletrodo indicador.
PORQUE
O eletrodo Ag/AgCl tem um potencial conhecido, que é essencialmente constante e insensível à composição das soluções de estudo, sendo, ainda, construído com base em uma reação reversível; obedece à Equação de Nerst, pode retornar ao seu potencial original após ser submetido a pequenas correntes e exibe baixa histerese sob ciclos de temperatura.
A esse respeito, conclui-se que
Provas
Questão presente nas seguintes provas
Uma solução de uma dada amostra apresenta absortividade de 200 L•mol–1•cm–1. Foi analisada por espectroscopia na região do UV/Vis em um comprimento de onda na qual se obedece à lei Lambert Beer na concentração empregada nesse experimento. Considere que o caminho óptico é de 1 mm, e a absorbância observada é 0,4. Empregando esse resultado na equação de Lambert-Beer, conclui-se que a concentração da amostra é, aproximadamente,
Provas
Questão presente nas seguintes provas
Para se determinar o teor de cloreto em 1 litro de uma solução salina pelo método de Volhard, retirou-se uma alíquota de 25 mL da mesma, que foi tratada com 40 mL de uma solução padrão de nitrato de prata com concentração 0,150 M. Após a precipitação quantitativa do cloreto na forma de AgCl, titulou-se o excesso de prata remanescente com uma solução padrão de KSCN 0,200 M, contendo íons Fe3+ como indicador. O volume de titulante gasto para se atingir o ponto de equivalência foi de 5 mL.
Com base nesses dados, conclui-se que a massa de cloro presente na forma de cloreto na solução inicial é, aproximadamente, de
Provas
Questão presente nas seguintes provas
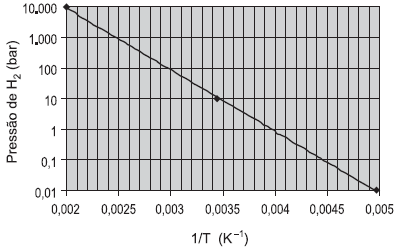
O armazenamento de hidrogênio em volumes reduzidos pode ser conseguido por meio da formação de hidretos metálicos. O gráfico de Van’t Hoff apresentado acima exibe a pressão de equilíbrio de hidrogênio, em função da temperatura para a seguinte reação:
Be + H2 !$
ightarrow !$ BeH2
Qual a variação de entalpia, em kJ, estimada para essa reação?
Dado: (R = 8 J•mol−1•K−1; ln 10 = 2,3)
Provas
Questão presente nas seguintes provas
Soluções de permanganato de potássio utilizadas em titulações são frequentemente padronizadas por reação com ácido oxálico. Qual a relação molar de permanganato/ ácido oxálico dessa reação?
Provas
Questão presente nas seguintes provas
O abaixamento crioscópico do benzeno é utilizado na indústria do petróleo para medir massas molares de solutos. A equação que rege esse fenômeno pode ser expressa por:
!$ In(x_1)={large{Delta_fH over R}} left({large{1 over T_0}}-{large{1 over T}}
ight) !$
Sabe-se que:
• !$ x_1 !$ é a fração molar de solvente em solução que cristaliza na temperatura T;
• !$ Delta_f H !$ e !$ T_0 !$ são, respectivamente, a variação de entalpia e a temperatura de fusão do solvente puro;
• R é a constante universal dos gases que pode ser aproximada por 2 cal/(mol•K);
• a variação de entropia de fusão do benzeno puro é 8 cal/(mol•K);
• a massa molar do benzeno é 78 g/mol;
• a temperatura de fusão do benzeno (!$ T_0 !$) é 278,5 K.
A massa molar do soluto, a 278 K, necessária para a cristalização do benzeno a partir de uma solução de 10 g de soluto em 780 g de benzeno, em g/mol, é
Dado:!$ lim_{y
ightarrow 0} (In(1-y))cong -y !$
Provas
Questão presente nas seguintes provas

A figura acima apresenta dados experimentais de tensão superficial em função da concentração de surfactante (tenso-ativo) não iônico. Notam-se duas regiões distintas, uma de 0 a 0,003 M, e outra para concentrações acima de 0,005 M. A partir de uma análise, conclui-se que
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container