Foram encontradas 35.978 questões.
As embalagens comerciais de sal de cozinha apresentam um aditivo antiaglomerante. Trata-se de um sal solúvel em água formado entre o cátion potássio e o íon complexo hexacianoferrato(II), Kx [Fe(CN)6 ].
O número que representa x na fórmula do hexacianoferrato(II) de potássio e a quantidade em mols de íons na solução formada pela dissolução de um mol desse sal são, respectivamente,
Provas
 (Ciencias_Natureza_Nova_Eja_Aluno_Mod02_Vol01_Vol02_Ok.indb)
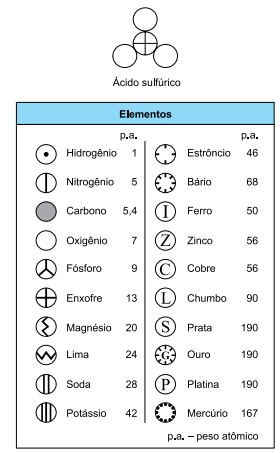
(Ciencias_Natureza_Nova_Eja_Aluno_Mod02_Vol01_Vol02_Ok.indb) Considerando os elementos representados no quadro e seus respectivos pesos atômicos definidos à época dos estudos de Dalton, a razão entre as massas da molécula do ácido sulfúrico, H2 SO4 , calculada a partir dos dados atuais apresentados na Classificação Periódica, e o ácido sulfúrico de Dalton, calculada a partir de seus pesos atômicos, é de
Provas
A tabela apresenta o poder calorífico por massa de dois combustíveis, metano e hidrogênio.
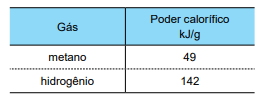
Sabendo que nas CATP o volume molar de qualquer gás é 25 L/mol, a quantidade de energia gerada pela queima de 1 kg de gás metano equivale à energia gerada pela queima do volume de gás hidrogênio nas CATP de, aproximadamente:
Provas
Considere as imagens a seguir que demonstram fenômenos observados em líquidos.

(Atkins, Peter; Loretta, Jones; Laverman, Leroy. Princípios de Química: questionando a vida moderna e o meio ambiente, 2006)
A formação do menisco no tubo de vidro contendo o mercúrio evidencia que as forças de coesão dos átomos no interior do líquido são___________ do que as forças de adesão dos átomos do metal à superfície do vidro. Já a ____________tensão superficial entre as moléculas da água causam a forma esférica das gotas sobre a superfície encerada.
As lacunas do texto são, correta e respectivamente, preenchidas por:
Provas
Provas
1) Liberação do cloro a partir da ação dos raios ultravioleta:
CF2Cl2 → CF2Cl + Cl
2) Reação do átomo de cloro com o ozônio:
Cl + O3 → ClO + O2
3) Reação do monóxido de coro com oxigênio livre formando gás oxigênio e liberando o cloro livre:
ClO + O → O2 + Cl
4) Após essas reações, o cloro, que não é consumido nas reações, fica livre para reagir com mais ozônio, participando da destruição da camada.
Considerando as informações, verifica-se que nessa sequência de reações os átomos de cloro
Provas
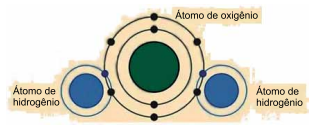
(https://www.todamateria.com.br/ligacoes-quimicas/. Adaptado)
Esse tipo de ligação apresenta como característica
Provas
Provas
Provas
Provas
Caderno Container