Foram encontradas 36.142 questões.
O nitrogênio forma diversos óxidos que interagem na atmosfera de forma variada. A seguir são dadas as equações termoquímicas envolvendo espécies nitrogenadas.
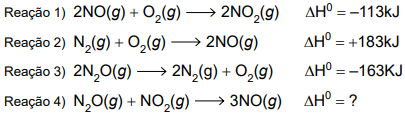
A variação da entalpia da reação 4 é igual a
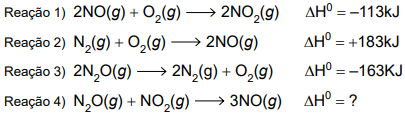
A variação da entalpia da reação 4 é igual a
Provas
Questão presente nas seguintes provas
Na combustão de 0,01 mol de um composto orgânico constituído apenas por carbono, hidrogênio e oxigênio foram formados 0,12 mol de CO2 e 0,08 mol de H2O. Descobriu-se, por meio de outras técnicas analíticas, que a massa de oxigênio nesse composto corresponde ao dobro de massa de hidrogênio que ele contém.
A fórmula mínima desse composto é
A fórmula mínima desse composto é
Provas
Questão presente nas seguintes provas
A figura representa, esquematicamente, o poder de penetração das três principais emissões radioativas naturais em três diferentes materiais. 1 2 3 papel aço chumbo
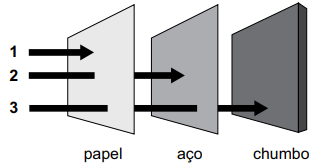
(Arquivo pessoal; imagem usada com autorização)
As emissões radioativas 1, 2 e 3 são, respectivamente,

(Arquivo pessoal; imagem usada com autorização)
As emissões radioativas 1, 2 e 3 são, respectivamente,
Provas
Questão presente nas seguintes provas
A molécula de oxigênio (O2) apresenta comportamento paramagnético, sendo atraída por campos magnéticos, o que indica a presença de elétrons desemparelhados em sua estrutura.
A explicação para o comportamento paramagnético da molécula de oxigênio é dada pela teoria
A explicação para o comportamento paramagnético da molécula de oxigênio é dada pela teoria
Provas
Questão presente nas seguintes provas
A figura representa um diagrama das entalpias envolvidas na formação de uma solução aquosa a partir de um soluto sólido iônico cristalino.
A entalpia de solução (∆Hsol) é o resultado da soma da entalpia de rede cristalina (∆HL) e a entalpia de hidratação (∆Hhid)
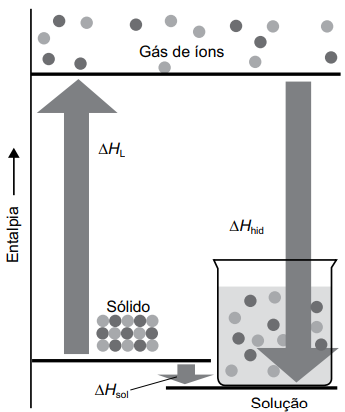
(ATKINS, Peter; LORETTA, Jones, LAVERMAN, Leroy. Princípios de Química: questionando a vida moderna e o meio Ambiente. 2. ed. Porto Alegre: Bookman, 2006)
A tabela apresenta os valores, em módulo, de entalpia de rede (∆HL) e entalpia de hidratação (ΔHhid) de alguns sais.
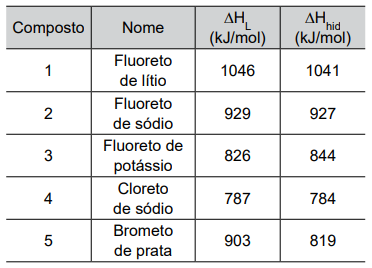
(ATKINS, Peter; LORETTA, Jones, LAVERMAN, Leroy. Princípios de Química: questionando a vida moderna e o meio Ambiente. 2. ed. Porto Alegre: Bookman, 2006)
O diagrama de energia da figura é compatível ao processo de dissolução do composto
A entalpia de solução (∆Hsol) é o resultado da soma da entalpia de rede cristalina (∆HL) e a entalpia de hidratação (∆Hhid)

(ATKINS, Peter; LORETTA, Jones, LAVERMAN, Leroy. Princípios de Química: questionando a vida moderna e o meio Ambiente. 2. ed. Porto Alegre: Bookman, 2006)
A tabela apresenta os valores, em módulo, de entalpia de rede (∆HL) e entalpia de hidratação (ΔHhid) de alguns sais.

(ATKINS, Peter; LORETTA, Jones, LAVERMAN, Leroy. Princípios de Química: questionando a vida moderna e o meio Ambiente. 2. ed. Porto Alegre: Bookman, 2006)
O diagrama de energia da figura é compatível ao processo de dissolução do composto
Provas
Questão presente nas seguintes provas
A Teoria da Repulsão dos Pares de Elétrons da Camada de Valência (Valence Shell Electron Pair Repulsion ou VSEPR) é utilizada para prever a geometria molecular com base na repulsão entre pares de elétrons ao redor do átomo central.
A representação AX3E2 (em que E representa par de elétrons não ligados) corresponde a uma molécula polar com formato de T, e um exemplo dessa molécula é:
A representação AX3E2 (em que E representa par de elétrons não ligados) corresponde a uma molécula polar com formato de T, e um exemplo dessa molécula é:
Provas
Questão presente nas seguintes provas
As estruturas ressonantes são representações alternativas das ligações químicas de uma mesma molécula ou íon que não podem ser descritos adequadamente por uma única estrutura de Lewis e são mais bem representados por um híbrido de ressonância.
Assinale a alternativa que apresenta a fórmula de uma espécie química que tem uma forma híbrida de ressonância para representação de suas ligações químicas por meio do modelo de Lewis.
Assinale a alternativa que apresenta a fórmula de uma espécie química que tem uma forma híbrida de ressonância para representação de suas ligações químicas por meio do modelo de Lewis.
Provas
Questão presente nas seguintes provas
O frâncio é um elemento químico radioativo extremamente raro, sendo o segundo menos abundante na natureza, atrás apenas do astato. Enquanto o frâncio pertence ao grupo dos metais alcalinos, o astato integra o grupo 17 da tabela periódica.
Considerando as propriedades características dos elementos desses grupos, é possível prever que o íon frâncio apresenta um estado de oxidação estável _______________ e forma um óxido _______________. Além disso, um composto hipotético entre frâncio e astato teria fórmula mínima com proporção estequiométrica _______________.
As lacunas são preenchidas, correta e respectivamente, por
Considerando as propriedades características dos elementos desses grupos, é possível prever que o íon frâncio apresenta um estado de oxidação estável _______________ e forma um óxido _______________. Além disso, um composto hipotético entre frâncio e astato teria fórmula mínima com proporção estequiométrica _______________.
As lacunas são preenchidas, correta e respectivamente, por
Provas
Questão presente nas seguintes provas
A equação de reação não balanceada refere-se a uma síntese de um composto de vanádio utilizado como catalisador em reações orgânicas.
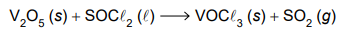
A soma dos coeficientes estequiométricos dessa reação balanceada com a participação de 1 mol de V2 O5 é igual a
A soma dos coeficientes estequiométricos dessa reação balanceada com a participação de 1 mol de V2 O5 é igual a
Provas
Questão presente nas seguintes provas
Os combustíveis renováveis têm ganhado destaque na matriz energética mundial devido à busca por alternativas sustentáveis aos combustíveis fósseis.
Um combustível considerado renovável é:
Um combustível considerado renovável é:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container