Foram encontradas 36.174 questões.
O controle de qualidade de fármacos pode ser feito
utilizando técnicas cromatográficas, como a
cromatografia líquida de alta eficiência (HPLC, da
sigla em inglês High-Performance Liquid
Chromatography). Um sistema desse tipo
geralmente inclui um suporte e uma fase
estacionária contidos numa coluna, em que uma
fase móvel líquida é injetada por meio de uma
bomba. Um dispositivo de injeção insere as
amostras na entrada, e um detector monitora e
mede os analitos na saída da coluna. O que torna
possível a separação e a identificação dos analitos
é
Provas
Questão presente nas seguintes provas
Quando os átomos de uma amostra se encontram livres no estado gasoso e recebem energia térmica
suficiente, eles sofrem uma transição para um estado de energia mais alto, o estado excitado. Quando esses
átomos retornam ao seu estado fundamental, liberam radiação eletromagnética com energia e comprimento
de onda característicos dessa transição em particular e do tipo de átomo que gera a transição. A técnica
analítica que se fundamenta na leitura dos espectros produzidos por essa radiação é chamada:
Provas
Questão presente nas seguintes provas
O permanganato de potássio (KMnO4) é um agente oxidante forte amplamente usado em análises químicas.
Sua concentração em uma solução pode ser determinada utilizando a espectrofotometria na faixa do espectro
visível, em um comprimento de onda (λ) igual a 525 nm. Nesse comprimento de onda, uma solução de KMnO4
apresenta um valor de absorbância (A) igual a 0,800. Considerando um caminho óptico (b) de 2,0 cm e uma
absortividade molar (ε) igual a 2,0 X 103 L.mol-1
.cm-1
, a concentração (C) de KMnO4, em mol.L-1
, nessa
solução é de:
Provas
Questão presente nas seguintes provas
A emissão do gás carbônico, CO2, acarreta impactos ambientais relacionados a alterações climáticas,
desequilíbrio do efeito estufa, poluição do ar, formação de chuva ácida etc. Combustíveis derivados do
petróleo, que, ao serem queimados, produzem CO2 são especialmente problemáticos do ponto de vista
ambiental, em razão de serem derivados de uma fonte de energia não renovável. O propano, C3H8, por
exemplo, é um gás derivado do petróleo presente na composição do GLP (gás liquefeito do petróleo,
popularmente chamado de gás de cozinha), presente nos botijões para uso doméstico e industrial.
Considerando que, na combustão completa do gás propano com gás oxigênio, O2, presente na proporção de
21% em volume de ar atmosférico, são produzidos exclusivamente gás carbônico, CO2, e água, H2O. Pode-se afirmar CORRETAMENTE que:
(considere: massas molares em g/mol: C = 12, H = 1, O = 16; volume molar em L/mol = 22,4)
C3H8 + 5 O2 → 3 CO2 + 4 H2O
(considere: massas molares em g/mol: C = 12, H = 1, O = 16; volume molar em L/mol = 22,4)
C3H8 + 5 O2 → 3 CO2 + 4 H2O
Provas
Questão presente nas seguintes provas
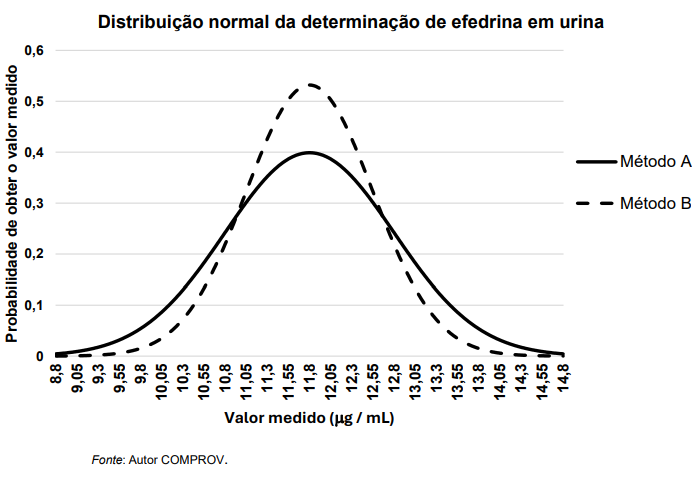
Alguns suplementos nutricionais dispõem de efedrina com a promessa de auxiliar na queima de gordura e
melhora do desempenho de atletas que fazem uso desses suplementos. Devido a seus efeitos, o COI (Comitê
Olímpico Internacional) incluiu a efedrina na lista de substâncias proibidas para atletas em competições
oficiais. No estudo de métodos para quantificação de efedrina, foram coletados dois conjuntos de dados a
partir de medições feitas por dois métodos diferentes, respectivamente, aplicados para uma mesma amostra
de urina de um voluntário usuário de efedrina. A partir dos conjuntos de dados, foram construídos gráficos de
distribuição normal para cada método proposto. Pode-se dizer que:

Provas
Questão presente nas seguintes provas
O National Institute of Standards and Technology indica a análise gravimétrica como uma técnica “padrão
ouro”, ou método de referência, para avaliar a exatidão de outras técnicas analíticas. Pode-se dizer que isso
se deve ao fato de que:
Provas
Questão presente nas seguintes provas
O potencial de uma célula galvânica mede a
força eletromotriz (fem) em volts da célula. A
relação do potencial da célula com as
concentrações de produtos e reagentes de
uma reação de oxirredução pode ser verificada
a partir da Equação de Nernst, apresentada
abaixo:
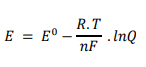
Onde:
E = potencial da célula;
E0 = potencial da célula nas condições padrão;
R = constante ideal dos gases;
T = Temperatura absoluta;
n = número de elétrons transferidos na reação;
F = constante de Faraday;
Q = Quociente de reação.
Em relação às aplicações da equação de Nernst, analise as assertivas:
I - Pode-se calcular o potencial da célula nas condições padrão, igualando o quociente de reação à constante de equilíbrio da reação.
II - O potencial da célula galvânica antes de atingir o equilíbrio é sempre positivo.
III - A condição de equilíbrio é alcançada quando o quociente da reação se torna igual a 1, pois o logaritmo natural de 1 é igual a 0, fazendo com que o potencial da célula se torne igual ao potencial padrão.
Considerando as assertivas, indique as proposições CORRETAS:
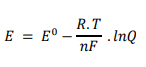
Onde:
E = potencial da célula;
E0 = potencial da célula nas condições padrão;
R = constante ideal dos gases;
T = Temperatura absoluta;
n = número de elétrons transferidos na reação;
F = constante de Faraday;
Q = Quociente de reação.
Em relação às aplicações da equação de Nernst, analise as assertivas:
I - Pode-se calcular o potencial da célula nas condições padrão, igualando o quociente de reação à constante de equilíbrio da reação.
II - O potencial da célula galvânica antes de atingir o equilíbrio é sempre positivo.
III - A condição de equilíbrio é alcançada quando o quociente da reação se torna igual a 1, pois o logaritmo natural de 1 é igual a 0, fazendo com que o potencial da célula se torne igual ao potencial padrão.
Considerando as assertivas, indique as proposições CORRETAS:
Provas
Questão presente nas seguintes provas
A constante de dissociação iônica em meio aquoso
aumenta com o aumento da temperatura.
Considerando que a constante de dissociação
iônica do ácido acético a 35 °C seja de 2,00.10-5
,
qual seria aproximadamente o pH de uma solução
0,05 M deste ácido a 35 °C?
Provas
Questão presente nas seguintes provas
O erro aleatório na coleta de dados está
relacionado a variações nas condições
experimentais, operações e leitura de
instrumentos que fogem ao controle do técnico
operador. Uma operação laboratorial realizada em
mais de uma etapa faz com que o erro se
propague. Um caso típico é a determinação da
densidade em que se tem o erro na medida de
massa e na medida de volume. Imagine que
durante um experimento, um técnico em química
precisa determinar a densidade de uma amostra
de um combustível. Ele mede a massa da amostra
e o volume correspondente. As medições foram:
• Massa: m = 40,0 g ± 0,025 g
• Volume: V = 50,0 mL ± 0,1 mL
Em relação à precisão das medidas e determinação da densidade, pode-se dizer que:
• Massa: m = 40,0 g ± 0,025 g
• Volume: V = 50,0 mL ± 0,1 mL
Em relação à precisão das medidas e determinação da densidade, pode-se dizer que:
Provas
Questão presente nas seguintes provas
Durante um experimento de laboratório, um
técnico em química precisa isolar e purificar 10g de
ácido benzoico. Sabendo que o ácido benzoico é
um sólido pouco solúvel em água fria, mas muito
solúvel em água quente. Qual dos seguintes
métodos é mais adequado para o propósito
descrito?
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container