Foram encontradas 35.922 questões.
Durante a preparação de uma solução padrão em um laboratório
de controle de qualidade, o analista precisa escolher um composto
adequado para atuar como padrão primário em uma titulação.
Para garantir a precisão dos resultados, esse composto deve atender a requisitos específicos, e uma característica que deve ser evitada é a elevada
Para garantir a precisão dos resultados, esse composto deve atender a requisitos específicos, e uma característica que deve ser evitada é a elevada
Provas
Questão presente nas seguintes provas
A corrosão metálica é um fenômeno eletroquímico espontâneo
que envolve reações simultâneas de oxidação e redução,
resultando na degradação gradual de materiais metálicos e
gerando impactos econômicos e operacionais relevantes na
indústria. Esse processo é acelerado quando metais estão em
contato com meios eletrolíticos condutores, especialmente na
presença de agentes oxidantes, como o oxigênio dissolvido em
soluções aeradas.
Considere o seguinte cenário:
1. Uma indústria conduz uma operação contínua, na qual uma solução aquosa eletrolítica aerada escoa pelo interior de uma tubulação de aço carbono, promovendo contato direto entre o fluido e a superfície metálica.
2. O processo apresenta corrosão localizada, evidenciada pela redução irregular de espessura da parede metálica e pela formação de óxidos superficiais aderidos, indicando atividade eletroquímica heterogênea ao longo do duto.
3. O oxigênio dissolvido na solução participa da semirreação catódica, atuando como o principal receptor de elétrons no mecanismo de corrosão em meio aquoso não ácido.
Com base nessas observações, assinale a afirmativa incorreta.
Considere o seguinte cenário:
1. Uma indústria conduz uma operação contínua, na qual uma solução aquosa eletrolítica aerada escoa pelo interior de uma tubulação de aço carbono, promovendo contato direto entre o fluido e a superfície metálica.
2. O processo apresenta corrosão localizada, evidenciada pela redução irregular de espessura da parede metálica e pela formação de óxidos superficiais aderidos, indicando atividade eletroquímica heterogênea ao longo do duto.
3. O oxigênio dissolvido na solução participa da semirreação catódica, atuando como o principal receptor de elétrons no mecanismo de corrosão em meio aquoso não ácido.
Com base nessas observações, assinale a afirmativa incorreta.
Provas
Questão presente nas seguintes provas
Uma das etapas do processo industrial de formação do aço é a
obtenção do ferro metálico a partir da hematita, conforme a
sequência de reações apresentadas.
3Fe2O3 + CO → 2Fe3O4 + CO2
Fe3O4 + CO → 3FeO + CO2
FeO + CO → Fe + CO2
Considerando 1 tonelada de hematita, com 70% de óxido férrico, a quantidade de mols de elétrons envolvidos no processo até a total conversão em ferro metálico é
3Fe2O3 + CO → 2Fe3O4 + CO2
Fe3O4 + CO → 3FeO + CO2
FeO + CO → Fe + CO2
Considerando 1 tonelada de hematita, com 70% de óxido férrico, a quantidade de mols de elétrons envolvidos no processo até a total conversão em ferro metálico é
Provas
Questão presente nas seguintes provas
De acordo com a SOS Mata Atlântica, o número de pontos de
captação com boa qualidade da água no rio Tietê diminuiu entre
2024 e 2025. Atualmente, apenas um ponto apresenta um IQA
(Índice de Qualidade das Águas) classificado como “bom” (entre
52 e 79). Entre os parâmetros que compõem esse índice, e
considerando a quantidade de lançamentos de esgoto
identificados no rio, podemos inferir que a DBO₅,₂₀ (Demanda
Bioquímica de Oxigênio) é um aspecto de extrema preocupação.
Diante desse cenário, é correto afirmar que
Provas
Questão presente nas seguintes provas
Com base nos coeficientes estequiométricos apresentados para
cada uma das reações,
I) 2 H3PO4 + 3 CaO → 1 _______ + 3 H2O
II) 1 _______ + 2 NaOH → 1 Na2HBO3 + 2 H2O
III) 1 SO2 + 1 Ca(OH)2 → 1 _______ + 1 H2O
IV) 1 H2SO4 + 2 KOH → _______ + 2 H2O
Complete as lacunas e assinale a opção que mostra as fórmulas corretas na ordem apresentada
I) 2 H3PO4 + 3 CaO → 1 _______ + 3 H2O
II) 1 _______ + 2 NaOH → 1 Na2HBO3 + 2 H2O
III) 1 SO2 + 1 Ca(OH)2 → 1 _______ + 1 H2O
IV) 1 H2SO4 + 2 KOH → _______ + 2 H2O
Complete as lacunas e assinale a opção que mostra as fórmulas corretas na ordem apresentada
Provas
Questão presente nas seguintes provas
O sulfito monoácido de sódio NaHSO3 é um importante insumo nas
indústrias de papel e couro. Ele pode ser obtido a partir da
seguinte equação:
Na2CO3 + 2 SO2 + H2O → 2 NaHSO3 + CO2
Em uma amostra de 500 kg de carbonato de sódio impuro, foram produzidos 176 kg de dióxido de carbono. A pureza da amostra é
Na2CO3 + 2 SO2 + H2O → 2 NaHSO3 + CO2
Em uma amostra de 500 kg de carbonato de sódio impuro, foram produzidos 176 kg de dióxido de carbono. A pureza da amostra é
Provas
Questão presente nas seguintes provas
A floculação é uma etapa importante nas estações de tratamento
de água. Nela o óxido de cálcio (CaO) e o sulfato de alumínio
(Al2SO4) são adicionados à água, para a remoção de impurezas.
Considere as equações não balanceadas envolvidas na floculação:
CaO + H2O → Ca(OH)2
Ca(OH)2 + Al2(SO4)3 → CaSO4 + Al(OH)3
Ao adicionarmos, em um tanque de tratamento, 672 kg de óxido de cálcio, a quantidade mínima de sulfato de alumínio que deve ser adicionada, considerando pureza e rendimento iguais a 100%, é de
CaO + H2O → Ca(OH)2
Ca(OH)2 + Al2(SO4)3 → CaSO4 + Al(OH)3
Ao adicionarmos, em um tanque de tratamento, 672 kg de óxido de cálcio, a quantidade mínima de sulfato de alumínio que deve ser adicionada, considerando pureza e rendimento iguais a 100%, é de
Provas
Questão presente nas seguintes provas
A tabela nutricional de determinado refrigerante reduzido em
açúcares indica a presença de 17100 mg de sacarose (C12H22O11) a
cada copo de 200 mL da bebida.
A concentração molar (mol.L-1 ) da sacarose nesse refrigerante é de, aproximadamente
A concentração molar (mol.L-1 ) da sacarose nesse refrigerante é de, aproximadamente
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
A estrutura espacial das moléculas, pode ser definida como arranjo
molecular a forma como as nuvens eletrônicas se dispõem em
torno do átomo central. Já a geometria pode ser definida a partir
da posição ocupada pelos átomos ligantes.
A geometria da molécula de pentafluoreto de bromo (BrF5) é denominada
A geometria da molécula de pentafluoreto de bromo (BrF5) é denominada
Provas
Questão presente nas seguintes provas
Com base no gráfico anexado, que ilustra a variação da Energia de
Ionização (eV) em função do Número Atômico (Z) dos elementos
químicos, analise os itens a seguir:
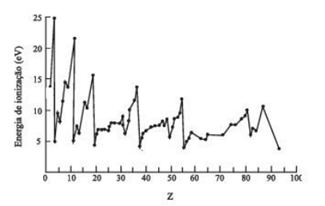
I. Os valores máximos (picos) na curva correspondem a elementos que possuem a camada de valência completa, como os Gases Nobres (Z=2, Z=10, Z=18, etc.), indicando a maior estabilidade e, consequentemente, a maior dificuldade para remover um elétron.
II. Os elementos localizados nos valores mínimos da curva, que ocorrem imediatamente após os picos, são os Metais Alcalinos (Z=3, Z=11, Z=19, etc.), que possuem o menor potencial de ionização em seus respectivos períodos devido à presença de um único elétron na camada de valência, afastado do núcleo.
III. Ao longo da Tabela Periódica (da esquerda para a direita em um período), observa-se uma tendência geral de aumento na energia de ionização. Isso ocorre porque o raio atômico diminui e a carga nuclear efetiva aumenta, tornando a atração sobre os elétrons mais forte.
IV. A energia de ionização dos elétrons da última camada, representada no gráfico (eV), é significativamente menor do que a energia de ligação dos elétrons das camadas internas (mais próximos do núcleo).
É correto o que se afirma em

I. Os valores máximos (picos) na curva correspondem a elementos que possuem a camada de valência completa, como os Gases Nobres (Z=2, Z=10, Z=18, etc.), indicando a maior estabilidade e, consequentemente, a maior dificuldade para remover um elétron.
II. Os elementos localizados nos valores mínimos da curva, que ocorrem imediatamente após os picos, são os Metais Alcalinos (Z=3, Z=11, Z=19, etc.), que possuem o menor potencial de ionização em seus respectivos períodos devido à presença de um único elétron na camada de valência, afastado do núcleo.
III. Ao longo da Tabela Periódica (da esquerda para a direita em um período), observa-se uma tendência geral de aumento na energia de ionização. Isso ocorre porque o raio atômico diminui e a carga nuclear efetiva aumenta, tornando a atração sobre os elétrons mais forte.
IV. A energia de ionização dos elétrons da última camada, representada no gráfico (eV), é significativamente menor do que a energia de ligação dos elétrons das camadas internas (mais próximos do núcleo).
É correto o que se afirma em
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container