Foram encontradas 35.922 questões.
Um técnico em química resolveu identificar cilindros de gás nitrogênio usados no laboratório com diferentes notações.
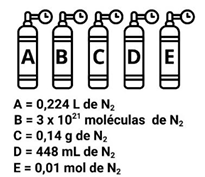
Qual dos cilindros listados apresenta a maior quantidade de moléculas de N2? (considere constante de Avogadro = 6 x 1023 e volume molar = 22,4L)
Provas
Uma curva de calibração para determinação da concentração de um analito (mg.L-1) por espectrofotometria foi construída a partir da análise de soluções padrão com concentrações conhecidas. Após a medição, os dados foram plotados e uma regressão linear pelo método dos mínimos quadrados forneceu a seguinte equação da reta:
y = 0,0160 x + 0,05 (R2 = 0,9998)
onde o eixo y é absorbância e o eixo x a concentração.
Uma amostra desconhecida do analito foi analisada pelo mesmo método e apresentou uma absorbância de 0,370.
A concentração aproximada do analito na amostra desconhecida é
Provas
A semirreação presente em um eletrodo conectado a um eletrodo padrão de referência é:
![]()
Na medida experimental, temos [H3AsO4] = [H3AsO3] e o valor lido no voltímetro para o par H3AsO4/H3AsO3 é de 0,259 V.
Considere para equação de Nernst que ![]() seja aproximadamente
seja aproximadamente ![]() e assinale a opção que mostra o pH da solução.
e assinale a opção que mostra o pH da solução.
Provas
Observe as equações a seguir:
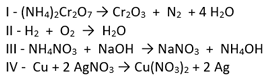
Assinale a opção que representa, respectivamente, a sequência das reações de síntese, análise, simples troca e dupla troca.
Provas
Com base nos coeficientes estequiométricos apresentados para cada uma das reações
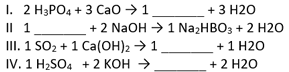
As fórmulas corretas para cada equação química, respectivamente são
Provas
Um eletrodo contendo a meia-reação:
![]()
Esse eletrodo é conectado a um eletrodo de referência Ag/AgCl (KCl sat.), cujo potencial padrão de redução é +0,197 V em relação ao EPH. Ao montar a célula eletroquímica, o potencial medido no voltímetro para o par Cu²⁺/Cu⁺ versus Ag/AgCl (KCl sat.) foi igual a -0,044V.
Determine o potencial padrão de redução do par Cu²⁺/Cu⁺ em relação ao eletrodo padrão de hidrogênio (EPH).
Provas
Sobre o eletrodo de vidro utilizado na determinação de pH, analise as afirmativas:
I. O potencial do eletrodo de vidro depende da diferença de atividade de íons H⁺ entre a solução interna e a solução externa.
II. O eletrodo de vidro apresenta resposta linear ao pH, obedecendo à equação de Nernst.
III. A presença de altas concentrações de íons Na⁺ pode interferir na leitura, causando erro ácido.
Está correto o que se afirma em
Provas
O rótulo de uma marca famosa de leite integral UHT (tratamento térmico a alta temperatura) consta que em 200 mL do leite contém 240 mg de cálcio (Ca2+). Um analista procedeu com o tratamento de uma amostra com o mesmo volume de leite que consta no rótulo, oxidando toda matéria orgânica e solubilizando os íons Ca2+ para posterior análise gravimétrica com oxalato (C2O42-). O precipitado foi calcinado até estabilização da massa e o valor obtido foi de 0,2800 g. As equações abaixo representam as etapas da análise.
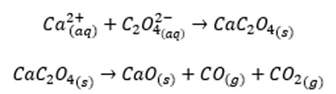
Sobre a conclusão da análise, é correto afirmar que o teor de cálcio determinado por gravimetria
Provas
Uma cartela de comprimidos de ácido acetil salicílico de uma marca famosa diz que cada comprimido contém 500 mg do medicamento. A fim de verificar a dosagem, um técnico em química dissolveu um comprimido em solução alcoólica, gotejou fenolftaleína e realizou a titulação com solução padronizada de NaOH 0,01 mol.L-1 (fator de correção = 1,000) e consumiu 24 mL até o ponto final da titulação.
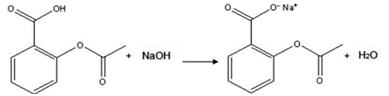
Com base na reação, a diferença percentual entre a massa informada na cartela e a medida experimentalmente é
Provas
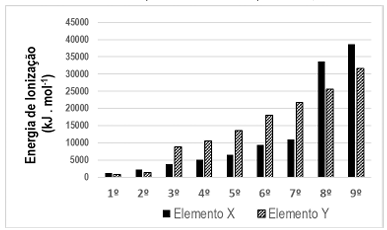
A fórmula resultante da combinação dos elementos e sua identificação é
Provas
Caderno Container