Foram encontradas 35.922 questões.
As reações de substituições em haletos de alquila ocorrem por meio de dois mecanismos fundamentais: Substituição Nucleofílica Unimolecular (SN1) e Substituição Nucleofílica Bimolecular (SN2). Dependendo dos reagentes utilizados, um ou outro desses mecanismos é favorecido.
Nesse contexto, a substituição que ocorre segundo o mecanismo SN1 emprega preferencialmente como reagente o iodeto de
Provas
O 1,2-dicloro-eteno é encontrado sob duas formas isômeras espaciais: cis-1,2-dicloro-eteno e trans-1,2-dicloro- -eteno. Com o intuito de separar esses dois isômeros, avaliou-se a possibilidade de separá-los em função de suas temperaturas de ebulição.
Ao comparar as temperaturas de ebulição desses compostos, observa-se que
Provas
A reação química de oxidação do dióxido de enxofre, representada pela equação termoquímica a seguir, foi analisada em um reator.
![]()
Com o intuito de deslocar o equilíbrio dessa equação e aumentar a concentração de SO3 no interior do reator, podem ser empreendidas as seguintes ações:
Provas
O íon tetraamincádmio(II) é formado a partir da seguinte equação química:
![]()
A constante de formação desse íon, a 25 ºC, é igual a 1,0 x 107 . Nesse contexto, considere um experimento, realizado a 25 ºC, no qual as concentrações de Cd2+ e NH3 no equilíbrio são, respectivamente, iguais a 2,0 x 10-3 mol/L e 5 x 10-2 mol/L.
Nessas condições, a concentração, em mol/L, do íon tetraamincádmio(II) é, aproximadamente, igual a
Provas
O pentafluoreto de cloro, cuja fórmula molecular é ClF5 , é um composto gasoso com elevado poder oxidante. Nesse composto, os átomos de flúor encontram-se ligados ao cloro, que ocupa a posição central.
A geometria molecular desse composto é
Provas
Em um processo radioativo, o radioisótopo urânio-238 decai emitindo 4 partículas alfa e 2 partículas beta.
Nesse decaimento, o radioisótopo formado corresponde ao
Provas
Em uma aula prática de Química, utilizou-se o procedimento experimental representado a seguir para analisar a condutividade de líquidos.
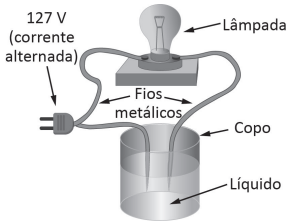
Nesse procedimento, o acendimento da lâmpada indica que o líquido conduz eletricidade, e o não acendimento da lâmpada indica que o líquido não conduz eletricidade. No experimento foram testados água, solução aquosa de sal de cozinha (cloreto de sódio), solução aquosa de sacarose (C12H22O11) e vinagre (solução aquosa de ácido etanoico). A partir dos resultados experimentais, o professor realizou uma discussão dos fenômenos observados com os alunos.
Considerando-se o experimento realizado e as observações feitas, pôde-se abordar prioritariamente, nessa discussão, conceitos relacionados ao seguinte tópico:
Provas
Uma amostra de 10,0 g de carbonato de chumbo II impuro teve seu grau de pureza analisado por meio de sua reação com ácido nítrico, conforme representado pela reação química a seguir.
![]()
As impurezas da amostra não reagiram com o ácido e, após o consumo de todo o carbonato de chumbo II presente na amostra, foram obtidos 6,62 g de nitrato de chumbo II.
Nesse contexto, o grau de pureza da amostra é igual a:
Dado
Massas molares:
PbCO3 = 267 g/mol
Pb(NO3 ) 2 = 331 g/mol
Provas
A bateria de chumbo é comumente utilizada em automóveis. As espécies químicas envolvidas na reação que ocorre nessa bateria estão presentes nas seguintes semirreações de redução:
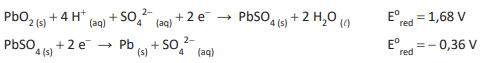
Em relação a esse tipo de bateria, a diferença de potencial padrão, em volts, e o ânodo correspondente são, respectivamente,
Provas
Um professor de Química desenvolveu um estudo para avaliar o comportamento da água em reações ácido-base. Nesse estudo, foram analisadas as seguintes equações químicas:
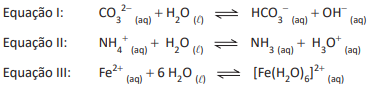
Considerando-se as teorias ácido-base de Bronsted-Lowry e de Lewis, a água, nas equações I, II e III, se comporta, respectivamente, como
Provas
Caderno Container