Foram encontradas 36.278 questões.
- Química OrgânicaReações OrgânicasReações Orgânicas: Oxidação, Redução e Polimerização
- Termoquímica e Termodinâmica
- Transformações Químicas e Energia
Use: Ered Sn2+ = -0,14V , Ered Cu2+ = +0,34 V e F = 96485,33 C.mol-1
Provas
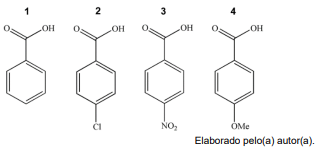
Dados os ácidos carboxílicos da figura, ordene-os em ordem decrescente de acidez.
Provas
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
- Química InorgânicaSoluções e Substâncias Inorgânicas
O modelo de ácidos e bases duros e moles se aproveita do modelo de Lewis para explicar comportamento dos ácidos e das bases, e constitui um guia empírico muito útil para predizer a reatividade de átomos, moléculas e íons. A medida da dureza e moleza dos ácidos e bases é baseada em suas polarizabilidades.
Dentre os ânions citados abaixo, oúnico considerado uma base dura é o ânion
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Química Orgânica
Use: Massas Molares: O = 16,0 g mol-1; C = 12 g mol-1; H = 1 g mol-1; N = 14 g mol-1; Cl = 35,5 g mol-1
Provas
- FundamentosPropriedades das Substâncias
- FundamentosSubstâncias, Misturas e Processos de Separação
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
- Transformações Químicas e Energia
Provas
- Química OrgânicaIsomeria Plana e Espacial
- Química OrgânicaPropriedades Químicas dos Compostos Orgânicos
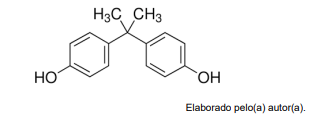
Em uma análise de ressonância magnética nuclear de hidrogênio (RMN H1) para uma amostra de bisfenol-A,o número de sinais respectivos a átomos de hidrogênio esperados no espectro é:
Provas
- Química InorgânicaSoluções e Substâncias Inorgânicas
- Técnicas de LaboratórioEquipamentos e Técnicas Básicas
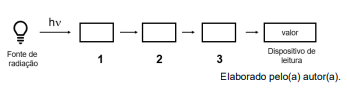
Com base no esquema acima, os componentes 1, 2, e 3 são, respectivamente:
Provas
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química OrgânicaPropriedades Físicas dos Compostos Orgânicos
Analise a tabela de pontos de ebulição para diversos cloretos a seguir.
| PE (ºC) | composto | PE (ºC) | composto | PE (ºC) | composto |
| 1380 | LiCl | 12,5 | BCl3 | 76 | CCl4 |
| 1440 | NaCl | 183 | AlCl3 | 57 | SiCl4 |
| 1380 | KCl | 1000 | ScCl3 | 136 | TiCl4 |
Elaborado pelo(a) autor(a).
O caráter das ligações químicas nas substâncias tem grande influência nas suas propriedades químicas. As substâncias da tabela que apresentam os maiores pontos de ebulição apresentam, predominantemente, ligações de caráter
Provas
- Química OrgânicaCadeias Carbônicas
- Química OrgânicaFunções Nitrogenadas: Amina, Amida, Nitrila, Isonitrila e Nitro Composto
- Química OrgânicaIsomeria Plana e Espacial
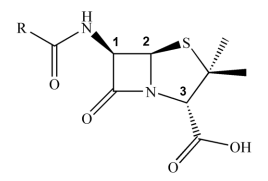
Elaborado pelo(a) autor(a).
A molécula de penicilina apresenta três centros assimétricos. As configurações absolutas dos carbonos assinalados com 1, 2 e 3 na figura são, respectivamente:
Provas
Uma solução tampão é uma mistura de um ácido fraco e sua base conjugada, ou de uma base fraca e seu ácido conjugado, que resiste a variações de pH quando pequenas quantidades de ácido ou base são adicionadas. Este efeito estabilizador ocorre porque os componentes da solução tampão neutralizam os íons H+ ou OH− adicionados, mantendo o pH da solução relativamente constante.
Quando se misturam as soluções de ácido fórmico e formiato de sódio estabelecem-se os seguintes equilíbrios:
HCOOH(aq) + H2O(l) ⇌ H3O+(aq) + HCOO-(aq) Ka = 1,8 x 10-4
HCOO-(aq) + H2O(l) ⇌ HCOOH+(aq) + OH-(aq) Kb = Kw.Ka-1 = 5,56 x 10-11
Calcule a concentração de íons hidrônio de uma solução tampão obtida pela mistura das soluções ácido fórmico 0,25 mol L-1 e formiato de sódio 0,9 mol L-1.
Provas
Caderno Container