Foram encontradas 36.279 questões.
Você precisa preparar 100 mL de uma solução estoque de NaOH
com concentração de 3 M, e, a partir dessa preparação, 1 L de
uma solução de NaOH com concentração de 60 mM. Para isso, a
massa (em g) de NaOH necessária para preparar a primeira
solução (3 M) e o volume (em mL) da solução a 3 M necessário
para preparar a solução a 60 mM são, respectivamente,
Dado: massa molar do NaOH = 40 g/mol.
Dado: massa molar do NaOH = 40 g/mol.
Provas
Questão presente nas seguintes provas
Os cianetos são sais extremamente tóxicos e podem levar à
morte em caso de contaminação. Um composto muito usado em
misturas de fases móveis em cromatografia líquida que não pode
ser submetido à incineração como forma de disposição final, pois
sua degradação térmica leva à formação de cianeto. Soluções
contendo esse composto passa por um pré-tratamento antes do
descarte.
O composto em questão e o tratamento utilizado antes de seu descarte são, respectivamente,
O composto em questão e o tratamento utilizado antes de seu descarte são, respectivamente,
Provas
Questão presente nas seguintes provas
Uma mistura pode ser classificada como uma combinação de
duas ou mais substâncias que não reagem entre si, mantendo as
suas identidades e as suas propriedades individuais. Essas
diferem das substâncias puras por não possuírem uma
composição fixa e constante. Exemplos comuns de misturas
incluem o leite, que é uma combinação de carboidratos,
gorduras, proteínas e sais minerais, e o bronze, que é uma liga
metálica formada pela combinação de cobre e estanho.
De acordo com essas informações, assinale a alternativa que é um exemplo de mistura química.
De acordo com essas informações, assinale a alternativa que é um exemplo de mistura química.
Provas
Questão presente nas seguintes provas
O conhecimento sobre a ligação química do carbono é crucial
para a síntese de compostos orgânicos, a manipulação de
reações químicas e a compreensão das propriedades
físico-químicas dos materiais estudados. Além disso, a
compreensão dos princípios da ligação química do carbono é
essencial para interpretar estruturas moleculares, para prever
comportamentos químicos e para realizar modificações
estruturais, com o objetivo de melhorar as propriedades de
compostos específicos. Na natureza, o gás metano (CH4) não
resulta da reação de um átomo de carbono com átomos de
hidrogênio; ele deriva de processos biológicos complexos. Existia
um enigma desafiador no início da Teoria de Ligação de Valência
(TLV), que seja: o fato de o átomo de carbono ter a habilidade de
realizar 4 (quatro) ligações com 4 (quatro) átomos de hidrogênio.
Tal teoria previa uma configuração eletrônica compatível para
explicar apenas 2 (duas) ligações, 1s2
2s2
2px
1
2py
1
.
Sobre o átomo de carbono do ponto de vista da TLV, assinale a alternativa correta.
Sobre o átomo de carbono do ponto de vista da TLV, assinale a alternativa correta.
Provas
Questão presente nas seguintes provas
Diversos processos de análises de materiais químicos ou de
desenvolvimento de novos produtos envolvem diferentes tipos de
equilíbrios químicos, os quais poderão envolver aspectos
termodinâmicos, para os quais o/a analista deverá estar apto/a
para lidar com eles. No equilíbrio químico, ou seja, em condições
de temperatura e de pressão constantes, as atividades de todas
as substâncias envolvidas nesse processo possuem um “valor de
equilíbrio”, nomeado constante de equilíbrio, que é representada
pela letra K.
Sobre o equilíbrio químico, dadas as afirmativas,
I. Para reações exotérmicas, quando a temperatura aumenta a composição da mistura em equilíbrio, há deslocamento em favor dos produtos e o oposto ocorre para as reações endotérmicas.
II. A energia livre de Gibbs pode ser relacionada à constante K, em que o ∆G t° (valor da energia de Gibbs no equilíbrio) é positivo; então, ln K (logaritmo natural da constante de equilíbrio) deverá ser negativo e, portanto, K < 1, indicando que os reagentes estão sendo favorecidos no equilíbrio químico.
III. A energia livre de Gibbs pode ser relacionada à constante K, em que o ∆G t° (valor da energia de Gibbs no equilíbrio) é negativo; então, ln K (logaritmo natural da constante de equilíbrio) deverá ser negativo e, portanto, K > 1, indicando que os produtos estão sendo favorecidos no equilíbrio químico.
verifica-se que está/ão correta/s
Sobre o equilíbrio químico, dadas as afirmativas,
I. Para reações exotérmicas, quando a temperatura aumenta a composição da mistura em equilíbrio, há deslocamento em favor dos produtos e o oposto ocorre para as reações endotérmicas.
II. A energia livre de Gibbs pode ser relacionada à constante K, em que o ∆G t° (valor da energia de Gibbs no equilíbrio) é positivo; então, ln K (logaritmo natural da constante de equilíbrio) deverá ser negativo e, portanto, K < 1, indicando que os reagentes estão sendo favorecidos no equilíbrio químico.
III. A energia livre de Gibbs pode ser relacionada à constante K, em que o ∆G t° (valor da energia de Gibbs no equilíbrio) é negativo; então, ln K (logaritmo natural da constante de equilíbrio) deverá ser negativo e, portanto, K > 1, indicando que os produtos estão sendo favorecidos no equilíbrio químico.
verifica-se que está/ão correta/s
Provas
Questão presente nas seguintes provas
Para que uma reação química ocorra, são necessárias algumas
condições como: afinidade química, contato e colisão efetiva
entre os reagentes, bem como energia de ativação. Um exemplo
que abarca todas essas condições é quando o sódio metálico em
contato com o ar leva a uma reação violenta e altamente
exotérmica.
Qual das alternativas descreve corretamente o que ocorre durante essa reação?
Qual das alternativas descreve corretamente o que ocorre durante essa reação?
Provas
Questão presente nas seguintes provas
O benzeno (C6H6) é um composto aromático que apresenta uma
baixa reatividade. No entanto, quando o benzeno é exposto ao
gás bromo, na presença de catalisador de tribrometo de ferro,
ocorre uma reação de substituição eletrofílica aromática, levando
à formação do bromo-benzeno (C6H5Br).
Dados: C = 12,01; H = 1,01; Br = 79,91
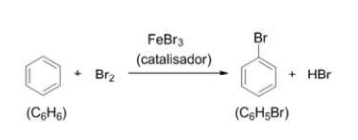
Determine o rendimento teórico do bromo-benzeno, quando 30 g de benzeno reage com 65 g de bromo.
Dados: C = 12,01; H = 1,01; Br = 79,91

Determine o rendimento teórico do bromo-benzeno, quando 30 g de benzeno reage com 65 g de bromo.
Provas
Questão presente nas seguintes provas
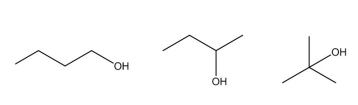
Dadas as afirmativas relacionadas a propriedades dos três isômeros do butanol da figura,
I. O 1-butanol apresenta o maior ponto de ebulição dentre os três compostos acima.
II. O 2-butanol apresenta o menor ponto de ebulição dentre os três compostos acima.
III. O 2-metil-2-propanol é o composto mais polar dessa série.
IV. O 1-butanol é o composto menos polar dessa série.
verifica-se que está/ão correta/s
Provas
Questão presente nas seguintes provas
Um frasco contendo uma solução de NaOH, de concentração
desconhecida, foi encontrado no laboratório. Uma solução de
HCl 2 M foi usada para titular a solução básica. Uma alíquota de
20 mL do titulado foi transferida para um Erlenmeyer, e
fenolftaleína foi usada como indicador. O titulante foi transferido
para uma vidraria específica, e foram necessários 12 mL para
que o ponto de viragem fosse atingido.
O nome da vidraria usada e a concentração da solução de NaOH são, respectivamente,
O nome da vidraria usada e a concentração da solução de NaOH são, respectivamente,
Provas
Questão presente nas seguintes provas
O diamante (ou diagrama) de Hommel é uma ferramenta da
simbologia na rotulagem de produtos químicos que permite a
rápida visualização dos riscos associados a determinado
produto. Esse símbolo associa cores a quatro tipos de riscos
envolvendo um produto químico. Esses riscos são:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container