Foram encontradas 35.936 questões.
Durante a preparação de uma titulação em laboratório,
é necessário realizar a ambientação da bureta. Esse
procedimento evita contaminações, e garante maior
precisão no volume dispensado.
Para isso, a bureta deve ser previamente enxaguada com pequenas porções
Para isso, a bureta deve ser previamente enxaguada com pequenas porções
Provas
Questão presente nas seguintes provas
A espectrofotometria na região do UV/Vis é uma técnica
amplamente utilizada em análises químicas.
A respeito dos princípios dessa técnica e da aplicação dessa técnica analítica, é correto afirmar que
A respeito dos princípios dessa técnica e da aplicação dessa técnica analítica, é correto afirmar que
Provas
Questão presente nas seguintes provas
Em uma análise gravimétrica, uma amostra de 2,000 g
de uma mistura contendo oxalato de amônio monoidratado ((NH4)2C2O4 · H2O), e um material quimicamente
inerte nas condições do ensaio, foi aquecida, em um
cadinho até massa constante. Nessas condições, o oxalato de amônio monoidratado decompõe-se completamente liberando os gases amônia, dióxido de carbono,
monóxido de carbono e vapor d’água.
Após o resfriamento, o cadinho apresentou um resíduo sólido de massa 1.200 g.
O teor percentual em massa de oxalato de amônio monoidratado na amostra e a soma dos coeficientes estequiométricos da equação de reação de um mol de oxalato de amônio são iguais a
Após o resfriamento, o cadinho apresentou um resíduo sólido de massa 1.200 g.
O teor percentual em massa de oxalato de amônio monoidratado na amostra e a soma dos coeficientes estequiométricos da equação de reação de um mol de oxalato de amônio são iguais a
Provas
Questão presente nas seguintes provas
Um estudo da cinética reacional da formação do NO2
F a
partir da interação entre os gases dióxido de nitrogênio e
flúor empregou misturas reacionais e condições controladas da reação descrita na equação a seguir:
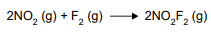
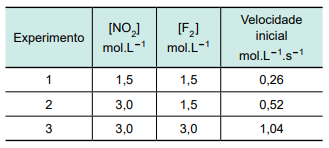
A tabela apresenta os dados desse estudo:
Essa reação é de
A tabela apresenta os dados desse estudo:

Essa reação é de
Provas
Questão presente nas seguintes provas
A figura apresenta o detalhe do corte da escala de duas
vidrarias de laboratório, I e II:
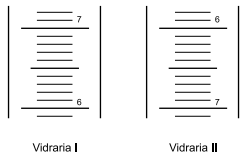
As vidrarias I e II são, respectivamente:

As vidrarias I e II são, respectivamente:
Provas
Questão presente nas seguintes provas
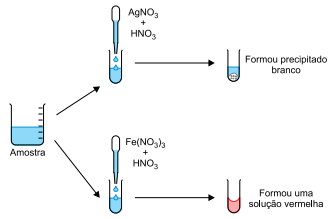
Para a identificação de um ânion presente em determinada amostra de uma solução aquosa, foram feitos os
testes representados na figura:
 (Arquivo pessoal; imagem usada com autorização)
(Arquivo pessoal; imagem usada com autorização)
De acordo com os resultados observados nos testes, concluiu-se que a amostra continha o ânion
 (Arquivo pessoal; imagem usada com autorização)
(Arquivo pessoal; imagem usada com autorização)
De acordo com os resultados observados nos testes, concluiu-se que a amostra continha o ânion
Provas
Questão presente nas seguintes provas
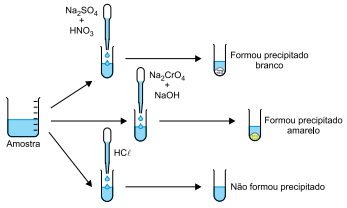
Para a identificação da identidade do cátion presente
em uma determinada amostra de solução aquosa, foram
feitos os testes representados na figura:
 (Arquivo pessoal; imagem usada com autorização)
(Arquivo pessoal; imagem usada com autorização)
De acordo com os resultados observados nos testes, concluiu-se que a amostra continha o cátion
 (Arquivo pessoal; imagem usada com autorização)
(Arquivo pessoal; imagem usada com autorização)
De acordo com os resultados observados nos testes, concluiu-se que a amostra continha o cátion
Provas
Questão presente nas seguintes provas
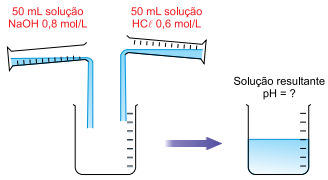
Em um laboratório químico, foram misturados 50 mL de
uma solução de NaOH 0,8 mol/L e 50 mL de uma solução
de HCl 0,6 mol/L, conforme representado na figura:
 (Arquivo pessoal; imagem usada com autorização)
(Arquivo pessoal; imagem usada com autorização)
Considerando que Kw = 1 x 10–14, a 25 ºC, o pH da solução resultante após a mistura, a 25 ºC, é igual a
 (Arquivo pessoal; imagem usada com autorização)
(Arquivo pessoal; imagem usada com autorização) Considerando que Kw = 1 x 10–14, a 25 ºC, o pH da solução resultante após a mistura, a 25 ºC, é igual a
Provas
Questão presente nas seguintes provas
A equação química e a constante do equilíbrio de formação da amônia a uma dada temperatura são:
![]()
Nessa mesma condição de temperatura, para a reação inversa dada pela equação a seguir:
![]()
O valor numérico para a constante de equilíbrio da equação (II), K2, nessa mesma condição de temperatura, é igual a:
Provas
Questão presente nas seguintes provas
Um composto orgânico contendo apenas carbono, hidrogênio e oxigênio foi analisado por reação de combustão
completa em excesso de O2. A queima de 0,050 mol do
composto gerou 0,80 mol de CO2 e 0,30 mol de H2O.
A partir do balanço de massas, determinou-se que a
amostra continha 3,2 g de átomos de oxigênio (O).
A massa molar desse composto orgânico é
A massa molar desse composto orgânico é
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container