Foram encontradas 35.936 questões.
C6H10O5 (s) + 6O2 (g) → 6CO2 (g) + 5H2O (g)
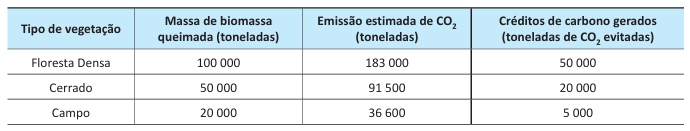
No contexto apresentado, a professora explicou que a Educação Ambiental pode promover a sensibilização crítica das pessoas sobre o greenwashing, ao revelar como algumas empresas podem utilizar discursos ecológicos para mascarar tanto práticas insustentáveis quanto a redução dos gases do efeito estufa (GEE).
A professora observou que os estudantes conseguiram integrar os conhecimentos químicos e ambientais apresentados, quando o grupo concluiu que,
Provas
Uma professora que atua em uma escola situada em uma cidade às margens do Rio Doce (MG) selecionou, para usar em suas aulas, o seguinte trecho de uma reportagem:
Tragédia de Mariana: desastre com barragem acordou “monstro” de poluentes no Rio Doce, diz perito.
O desastre ambiental com a Barragem de Fundão, decorrente da atividade mineradora, realizada pela Samarco em Mariana (MG), fez com que poluentes que estavam estabilizados no fundo do Rio Doce fossem suspensos, piorando as condições da água. O “monstro acordado” pode ser um dos responsáveis pelas concentrações “elevadas de sólidos em suspensão e metais pesados”, como manganês, cobre, alumínio e zinco, o que piorou a qualidade da água dois anos depois do desastre, conforme constatou a Fundação SOS Mata Atlântica. Segundo estudo da entidade, as condições estão ruins ou péssimas em 88,9% dos 18 pontos de coleta analisados. Isso ocorre não somente em função da toxicidade dos rejeitos, mas também da própria característica dos compostos, que ficam suspensos e mantêm a turbidez, com baixa transparência da água, o que também prejudica muito a proliferação da vida aquática ou a utilização do rio.
Disponível em: www.ihu.unisinos.br. Acesso em: 14 maio 2025 (adaptado).
Provas
Sabe-se que os potenciais padrão de redução (E°) dos metais são:
• Cu2+/Cu = +0,34 V
• Fe2+/Fe = -0,44 V
• Zn2+/Zn = -0,76 V
• Mg2+/Mg = -2,37 V
BROWN, T.; LEMAY, H. E.; BURSTEN, B. E. Química: a ciência central. São Paulo: Prentice-Hall, 2005.
Qual alternativa representa o raciocínio que explica a proteção catódica com base nos conceitos de eletroquímica?
Provas
Para promover a autonomia dos estudantes e com base no projeto da escola, o plano de aula deve conter ações que possibilitem que os estudantes compreendam o processo de
Provas

Provas
Representações do HX em água

SMITH, K. J.; METZ, P. A. Evaluating Student Understanding of Solution Chemistry Through Microscopic Representations. Journal of Chemical Education, n. 3, 1996 (adaptado).
O professor identifica que o estudante que relacionou corretamente a imagem aos conceitos optou pela representação
Provas
 Disponível em: http://quimicavida92.blogspot.com. Acesso em: 7 jun. 2025 (adaptado).
Disponível em: http://quimicavida92.blogspot.com. Acesso em: 7 jun. 2025 (adaptado). Para compreender a tirinha, os estudantes, considerando os conceitos eletroquímicos e os metais envolvidos, devem saber que, ao ar livre, o metal
Provas
Grupo A: “O zinco perde elétrons porque tem maior potencial de redução”.
Grupo B: “Não, eu acho que o zinco perde elétrons porque seu potencial de redução é menor que o do cobre”.
Professora: “Interessante o que vocês disseram. Como a diferença entre os potenciais padrão de redução influencia quem perde e quem ganha elétrons em uma reação?
Os estudantes se entreolharam e começaram a discutir entre si. Um deles comentou: “Se o potencial de redução é menor, ele oxida. Então, ele perde elétrons”.
Outro completou: “Isso! E o que tem maior potencial de redução atua como agente oxidante”.
Após a aplicação do jogo, a professora, juntamente com os estudantes, promoveu uma discussão sobre as principais questões observadas, relacionando-as à teoria.
Essa atividade pode ser caracterizada como um jogo pedagógico cujo foco principal é
Provas
H3C−CH2−O−CH2−CH3
O composto representado pela fórmula estrutural precedente corresponde
Provas
(1) Fusão.
(2) Sublimação.
(3) Condensação.
(4) Solidificação.
( ) Passagem direta da matéria do estado sólido para o estado gasoso, sem transitar pela fase líquida.
( ) Transformação da matéria do estado gasoso para o estado líquido, geralmente associada à diminuição da temperatura ou ao aumento da pressão.
( ) Conversão da matéria do estado líquido para o estado sólido, que ocorre em uma temperatura específica denominada ponto de solidificação.
( ) Mudança do estado sólido para o estado líquido, causada pelo aumento da temperatura e rompimento do arranjo cristalino das partículas.
Provas
Caderno Container