Foram encontradas 36.167 questões.
A descoberta de novos elementos químicos tem sido um processo de avanços desde os tempos da Antiguidade. À medida que o número de elementos conhecidos aumenta, os cientistas começam a investigar as possibilidades de classificá-los de maneira útil. A Tabela Periódica é a mais importante ferramenta que os químicos utilizam para organizar e lembrar fatos químicos. Sobre as propriedades periódicas, analise as afirmativas a seguir.
I. As afinidades eletrônicas dos gases nobres são todas positivas, porque o elétron adicionado ocuparia um novo subnível de energia mais alta.
II. A diminuição na energia de ionização do Berílio ao Boro ocorre porque os elétrons no orbital preenchido 2s são mais eficientes em blindar os elétrons no subnível 2p do que são em se blindarem.
III. Em uma série isoeletrônica, o tamanho dos átomos aumenta com o aumento da carga nuclear à medida que os elétrons são atraídos mais fortemente pelo núcleo.
Está correto o que se afirma em
Provas
A forma e o tamanho de uma molécula de determinada substância, com a força e a polaridade de suas ligações, determinam enormemente as propriedades daquela substância. As sensações de olfato e visão dependem em parte da forma molecular. Quando você inspira, as moléculas no ar são transportadas pelos sítios receptores em seu nariz. Se as moléculas têm forma e tamanho corretos, elas podem encaixar-se devidamente nesses sítios receptores, que transmitem impulsos para o cérebro. Sobre geometria molecular e teoria de ligação, marque V para as afirmativas verdadeiras e F para as falsas.
( ) Os orbitais não-ligantes têm influência na estabilidade da molécula.
( ) A ordem de ligação no íon He2 + é 1.
( ) O arranjo e a geometria molecular do SnCl3 - é tetraédrico e piramidal trigonal, respectivamente.
( ) O arranjo e a hibridização do átomo central em hexafluoreto de enxofre é octaédrico e sp3d2, respectivamente.
A sequência está correta em
Provas
Considere a pilha de Daniell evidenciada na imagem, bem como os respectivos dados de potenciais-padrão obtidos a 298 K. Os eletrodos são conectados por dois fios de platina.
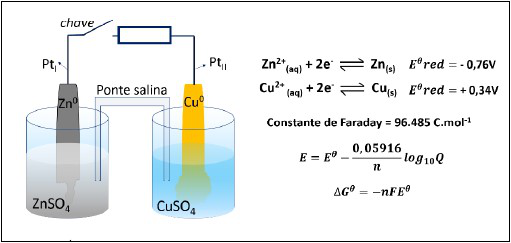
Diante do exposto, assinale a afirmativa correta.
Provas
“A solubilidade molar do não é influenciada pelo pH da solução.” Assinale a alternativa que completa corretamente a afirmativa anterior:
Provas
Sobre as propriedades de dispersões coloidais, analise as afirmativas a seguir.
I. Coloides representam a linha divisória entre as soluções e as misturas heterogêneas.
II. Os coloides são restritos ao estado líquido, ou seja, este tipo de dispersão não existe nos estados gasoso e sólido.
III. Einstein desenvolveu uma equação para o quadrado da média do deslocamento de uma partícula coloidal. Quanto maior a partícula coloidal, menor é o seu caminho livre médio em determinado líquido.
IV. Coloides são descritos por partículas com até 1 nm de diâmetro dispersas em determinado solvente.
V. O Efeito Tyndall explica porque o leite é branco e não transparente e porque as lanternas ou feixes de laser são mais visíveis nos nevoeiros e nas fumaças do que em ar claro e seco.
Está correto o que se afirma apenas em
Provas
Uma solução saturada de hidróxido de magnésio tem pH calculado de 10,52 e concentração de íons [Mg2+] de 1,7 x 10-4 mol . L-1. Suponha que o hidróxido de magnésio esteja em equilíbrio com uma solução tamponada de pH 9, de modo que a concentração de íons hidróxido seja 1,0 x 10-5 mol . L-1. Considerando o Kps (produto de solubilidade) de 1,8 x 10-11, a concentração de Mg2+ (em mol.L-1) nesta nova condição será de:
Provas
Sobre a eletrólise ígnea e em solução aquosa, analise as afirmativas a seguir.
I. Reações de eletrólise são típicas das chamadas células voltaicas, as quais empregam uma fonte externa de eletricidade para promover uma reação eletroquímica não espontânea.
II. O meio que transporta a corrente na célula voltaica pode ser um sal fundido ou uma solução de eletrólito.
III. Assim como nas células galvânicas, o eletrodo onde ocorre a redução é chamado de cátodo e o eletrodo em que ocorre a oxidação é chamado de ânodo.
IV. A eletrólise em sal fundido e em solução aquosa sempre levará aos mesmos produtos.
Está correto o que se afirma apenas em
Provas
Considere os alimentos evidenciados no quadro a seguir, bem como os resultados empíricos obtidos por calorimetria à pressão constante. O equipamento calorímetro (com certo volume de água) foi previamente calibrado e a capacidade calorífica obtida foi de 0,71 Cal . °C-1.
| Amendoim | Noz | Castanha-do-Pará | Ovo | |
| Massa da amostra (g) | 2,5 | 2,0 | 3,2 | 10,0 |
| Temperatura inicial (°C) | 20,0 | 20,0 | 20,0 | 20,0 |
| Temperatura final (°C) | 40,0 | 37,0 | 50,0 | 42,0 |
Considerando os resultados experimentais fornecidos, o alimento mais calórico será:
Provas
Antes do desenvolvimento do processo eletrolítico, o alumínio era obtido por meio de reação química. A rota experimental era onerosa e atribuía ao alumínio um custo por quilograma superior ao ouro. Em 1855, em uma exposição em Paris, o alumínio foi apresentado como um metal raro, mesmo sendo um dos elementos mais abundantes da crosta terrestre. Graças ao advento da eletrólise, o alumínio pôde ser produzido em larga escala, passando a se tornar um objeto comum no cotidiano das pessoas. O processo eletrolítico usado comercialmente para produzir alumínio denomina-se:
Provas
Considerando as informações sobre as variáveis termoquímicas das reações, marque V para as afirmativas verdadeiras e F para as falsas.
( ) A entalpia é um dado suficiente para avaliar se a reação ocorrerá de forma espontânea.
( ) Quando calor é adicionado a um sistema ou trabalho é realizado no sistema, sua energia interna aumenta.
( ) É possível obter o valor absoluto da energia interna e da entalpia para cada elemento químico.
( ) A energia interna não é afetada pela pressão e pela temperatura.
( ) A energia interna é uma propriedade extensiva.
A sequência está correta em
Provas
Caderno Container