Foram encontradas 36.167 questões.
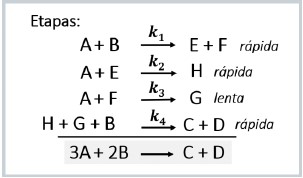
Considere a reação hipotética 3A + 2B !$ → !$A lei de velocidade para a reação global será:
Provas
Considere a reação A(aq) + B(aq) !$ → !$ C(aq) e os dados empíricos das velocidades iniciais medidas para várias concentrações iniciais diferentes dos reagentes.
| Número do | [A] mol.L-1 | [B] mol.L-1 | Velocidade mol.L-1.s-1 |
| 1 | 0,10 | 0,10 | 0,4 |
| 2 | 0,10 | 0,20 | 0,4 |
| 3 | 0,20 | 0,10 | 1,6 |
A velocidade da reação (em mol . L-1.s-1) quando [A] = 0,30 mol . L-1 e [B] for 0,10 mol . L-1 será de:
Provas
Considere a imagem a seguir que evidencia duas etapas de diluições. Inicialmente, foi adicionada uma solução básica (10 mL) no frasco A (formando a solução A), seguida da obtenção da solução B pela transferência de 100 ml de A para o frasco B.
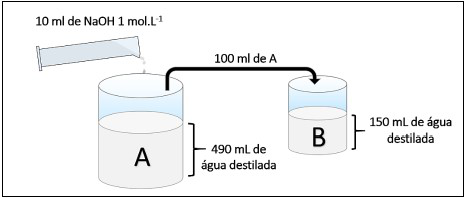
(Dados: log 2 = 0,30, log 3 = 0,48 e log 5= 0,70)
Com base nos dados fornecidos, o pH (em número inteiro e com arredondamento) da solução B será de:
Provas
Uma pilha eletroquímica é um dispositivo capaz de produzir trabalho elétrico nas vizinhanças. Sobre os conceitos eletroquímicos e as semirreações a seguir, assinale a afirmativa correta.
| MnO4-(aq)+8H+(aq)+5!$ \bar{e} !$ !$ \rightleftharpoons !$ Mn2+(aq) + 4H2O(1) | E!$ θ !$=1,51 V |
| 2CO2(g)+2H+(aq)+2!$ \bar{e} !$ !$ \rightleftharpoons !$ H2C2O4(aq) | E!$ θ !$=-0,49 V |
Provas
O fluoreto de cálcio é adicionado à água pura a 25° C e parte do sólido permanece como precipitado. A análise da solução no equilíbrio mostra que a concentração de íons cálcio é de 2,0 x 10-4 mol . L-1. Considerando as informações fornecidas e que nenhum outro equilíbrio químico esteja envolvido, o produto de solubilidade do fluoreto de cálcio será de:
Provas
Existem vários diagramas que apresentam a estabilidade relativa para diferentes estados de oxidação em solução aquosa. Em um deles o valor numérico do potencial-padrão (em volts) é escrito sobre a linha horizontal que conecta as espécies de um elemento em diferentes estados de oxidação. A forma mais oxidada de um elemento fica à esquerda e as espécies à direita estão em estados de oxidação sucessivamente mais baixos. As informações se referem ao diagrama de:
Provas
As tendências nos potenciais-padrão de redução (E!$ θ !$) em solução aquosa podem ser explicadas pelas contribuições termodinâmicas. O quadro a seguir evidencia os valores para alguns metais a 298 K; observe:
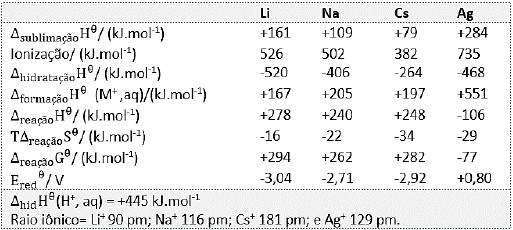
Considerando os dados fornecidos, assinale a afirmativa INCORRETA.
Provas
Considere uma base dissolvida em um solvente genérico (HSol) conforme a representação fornecida. A indicação “sol” significa solução em determinado solvente.
NH3(so1)+HSO1(1)!$ → !$NH4+(so1)+So1-(so1)
O efeito nivelador dessa base pode ser expresso em termos do pKb, onde Kb é a constante de basicidade da base em HSol. Sabendo que pK!$ α !$ + pKb = pKsol, tal critério para o nivelamento pode ser explicado como:
Provas
Considere as seguintes reações de oxirredução:
| I. | 4Fe2+(aq) + 02(g) + 4H+(aq) !$ \rightleftharpoons !$ 4Fe3+(aq) + 2H2O(1) |
| II. | 4Co3+(aq) +2H2O(1) !$ \rightleftharpoons !$ 4Co2+(aq) + O2(g) + 4H+(aq) |
| III. | 5HC1O(aq) !$ \rightleftharpoons !$ 2C12(g) + C1O3-(aq) + 2H2O(1) + H+(aq) |
| IV. | 2H+(aq) + Zn(s) !$ \rightleftharpoons !$ H2(g) + Zn2+(aq) |
| V. | 5HMnO4-(aq) + 3H+(aq) !$ \rightleftharpoons !$ 4MnO4-(aq) + Mn2+(aq) + 4H2O(1) |
Ocorre reação de desproporcionamento apenas em:
Provas
Sobre o efeito nivelador do solvente, assinale a afirmativa correta.
Provas
Caderno Container