Foram encontradas 36.142 questões.
O decaimento radioativo é acompanhado por uma grande variação de energia, muito maior do que uma reação química e, por isso, é considerado uma fonte de energia eficiente. O decaimento de 1 mol de Urânio-238, conforme a equação abaixo, é 50 vezes maior que a queima do metano:
!$ ^{238}_{92}U \rightarrow ^{234}_{90}Th + ^4_2He !$
Considerando a velocidade da luz igual a 3,0 x 108 m s-1 e as massas dos núcleos de urânio iguais a 238,0003, de tório iguais a 233,9942 e de hélio iguais a 4,0015, a energia liberada nessa reação é de:
Provas
Uma pilha pode ser construída com dois eletrodos de hidrogênio: o primeiro com 1,00 atm de gás hidrogênio e o segundo com uma solução ácida de pH = 2,0. A 298 K, observa-se que a corrente elétrica flui do primeiro eletrodo para o segundo, e o potencial da célula é de:
(Dados: R=8,314J mol-1 K-1; F=96500sAmol-1)
Provas
A decomposição térmica do ciclopropano ocorre a 500°C, formando o propeno. A velocidade dessa reação ocorre por um mecanismo de primeira ordem. Se a constante de velocidade dessa reação, nessa temperatura, é de 7 x 10-4 s-1, o tempo necessário para decompor 3 x 103 em 2,1 x 10-3 mol dm-3 é de aproximadamente:
(Dados: In = 2,3 log; log 2 = 0,3; log 3 = 0,47; log 5 = 0,69; log7=0,84)
Provas
O limoneno, produto natural encontrado na casca da laranja, é um composto com alto valor agregado, com diversas aplicações na indústria farmacêutica, e está representado a seguir:

Durante a síntese de uns desses materiais de interesse, o limoneno sofre hidrogenação catalítica, com o intuito de eliminar todas as suas insaturações. Em CNTP, o volume de hidrogênio necessário para obter o produto de interesse a partir de 8,5 9 de limoneno (teor de pureza de 80%) é de:
(Dados: MM limoneno = 136 g mol-1 ; Volume molar em CNTP = 22,4 L)
Provas
O brometo de benzila ou !$ \alpha !$-bromotolueno é um agente lacrimogênio que pode ser produzido a partir do benzeno em uma sequência de reações conforme o esquema simplificado a seguir:
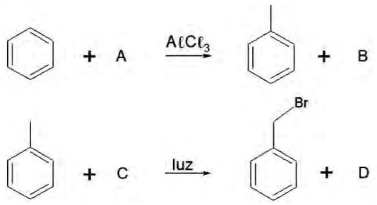
Os reagentes A e C que completam o esquema reacional são:
Provas
Na síntese de amônia para a produção de fertilizantes, o nitrogênio e o hidrogênio molecular são misturados sob alta temperatura e pressão, a fim de se obter o maior rendimento do produto de interesse. Supondo que a reação seja realizada em um recipiente de 10 litros, que a quantidade inicial de nitrogênio e de hidrogênio seja, respectivamente, de 3 e 8 mols e que no final do processo conste a presença de 1 mol de nitrogênio, a constante de equilíbrio em termos de concentração (Kc) nessas condições de temperatura e pressão é de aproximadamente:
Provas
Na atmosfera, a reação química entre NO e O3 acarreta a formação do seguinte óxido:
Provas
Uma alíquota de 20 mL de uma solução aquosa de HCI foi completamente neutralizada por 46 mL de solução aquosa 0,10 mol L-1 de NaOH. A concentração da solução de HCI, em mol L-1, é igual a:
Provas
Durante uma operação Industrial, 800 L de uma solução aquosa 0,10 mol L-1 de NaNO3 foram completamente misturados com 200 L de uma solução aquosa 0,20 mol L-1 de Mg(NO3)2. Assumindo que os solutos se encontram completamente dissociados, a concentração de íons nitrato, em mol L-1 na solução formada na mistura é igual a:
Provas
Em um laboratório, dispõe-se de uma solução com concentração percentual mássica 20% m/m e massa especifica 0,9 kg L-1. A concentração dessa solução, em gramas por litro, é expressa por:
Provas
Caderno Container