Foram encontradas 35.976 questões.
Analise as seguintes reações:
I. !$ \mathbf{ CH_{4(g)} + O_{2(g)} \rightarrow CO_{2(g)} + H_2 O_{(g)}} !$
II. !$ \mathbf{ CaO_{(s)} + CO_{2(g)} \rightarrow CaCO_{3(s)}} !$
III.!$ \mathbf{ Pb CO_{3(s)} \rightarrow PbO_{(s)} + CO_{2 (g)}} !$
IV.!$ \mathbf{ 2N_{2(g)} + 3H_{2(g)} \rightarrow 2 NH_{3(g)}} !$
V.!$ \mathbf{ Fe_{(s)} + 2 HCl_{(aq)} \rightarrow FeCl_{2(aq)} + H_{2(g)}} !$
Assinale a alternativa que classifica corretamente a reação apresentada.
Provas
A adrenalina ou epinefrina é um hormônio do corpo humano, secretado pelas glândulas suprarrenais e que atua no sistema nervoso simpático (neurotransmissor). Observe a fórmula estrutural da adrenalina:
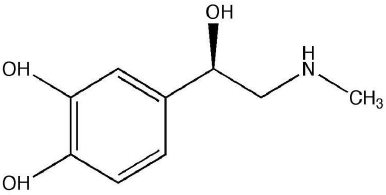
Sobre a molécula da adrenalina, assinale a alternativa CORRETA:
Provas
No laboratório de química foi realizado um experimento para detectar soluções eletrolíticas. O aparelho utilizado é esquematizado a seguir:
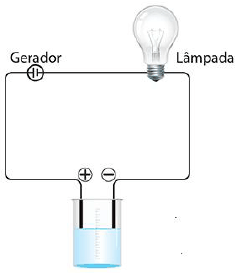
São solutos que, quando adicionados em quantidades adequadas à água, provocam brilho intenso na lâmpada, EXCETO:
Provas
Os elementos químicos têm presença marcante em nossa vida diária e em aspectos da tecnologia e da produção industrial. Muitas propriedades dos elementos químicos podem ser explicadas conforma a disposição na tabela periódica, sendo ela um instrumento de muita aplicabilidade na ciência.
Sobre a estrutura da tabela periódica e as propriedades periódicas dos elementos assinale a alternativa CORRETA:
Provas
Em uma aula prática de química um estudante distraído derrubou um frasco de solução de ácido sulfúrico 0,1M sobre a bancada causando o derramamento de 100mL do conteúdo. Para evitar acidentes, o ácido sulfúrico deve ser rapidamente neutralizado com carbonato ou bicarbonato de sódio.
Considerando que no laboratório há apenas um frasco com solução de bicarbonato de sódio 0,2M, assinale a alternativa que indica CORRETAMENTE o volume de bicarbonato de sódio que será necessário para completa neutralização do ácido sulfúrico derramado.
Provas
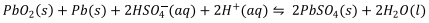
Dados: E° red (cátodo) = + 1,685 V e E° red (ânodo) = - 0,356 V
Analise as afirmações numeradas de I a IV em relação a esse tipo de bateria.
I. Os eletrodos de PbO2(s) e Pb(s) são inertes, sendo o potencial de pilha dependente apenas da concentração de ácido sulfúrico.
II. No processo de recarga da bateria ocorre redução do pH do meio aquoso.
III. O Pb(s) atua como agente redutor no processo de recarga da bateria.
IV. O processo de descarga leva a um potencial padrão de pilha de +2,041 V e a uma redução da densidade do eletrólito.
Assinale a alternativa CORRETA.
Provas
Ao longo do tempo, vários modelos foram propostos para compreender como era essa estrutura do átomo e quais as suas características. Cada modelo teve uma representação, para que houvesse uma melhor compreensão da conclusão de cada autor. Um dos modelos apresentados a partir das conclusões dos cientistas encontra-se a seguir.
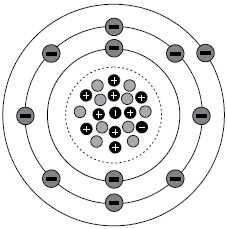
(https://conhecimentocientifico.com/modelos-atomicos-2/.Adaptado)
Esse modelo está de acordo com o seguinte cientista e sua descrição:
Provas
“Pegue uma lâmina de titanato de estrôncio (SrTiO3) e aqueça-a a 550 ºC. À parte, ferva separadamente um punhado de átomos de bismuto, estrôncio, cálcio, cobre e oxigênio. Quando os elementos químicos começarem a evaporar, abaixe o fogo e inicie a montagem das camadas atômicas dirigindo o vapor para a placa de SrTiO3. Vaporize cada elemento sobre a lâmina, alternando CuO2 e os átomos de estrôncio (Sr). Envolva as camadas com os demais elementos, bismuto (Bi) e cálcio (Ca), formando uma espécie de sanduíche. E, voilà! Sirva “quente”, a –23 ºC.”
(https://super.abril.com.br/ciencia/supercondutores-receita-francesa-para- -alcancar-um-recorde/. Adaptado)
Super condutores são materiais capazes de conduzir a eletricidade sem resistência, assim que atingem uma temperatura muito baixa. Em sua fabricação, indicada no texto, são utilizados vários elementos químicos e duas substâncias químicas, que são classificadas como
Provas
Água dura é o nome dado à água que contém sais de cálcio dissolvidos. Em aquíferos subterrâneos essa água é formada a partir da água da chuva, que dissolve dióxido de carbono do ar e forma uma solução muito diluída de ácido carbônico. Quando a água penetra o solo originado de rocha calcárea, o ácido carbônico reage com o carbonato de cálcio da rocha e forma o hidrogenocarbonato, que fica dissolvido nessa água. Para se obter água pura a partir da água dura, isto é, sem os sais de cálcio nela dissolvidos, o método mais adequado é o da
Provas
I. Na técnica de absorção atômica, os átomos da amostra absorvem parte da radiação proveniente de uma lâmpada e a luz não absorvida alcança o detector. A absorbância de um elemento químico, que é proporcional à sua concentração, pode ser determinada experimentalmente para cada pico referente ao elemento.
II. Na técnica de emissão atômica, nenhuma fonte de radiação precisa ser utilizada. A temperatura da chama e as colisões promovem os átomos da amostra a estados excitados que emitem fótons espontaneamente ao retornarem ao estado fundamental. A intensidade de emissão de um elemento químico é proporcional à sua concentração.
III. No experimento de fluorescência atômica, os átomos da amostra são irradiados com um laser e promovidos a estados excitados a partir do qual eles podem fluorescer para retornarem ao estado fundamental. Como esse processo envolve transições não-radiativas, a intensidade de emissão de um elemento não deve ser usada para determinar sua concentração.
Assinale a alternativa que contém as afirmativas CORRETAS.
Provas
Caderno Container