Foram encontradas 35.936 questões.
Assinale a opção que apresenta a sequência que melhor descreve o ciclo de ações envolvidas no método científico (hipotético - dedutivo):
Provas
Considere a seguinte configuração experimental, constituída de um canhão de partículas !$ \alpha !$, dois detectores de partículas !$ \alpha !$ posicionados ortogonalmente entre si e uma folha fina de um determinado material (W, X, Y, Z).
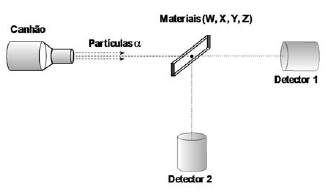
Experimentos foram realizados, bombardeando cada material com uma quantidade de partículas !$ \alpha !$ e registrando o número de partículas coletadas em cada detector, conforme a tabela abaixo.
| Experimento | Partículas lançadas | Material | Partículas Coletadas | |
| Detector 1 | Detector 2 | |||
| I | 8000 | W | 7903 | 1 |
| II | 10 | X | 10 | 0 |
| III | 10 | Y | 10 | 0 |
| IV | 10 | Z | 10 | 0 |
A partir dessas informações, assinale a alternativa que apresenta a conclusão CORRETA sobre as observações feitas nos experimentos.
Provas
Sistemas compostos por água e tensoativos em diferentes proporções, depois de homogeneizados, passam por um processo termodinâmico quando atingem temperaturas em torno de 0°C. A variação de entalpia (ΔH) desse processo foi determinada para cada mistura em função da composição do sistema, conforme apresentado no gráfico.
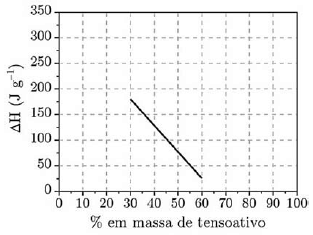
Considere que o ponto de fusão do tensoativo puro é menor que -20 °C e o calor latente de fusão da água pura é 334 J.g-1. Sobre esses sistemas são feitas as seguintes afirmações:
I. O ΔH refere-se à transição de fase do tensoativo.
II. O calor latente de fusão do tensoativo puro é -180 J.g-1.
III. Até 35% em massa de água pode se apresentar na forma associada à substância e não funde.
IV. O ΔH é proporcional à quantidade de água não associada ao tensoativo.
Com base no gráfico e nas informações do enunciado, assinale a opção que indica a(s) afirmação(ões) CORRETA(S).
Provas
São feitas as seguintes afirmações a respeito do ciclo do oxigênio no meio ambiente:
l. A concentração de oxigênio na atmosfera está diminuindo significativamente no último século, devido à queima de combustíveis fósseis e à redução da vegetação terrestre e marinha.
II. Os maiores contribuintes para a produção de oxigênio e sua liberação na atmosfera terrestre são florestas densas, pastagens, ervas e arbustos.
III. O oxigênio está envolvido, em algum grau, em todos os outros ciclos biogeoquímicos.
IV. Águas doces frias são as maiores fontes de oxigênio livre na Terra.
Assinale a alternativa que apresentam as afirmações ERRADAS.
Provas
Considere as seguintes afirmações sobre os aminoácidos:
I. Os aminoácidos são pequenas moléculas com propriedades bioquímicas únicas determinadas por seus grupos funcionais.
II. Os aminoácidos em pH fisiológico (~7,4) apresentam os grupamentos amina protonados, enquanto os grupos carboxílicos assumem sua forma de base conjugada.
III. Os aminoácidos podem se polimerizar por meio de reações de adição para formar as ligações peptídicas (CO-NH).
IV. Às variações no comprimento e sequência de aminoácidos de polipeptídios são características que contribuem para a diversidade na forma e nas funções biológicas das proteínas.
V. Todos os aminoácidos obtidos de polipeptídios são opticamente ativos, isto é, eles desviam o plano da luz polarizada.
Assinale a alternativa que apresenta as afirmações CORRETAS.
Provas
O tempo de meia vida do 231Pa é 3,25 x 104 anos. Assinale a alternativa que apresenta a massa restante (em dg) de uma amostra inicial de 376,15 dg, após 3,25 x 105 anos.
Provas
Sobre a energia reticular, assinale a alternativa ERRADA.
Provas
Considere os seguintes pares de substâncias líquidas a 25ºC:
I. Água e metanol.
II. Acetona e dissulfeto de carbono.
III. Acetona e clorofórmio.
IV. n-hexano e n-heptano.
V. Metanol e etanol.
Assinale a alternativa que apresenta os pares de substâncias que formam soluções consideradas ideais.
Provas
Considere a representação simplificada dos seguintes decaimentos radioativos conhecidos:
!$ ^{238}_{92} U \xrightarrow {x_1} ^{234}_{90}Th !$
!$ ^{234}_{90} Th \xrightarrow {x_2} ^{234}_{91}Pa !$
!$ ^{222}_{86} Rn \xrightarrow {x_3} ^{218}_{84}Po !$
!$ ^{218}_{84} Po \xrightarrow {x_4} ^{214}_{82}Pb !$
!$ ^{214}_{82} Pb \xrightarrow {x_5} ^{214}_{83}Bi !$
Com relação aos decaimentos acima, é possível afirmar que:
Provas
Uma amostra de 390 g de sulfito de cálcio com 25% de impurezas, em massa, é atacada por ácido clorídrico concentrado em um meio reacional a 2 atm e 300 K. Considere comportamento ideal de gases.
Dados:
• massa molar do enxofre = 32 g.mol-1;
• massa molar do cálcio = 40 g.mol-1; e
• massa molar do oxigênio = 16 g.mol-1.
Pode-se afirmar que o volume, em litros, de anidrido sulforoso obtido pelo consumo completo do sulfito é:
Provas
Caderno Container