Foram encontradas 35.936 questões.
Considere a célula eletroquímica abaixo:
!$ Pt(s)|H_2(g)|HCl(aq)||Hg_2Cl_2(s)|Hg(l) !$
Admita, ainda, a reação a seguir:
!$ Hg_2Cl_2(s) + H_2(g) \rightarrow 2Hg(l) + 2HCl(aq) !$
O potencial-padrão da célula acima a 294,5 K é +0,2678 V e a 302,5 K é +0,2638 V. Considere que tanto a entalpia, quanto a entropia de reação mudam muito pouco para variações de temperatura não muito amplas. A constante de Faraday é 96500 C.mol-1. A entropia-padrão da reação acima, a 298,15 K, em J.(K.mol)-1, será aproximadamente:
Provas
Bicarbonato de sódio reage estequiometricamente, em processo isotérmico a 300 K, com 50 mL de uma solução aquosa de um ácido monoprótico forte, em um recipiente rígido e fechado que, quando vazio, apresenta um volume útil de 74,9 mL, conforme o esboço abaixo:

O cristal piezoelétrico tem espessura (t) de 2 mm e suscetibilidade voltaica !$ (\Phi) !$ de 0,050 V.(m.Pa)-1 e, quando a reação atinge o equilíbrio, fornece um potencial elétrico (U) de 1,0 V. Considere a solubilidade molar de gases na água desprezível e a constante universal dos gases R = 8,3 J.(mol.K)-1. Se o volume reacional é constante e igual ao volume da solução ácida inicial, a concentração molar inicial da solução do ácido monoprótico, em mol.L-1, é:
Provas
É correto afirmar que:
Provas
Assinale a afirmativa correta sobre as propriedades e características dos polímeros.
Provas
Na desidratação a alta temperatura de uma mistura reacional composta pelos ácidos fórmico, acético e propiônico, qual a quantidade máxima de diferentes anidridos que poderá ser obtidos?
Provas
Considere a seguinte reação em equilíbrio:
!$ 2SO_2(g) + O_2(g) \rightleftharpoons 2SO_3(g) !$
Dados:
• R = 8,3 J.(K.mol)-1;
• ln 1,6 = 0,47; e
• ln 10 = 2,3.
Sabe-se que a constante de equilíbrio dessa reação é 4,0.1024, a 27 ºC e 2,5.1010, a 227 ºC.
Qual a variação de entalpia padrão da reação, em kJ.mol-1, considerando que ela seja constante nessa faixa de temperatura?
Provas
A figura é uma representação esquemática de uma estação de tratamento de água. Nela podem ser observadas as etapas que vão desde a captação em represas até a distribuição à população. No intuito de minimizar o custo com o tratamento, foi proposta a eliminação da etapa de adição de hipoclorito de sódio e o resultado foi comparado com o da água tratada em todas as etapas.
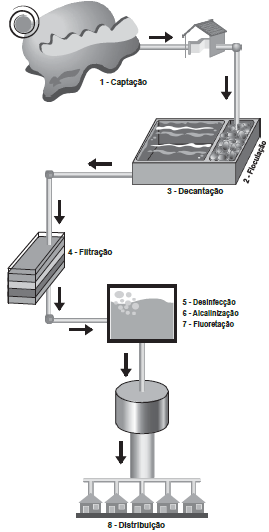
Disponível em: http://ecopoa.orgfree.com. Acesso em: 18 dez. 2012 (adaptado).
Caso fosse aceita a proposta apresentada, qual seria a mudança principal observada na qualidade da água que seria distribuída às residências?
Provas
Um marceneiro esqueceu um pacote de pregos ao relento, expostos à umidade do ar e à chuva. Com isso, os pregos de ferro, que tinham a massa de 5,6 g cada, acabaram cobertos por uma camada espessa de ferrugem (Fe2O3 −H2O), uma substância marrom insolúvel, produto da oxidação do ferro metálico, que ocorre segundo a equação química:
2 Fe (s) + 3!$ \dfrac{3}{2} !$O2 (g) + H2O (l) — Fe2O3 −H2O (s)
Considere as massas molares (g/mol): H = 1; O = 16; Fe = 56.
Qual foi a massa de ferrugem produzida ao se oxidar a metade (50%) de um prego?
Provas
Uma antiga forma de produzir um dos constituintes de argamassas é o aquecimento a altas temperaturas de materiais componentes dos sambaquis, que são sítios arqueológicos formados essencialmente por restos de moluscos. A decomposição térmica da principal substância desses sítios arqueológicos resulta na formação de dois compostos apenas. Um deles é um óxido sólido e o outro é um óxido gasoso. A reação do primeiro com água resulta na formação de Ca(OH)2 (aquoso), enquanto a reação do segundo resulta em H2CO3 (aquoso). A fórmula da principal substância encontrada nesses sítios arqueológicos é:
Provas
Para preparar o vinho de laranja, caldo de açúcar é misturado com suco de laranja, e a mistura é passada em panos para retenção das impurezas. O líquido resultante é armazenado em garrafões, que são tampados com rolhas de cortiça. Após oito dias de repouso, as rolhas são substituídas por cilindros de bambu e, finalmente, após dois meses em repouso ocorre novamente a troca dos cilindros de bambu pelas rolhas de cortiça.
RESENDE, D. R.; CASTRO, R. A.; PINHEIRO, P. C. O saber popular nas aulas de química: relato de experiência envolvendo a produção do vinho de laranja e sua interpretação no ensino médio. Química Nova na Escola, n. 3, ago. 2010 (adaptado).
Os processos físico e químico que ocorrem na fabricação dessa bebida são, respectivamente,
Provas
Caderno Container