Foram encontradas 35.934 questões.
Na Idade Média, para fabricarem tintas, os pintores usavam algum tipo de substância líquida e colante, como a clara do ovo, que era o meio dispersante utilizado para a fixação da cor. O colorante era comumente obtido de algum mineral que contivesse um composto inorgânico principal. Para obterem as tintas destinadas à pintura, os pintores medievais moíam e misturavam antes os pigmentos, para, em seguida, acrescentá-los aos ligantes. Para tal, usavam uma pedra e um pilão de face plana. Quanto mais fino o pigmento (partículas micrométricas ou nanométricas), melhor era a qualidade da tinta.
Internet: <www.bdce.unb.br> (com adaptações).
Na tabela a seguir, são listadas algumas cores e a composição principal do pigmento mineral correspondente a cada uma delas.
|
cor |
compostos principais |
|
verde |
NiCO3 |
|
amarelo |
CdS, ZnCrO4 |
|
branco |
TiO2, ZnO, Sb2O3 |
|
vermelho |
Fe2O3 |
|
violeta |
Co3(PO4)2 |
Considerando as informações do texto e da tabela precedentes, julgue o item.
Um dos compostos formados pela troca simultânea entre os cátions e os ânions dos compostos Fe2O3 e Co3(PO4)2 é o FePO4.
Provas
Na Idade Média, para fabricarem tintas, os pintores usavam algum tipo de substância líquida e colante, como a clara do ovo, que era o meio dispersante utilizado para a fixação da cor. O colorante era comumente obtido de algum mineral que contivesse um composto inorgânico principal. Para obterem as tintas destinadas à pintura, os pintores medievais moíam e misturavam antes os pigmentos, para, em seguida, acrescentá-los aos ligantes. Para tal, usavam uma pedra e um pilão de face plana. Quanto mais fino o pigmento (partículas micrométricas ou nanométricas), melhor era a qualidade da tinta.
Internet: <www.bdce.unb.br> (com adaptações).
Na tabela a seguir, são listadas algumas cores e a composição principal do pigmento mineral correspondente a cada uma delas.
|
cor |
compostos principais |
|
verde |
NiCO3 |
|
amarelo |
CdS, ZnCrO4 |
|
branco |
TiO2, ZnO, Sb2O3 |
|
vermelho |
Fe2O3 |
|
violeta |
Co3(PO4)2 |
Considerando as informações do texto e da tabela precedentes, julgue o item.
Infere-se do texto que a obtenção de uma tinta com mistura homogênea depende do grau de moagem do pigmento.
Provas
Na Idade Média, para fabricarem tintas, os pintores usavam algum tipo de substância líquida e colante, como a clara do ovo, que era o meio dispersante utilizado para a fixação da cor. O colorante era comumente obtido de algum mineral que contivesse um composto inorgânico principal. Para obterem as tintas destinadas à pintura, os pintores medievais moíam e misturavam antes os pigmentos, para, em seguida, acrescentá-los aos ligantes. Para tal, usavam uma pedra e um pilão de face plana. Quanto mais fino o pigmento (partículas micrométricas ou nanométricas), melhor era a qualidade da tinta.
Internet: <www.bdce.unb.br> (com adaptações).
Na tabela a seguir, são listadas algumas cores e a composição principal do pigmento mineral correspondente a cada uma delas.
| cor | compostos principais |
| verde | NiCO3 |
| amarelo | CdS, ZnCrO4 |
| branco | TiO2, ZnO, Sb2O3 |
| vermelho | Fe2O3 |
| violeta | Co3(PO4)2 |
Considerando as informações do texto e da tabela precedentes, assinale a opção correta.
O método mais indicado para separar o pigmento de seu meio dispersante nas tintas de que trata o texto é a
Provas
O peróxido de hidrogênio (H2O2), um dos agentes mais empregados em desinfecções, decompõe-se lentamente em água e oxigênio, conforme se observa na equação que se segue.
2 H2O2 (aq) → 2 H2O (l) + O2 (g)
Esse processo pode ser acelerado pela adição de HBr, cujo mecanismo envolve duas etapas, conforme as representações I e II, a seguir.
I 2Br− (aq) + H2O2 (aq) + 2 H+ (aq) → Br2 (aq) + 2 H2O (l)
II Br2 (aq) + H2O2 (aq) → 2 Br− (aq) + 2 H+ (aq) + O2 (g)
No gráfico seguinte, é representada a variação da entalpia em função da coordenada da reação referente ao mecanismo anterior nas condições padrão.
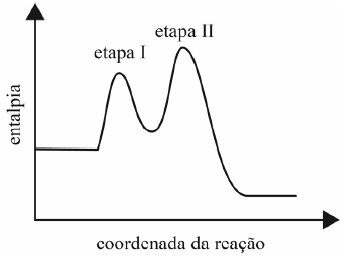
Com base nessas informações, julgue o item subsequente.
Dados o mecanismo e o perfil de variação de entalpia, infere-se que a decomposição do peróxido de hidrogênio na presença de HBr é uma reação com cinética de segunda ordem.
Provas
O peróxido de hidrogênio (H2O2), um dos agentes mais empregados em desinfecções, decompõe-se lentamente em água e oxigênio, conforme se observa na equação que se segue.
2 H2O2 (aq) → 2 H2O (l) + O2 (g)
Esse processo pode ser acelerado pela adição de HBr, cujo mecanismo envolve duas etapas, conforme as representações I e II, a seguir.
I 2Br− (aq) + H2O2 (aq) + 2 H+ (aq) → Br2 (aq) + 2 H2O (l)
II Br2 (aq) + H2O2 (aq) → 2 Br− (aq) + 2 H+ (aq) + O2 (g)
No gráfico seguinte, é representada a variação da entalpia em função da coordenada da reação referente ao mecanismo anterior nas condições padrão.

Com base nessas informações, julgue o item subsequente.
Na etapa I, o peróxido de hidrogênio atua como redutor, e, na etapa II, como oxidante.
Provas
O peróxido de hidrogênio (H2O2), um dos agentes mais empregados em desinfecções, decompõe-se lentamente em água e oxigênio, conforme se observa na equação que se segue.
2 H2O2 (aq) → 2 H2O (l) + O2 (g)
Esse processo pode ser acelerado pela adição de HBr, cujo mecanismo envolve duas etapas, conforme as representações I e II, a seguir.
I 2Br− (aq) + H2O2 (aq) + 2 H+ (aq) → Br2 (aq) + 2 H2O (l)
II Br2 (aq) + H2O2 (aq) → 2 Br− (aq) + 2 H+ (aq) + O2 (g)
No gráfico seguinte, é representada a variação da entalpia em função da coordenada da reação referente ao mecanismo anterior nas condições padrão.

Com base nessas informações, julgue o item subsequente.
O íon brometo, apesar de reagir na etapa I, atua como catalisador do processo de decomposição do peróxido de hidrogênio.
Provas
O peróxido de hidrogênio (H2O2), um dos agentes mais empregados em desinfecções, decompõe-se lentamente em água e oxigênio, conforme se observa na equação que se segue.
2 H2O2 (aq) → 2 H2O (l) + O2 (g)
Esse processo pode ser acelerado pela adição de HBr, cujo mecanismo envolve duas etapas, conforme as representações I e II, a seguir.
I 2Br− (aq) + H2O2 (aq) + 2 H+ (aq) → Br2 (aq) + 2 H2O (l)
II Br2 (aq) + H2O2 (aq) → 2 Br− (aq) + 2 H+ (aq) + O2 (g)
No gráfico seguinte, é representada a variação da entalpia em função da coordenada da reação referente ao mecanismo anterior nas condições padrão.

Com base nessas informações, julgue o item subsequente.
No processo de decomposição do peróxido de hidrogênio em condições padrão, a energia absorvida para romper as ligações da molécula de H2O2 é superior à energia liberada na formação das ligações das moléculas H2O e O2.
Provas
A titulação é uma técnica muito utilizada na química para determinar a quantidade de uma espécie química em uma solução (amostra). Na titulação, uma segunda solução, de concentração conhecida de outra espécie que reage com a primeira e cuja concentração se deseja determinar, é adicionada gradualmente à amostra que contém a substância, ou espécie, de interesse.
Com base nesses princípios, um estudante idealizou um experimento para determinar a quantidade de CO2 contida em um cilindro rígido, tendo realizado o trabalho em três etapas:
I borbulhou o CO2 em água destilada, de modo que todo o CO2 contido no cilindro se transformasse em H2CO3, formando uma solução desse ácido;
II titulou, completamente, a solução de H2CO3 preparada, com uma solução de NaOH de concentração 0,1 mol/L;
III determinou, por meio de cálculos estequiométricos, o volume de CO2 inicialmente contido no cilindro, considerando todas as condições do experimento ideais e rendimentos reacionais completos.
Tendo como referência o texto e a situação hipotética precedentes, julgue o item.
O aumento tanto da pressão parcial de CO2 quanto da temperatura da água destilada torna a etapa I mais eficiente.
Provas
A titulação é uma técnica muito utilizada na química para determinar a quantidade de uma espécie química em uma solução (amostra). Na titulação, uma segunda solução, de concentração conhecida de outra espécie que reage com a primeira e cuja concentração se deseja determinar, é adicionada gradualmente à amostra que contém a substância, ou espécie, de interesse.
Com base nesses princípios, um estudante idealizou um experimento para determinar a quantidade de CO2 contida em um cilindro rígido, tendo realizado o trabalho em três etapas:
I borbulhou o CO2 em água destilada, de modo que todo o CO2 contido no cilindro se transformasse em H2CO3, formando uma solução desse ácido;
II titulou, completamente, a solução de H2CO3 preparada, com uma solução de NaOH de concentração 0,1 mol/L;
III determinou, por meio de cálculos estequiométricos, o volume de CO2 inicialmente contido no cilindro, considerando todas as condições do experimento ideais e rendimentos reacionais completos.
Tendo como referência o texto e a situação hipotética precedentes, julgue o item.
Considere que, no experimento citado, a amostra de CO2 estivesse sob pressão de 20 atm no cilindro rígido em questão, pela manhã, a uma temperatura ambiente de 10 ºC. Considere, também, que à tarde a temperatura ambiente tenha chegado a 30 ºC e que, tanto de manhã quanto à tarde, a temperatura do cilindro tenha sido igual à temperatura ambiente. Nesse caso, à tarde a pressão no cilindro seria maior que 50 atm.
Provas
A titulação é uma técnica muito utilizada na química para determinar a quantidade de uma espécie química em uma solução (amostra). Na titulação, uma segunda solução, de concentração conhecida de outra espécie que reage com a primeira e cuja concentração se deseja determinar, é adicionada gradualmente à amostra que contém a substância, ou espécie, de interesse.
Com base nesses princípios, um estudante idealizou um experimento para determinar a quantidade de CO2 contida em um cilindro rígido, tendo realizado o trabalho em três etapas:
I borbulhou o CO2 em água destilada, de modo que todo o CO2 contido no cilindro se transformasse em H2CO3, formando uma solução desse ácido;
II titulou, completamente, a solução de H2CO3 preparada, com uma solução de NaOH de concentração 0,1 mol/L;
III determinou, por meio de cálculos estequiométricos, o volume de CO2 inicialmente contido no cilindro, considerando todas as condições do experimento ideais e rendimentos reacionais completos.
Tendo como referência o texto e a situação hipotética precedentes, julgue o item.
É neutro o pH de uma solução que contenha 8,0 g NaOH e 6,2 g de H2CO3.
Provas
Caderno Container