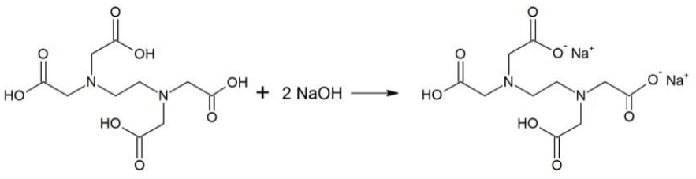
O ácido etilenodiamino tetra-acético (EDTA) é usado como “sequestrante” em detergentes, impedindo a precipitação do surfactante (princípio ativo) pelos íons \( Ca^{+2}, Mg^{+2} e Fe^{+3} \) presentes na água. Em análise química, o EDTA é utilizado como titulante para a determinação de dureza (\( Ca^{+2}, Mg^{+2} \)) de águas, cujo sal dissódico é obtido pela seguinte reação:
| Dados: Constantes de dissociação do EDTA | |
| \( K_{a1} = 1,02\; x\; 10^{-2} \) | \( pK_{a1} = 1,99 \) |
| \( K_{a2} = 2,14\; x\; 10^{-3} \) | \( pK_{a2} = 2,67 \) |
| \( K_{a3} = 6,92\; x\; 10^{-7} \) | \( pK_{a3} = 6,16 \) |
| \( K_{a4} = 5,5\; x\; 10^{-11} \) | \( pK_{a4} = 10,26 \) |
De acordo com a reação de neutralização parcial do EDTA acima apresentada, assinale a alternativa que apresenta o intervalo de pH no qual é obtido apenas o sal dissódico.
Provas
Questão presente nas seguintes provas