Foram encontradas 40 questões.
- Código PenalCrimes Contra a Administração PúblicaPraticados por Funcionário PúblicoConcussão e Excesso de Exação
De acordo com o Código Penal e a interpretação dos tribunais, a exigência ou solicitação de quantia de dinheiro para “furar a fila” de atendimento no Sistema Único de Saúde configura o crime de:
Provas
A ação de “retardar ou deixar de praticar, indevidamente, ato de ofício, ou praticá-lo contra disposição expressa de lei, para satisfazer interesse ou sentimento pessoal” configura crime de:
Provas
Sobre as pessoas jurídicas no direito civil brasileiro, assinale a alternativa correta.
Provas
Sobre a obrigação de indenizar a responsabilidade civil no direito brasileiro, assinale a alternativa INCORRETA.
Provas
As atividades realizadas nos laboratórios didáticos de Química precisam ser acompanhadas do descarte correto dos resíduos produzidos durante as aulas experimentais, sendo importante classificar os resíduos e escolher o tratamento mais adequado. Nesse sentido, numere a coluna da direita de acordo com sua correspondência com a coluna da esquerda.
1. Resíduos básicos concentrados, p. ex. aminas.
2. Resíduos fortemente oxidantes em solução, p. ex. permanganato.
3. Resíduo de mercúrio metálico.
4. Resíduo contendo sais de cianeto em solução aquosa diluída.
( ) Tratar com sulfito de sódio e depois ajustar o pH entre 7 e 9.
( ) Recobrir o resíduo com enxofre em pó e armazenar.
( ) Diluir até obtenção de uma solução com pelo menos 50% de água (em volume) e, em seguida, ajustar o pH entre 7 e 9.
( ) Adicionar 1 grama de NaOH por 100 mL de solução. Adicionar água sanitária.
Assinale a alternativa que apresenta a numeração correta da coluna da direita, de cima para baixo.
Provas
O ácido nítrico “branco” (100% puro; P.E. = 83 ºC) pode ser obtido em laboratório por destilação de uma mistura de \( KNO_3 \) e \( H_2SO_4 \), como mostra a reação a seguir:
\( KNO_3 + H_2SO_4 → HNO_3 + KHSO_4 \)
Tendo em vista que o \( HNO_3 \) é decomposto por aquecimento a \( NO_2 \) e \( H_2O \), assinale a alternativa que apresenta a técnica de destilação que deve ser utilizada nesse processo.
Provas
O ácido fosfórico (\( H_3PO_4 \)) de alta pureza é obtido por via seca ou térmica, pela combustão do fósforo elementar e posterior hidratação do \( P_2O_5 \), de acordo com as reações abaixo:
\( 4P + 5O_2 → 2P_2O_5 \;\; ΔH= -720 kcal \)
\( P_2O_5 + 3H_2O → 2H_3PO_4 \;\; ΔH= -45 kcal \)
Nesse processo, de acordo com as equações acima, assinale a alternativa que apresenta a quantidade de calor liberado na formação do \( H_3PO_4 \) (em kcal/mol).
Provas
Foi requisitado a um técnico de laboratório que preparasse uma solução de hidróxido de amônio, a partir de uma solução comercial concentrada, cujo rótulo contém as informações ao lado:
Dados: MM(\( NH_3 \)) = 17g/mol
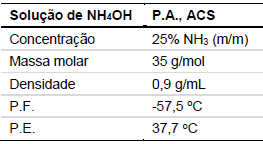
Assinale a alternativa que indica o volume aproximado da solução comercial (em mL) que o técnico deve utilizar para obter 5 litros de uma solução de \( NH_4OH \) 1 mol/L.
Provas
O jeans com aspecto “desbotado” pode ser obtido pela oxidação parcial do índigo impregnado no tecido (denim), utilizando-se uma solução de \( KMnO_4 \), como ilustrado pelo esquema reacional a seguir. Devido à formação de \( MnO_2 \), sólido castanho insolúvel em água, um outro reagente deve ser usado para que ele não impregne o tecido.
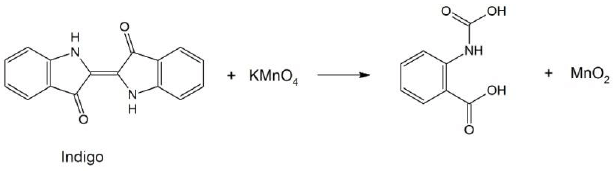
De acordo com os potenciais de redução fornecidos na tabela ao lado, assinale a alternativa que apresenta substâncias que podem ser usadas para transformar o \( MnO_2 \) na espécie solúvel \( Mn^{+2} \).

Provas
O ácido etilenodiamino tetra-acético (EDTA) é usado como “sequestrante” em detergentes, impedindo a precipitação do surfactante (princípio ativo) pelos íons \( Ca^{+2}, Mg^{+2} e Fe^{+3} \) presentes na água. Em análise química, o EDTA é utilizado como titulante para a determinação de dureza (\( Ca^{+2}, Mg^{+2} \)) de águas, cujo sal dissódico é obtido pela seguinte reação:
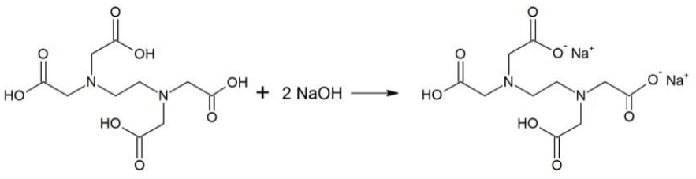
| Dados: Constantes de dissociação do EDTA | |
| \( K_{a1} = 1,02\; x\; 10^{-2} \) | \( pK_{a1} = 1,99 \) |
| \( K_{a2} = 2,14\; x\; 10^{-3} \) | \( pK_{a2} = 2,67 \) |
| \( K_{a3} = 6,92\; x\; 10^{-7} \) | \( pK_{a3} = 6,16 \) |
| \( K_{a4} = 5,5\; x\; 10^{-11} \) | \( pK_{a4} = 10,26 \) |
De acordo com a reação de neutralização parcial do EDTA acima apresentada, assinale a alternativa que apresenta o intervalo de pH no qual é obtido apenas o sal dissódico.
Provas
Caderno Container