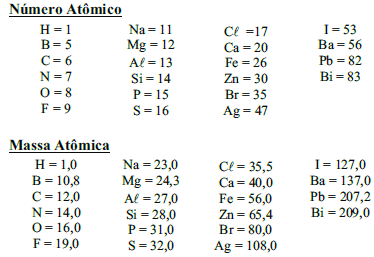
Constante Universal dos Gases Ideais: !$ R = 0,082 { \Large { atm.L \over mol.K}} !$
log10 1,111 = 0,0457
log10 2,08 = 0,318
ln 2,329 = 0,845
1 atm = 1,013 x 106 g.cm-1.s-1
1 atm = 760mmHg
A 300ºC a constante de velocidade para a reação:
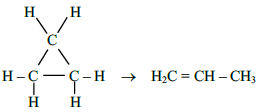
é 2,41x10-10s-1. A 400ºC seu valor é de 1,16x10-6s-1. Sendo !$ R = 8,314 { \large Joule \over mol\,x\,K} !$ (constante geral dos gases), podemos afirmar que a energia de ativação para essa reação é aproximadamente: