A equação de Clapeyron estabelece que o produto da pressão p e o volume V ocupado por um gás é igual ao produto da quantidade de matéria n do gás por sua temperatura T (em graus absoluto) e uma constante R, a denominada constante dos gases ideias:
pV = nRT [Equação de Clapeyron]
Gases que seguem exatamente o comportamento descrito pela equação de Clapeyron são denominados gases ideais.
Para qualquer gás, ideal ou não ideal, pode-se formar uma função termodinâmica chamada fator de compressibilidade, Z(p), e definida pela razão
!$ Z(p) = \dfrac {pV} {nRT} !$ Fator de compressabilidade de um gás]
Na figura abaixo, é apresentado o comportamento da função Z(p) em função da pressão p para 1 (um) mol dos gases nitrogênio (N2), metano (CH4), hidrogênio (H2) e dióxido de carbono (CO2), todos obtidos à temperatura ambiente.
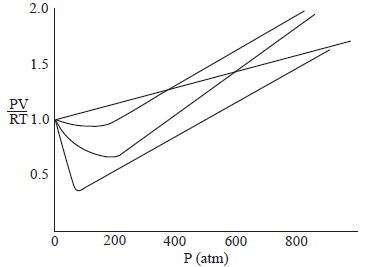
Variação da função fator de compressibilidade
Z(p) = pV / nRT em função da pressão para os gases
nitrogênio, metano, hidrogênio e dióxido de carbono
obtido a 25º.
Com as informações apresentadas, conclui-se que, à temperatura de 25º C: