A equação de Johannes Diderik van der Waals foi desenvolvida em 1873, com o propósito de considerar, no comportamento dos gases, as dimensões e as interações intermoleculares dos seus constituintes microscópicos. Sendo assim, van der Waals escreveu a equação
!$ P=\dfrac{RT}{Vm-b}-\dfrac{a}{V\underset{m}{2}} !$
em que p é a pressão, R é a constante dos gases; T, a temperatura absoluta; e Vm, o volume molar do gás em descrição.
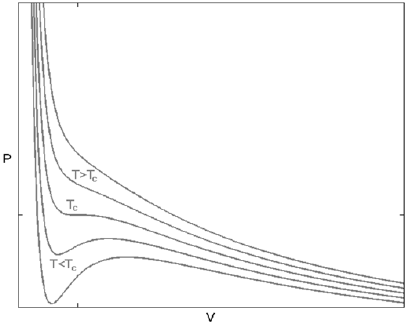
em que p é a pressão, R é a constante dos gases; T, a temperatura absoluta; e Vm, o volume molar do gás em descrição. Disponível em: <https://en.wikipedia.org/wiki/Van_der_Waals_equation#/ media/File:Van_der_Waals_Isotherms.PNG>. Acesso em: 24 set. 2022.
Sabendo que esse modelo produz as isotermas apresentadas, considerando os valores de temperatura relativos à temperatura crítica do material em estudo, e que o gás é composto por uma substância somente, assinale a alternativa correta.