Foram encontradas 60 questões.
A química quântica é a aplicação da mecânica quântica a problemas químicos, como, por exemplo, a descrição da estrutura eletrônica de átomos e de moléculas e os efeitos sobre sua reatividade. A base para a maioria dos métodos químicos quânticos é a equação de Schrödinger, que inicialmente foi resolvida para descrição do átomo de hidrogênio e que, em um segundo momento, foi numericamente solucionada para os sistemas moleculares. Em relação a esse assunto, assinale a alternativa correta.
Provas
A teoria do orbital molecular é uma das duas formas complementares de descrever a estrutura eletrônica das moléculas, ao lado da teoria da ligação de valência. O método foi desenvolvido por Friedrich Hund e Robert S. Mulliken e é usado atualmente para a maioria dos cálculos químicos quânticos. Acerca desse tema, assinale a alternativa correta.
Provas
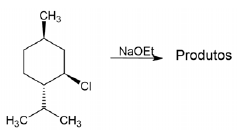
Assinale a alternativa que corresponde ao produto principal do fenômeno apresentado.
Provas
Assinale a alternativa que indica a compatibilidade entre as substâncias e os riscos associados à manipulação dos produtos químicos.
Provas
No que se refere à química dos compostos de coordenação, assinale a alternativa correta.
Provas
Uma das equações mais importantes na eletroquímica é a equação de Nernst. Isso porque tal formulação une a informação de dois potenciais: os potenciais químicos e elétricos em uma reação de oxirredução. Assim, a partir das relações !$ ΔG_r=-nFE\,\,e\,\,ΔG_r=ΔG\stackrel{o}{r}+RT\,ln\,Q !$, Nernst encontrou que
!$ E_{cel}=E\stackrel{o}{c}el-\dfrac{RT}{nF}ln\,Q !$
em que G é a energia livre de Gibbs, n é o número de elétrons envolvidos na reação de oxirredução, F é a constante de Faraday, E é o potencial elétrico da célula e Q, o quociente da reação. Com base nessas informações, assinale a alternativa correspondente à equação que relaciona o potencial elétrico de uma célula eletroquímica e a temperatura, assumindo que as variações de entalpia e de entropia de uma reação sejam constantes com a temperatura
Provas
A reação a seguir ocorre em um mecanismo ainda incógnito para um grupo de pesquisadores.
!$ A+B→C !$
Ao tentar descobrir as reações elementares que se sucedem na reação global, tais químicos encontraram os seguintes dados acerca da cinética da reação:
|
!$ \dfrac{v_A}{mol·L^{-1}·s^{-1}} !$ |
!$ \dfrac{v_B}{mol·L^{-1}·s^{-1}} !$ |
!$ \dfrac{v_C}{mol·L^{-1}·s^{-1}} !$ |
|
- 0,01 |
- 0,01 |
- 0,02 |
|
- 0,01 |
- 0,02 |
- 0,04 |
|
- 0,02 |
- 0,02 |
- 0,16 |
Desse modo, inicialmente puderam assegurar que a cinética da reação obedece a determinada equação de velocidade. Assinale a alternativa que indica essa equação.
Provas
Sabendo que o complexo !$ FeSCN^{2+} !$ tem absortividade molar !$ ∈= !$ 7000 !$ L !$ !$ · !$ !$ cm^{-1} !$ !$ · !$ !$ mol^{-1} !$, sob o comprimento de onda igual a 580 nm, calcule a absorbância de uma solução de concentração igual a 8,15 ppm. Considere o caminho ótico igual a 1cm e a massa molar do !$ FeSCN^{2+} !$ igual a 114 g/mol.
Provas
O processo de transformação da magnetita para a hematita pode ser representado da forma a seguir.
!$ 2Fe_30_4(s)+\dfrac{1}{2}0_2(g)→3Fe_20_3(s) !$
| !$ \dfrac{ΔH\stackrel{0}{f}(300K)}{KJ·mol^{-1}} !$ |
!$ \dfrac{s\stackrel{0}{m}(300K)}{J·K^{-1}·mol^{-1}} !$ |
|
|
!$ Fe_30_4 !$ |
-1118,4 |
146,4 |
|
!$ Fe_20_3 !$ |
-824,2 |
87,4 |
| !$ 0_2 !$ | 0 | 205 |
Com base nos dados termoquímicos demonstrados nessa tabela, a transformação da magnetita para hematita consiste em um processo
Provas
Considere que 2 mols de gás carbônico se expandam de 3 L a 6 L, isotérmica e reversivelmente, a uma temperatura de 27 oC. Sabendo que o trabalho é definido como
!$ W=-\textstyle \int\limits_{vi}^{v_f}p\,\,dV !$
e considerando o gás como perfeito, qual é o valor aproximado de W, em Joules, para essa expansão?
Dados: !$ R= !$ 8,314 !$ J/(K\,\,mol) !$, 1!$ atm !$ = 101325 !$ Pa !$, ln 2 !$ ln !$ 0,7.
Provas
Caderno Container