Foram encontradas 1.357 questões.
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
O hidróxido de sódio (NaOH) é uma substância fortemente alcalina e corrosiva, que deve ser manuseada com cuidado para evitar queimaduras na pele e danos aos olhos. Sabendo-se que a massa molecular do NaOH é de 40 g/mol.
A massa de Na(OH) presente em 50,0 cm3 de solução de Na(OH) 0,4 M é de
Provas
Sabe-se que a ligação covalente é o compartilhamento de elétrons entre átomos para formar moléculas, ocorrendo dentro de uma mesma molécula.
A ligação covalente que tem a maior polaridade é dada entre hidrogênio e o
Provas
As propriedades periódicas da tabela periódica são características dos elementos químicos que variam de maneira sistemática e previsível ao longo da tabela. Tais propriedades podem ser o raio atômico, a energia de ionização, a afinidade eletrônica, a eletronegatividade, a eletropositividade, a densidade e os pontos de fusão e ebulição.
É correto afirmar que
Provas
Após injetar a amostra realizando a técnica analítica de cromatografia em fase gasosa (CG) com detector de espectrômetro de massa (EM) do tipo aprisionamento de íons (íon trap) e ao final de 12 minutos da corrida cromatográfica, temos a figura do cromatograma a seguir
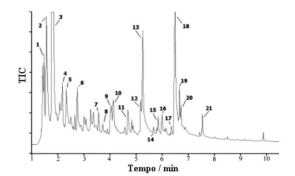
Com base na figura é correto afirmar que
Provas
Para extrair prata a partir de uma solução de nitrato de prata AgNO₃ (aq), utiliza-se uma reação de simples troca em que o zinco Zn (s), um metal mais reativo, substitui os íons de prata (Ag⁺) na solução. O zinco perde elétrons para formar íons de zinco (Zn²⁺), enquanto os íons de prata ganham esses elétrons e se transformam em prata metálica (Ag⁰), que se deposita na superfície do metal, formando cristais. Considere as massas molares (g/mol): Zn=65,4; Ag =108; O=16; N =14) e a reação química balanceada:
\( Z \)\( n \) (\( s \)) + 2\( A \)\( g \)\( N \)\( O \)3 (\( a \)\( q \)) → 2\( A \)\( g \)(\( s \)) + \( Z \)\( n \)(\( N \)\( O \)3)2(\( a \)\( q \))
Uma peça de zinco com massa de 2,0 g colocada em 10 mL de solução aquosa de 2M de Ag(NO3)2(aq) produzirá uma massa de prata de
Provas
Todos os anos, diversas pessoas utilizam o cloreto de cálcio (CaCl2) para derreter o gelo, pois atrai a umidade da superfície e do ar circundante, formando uma salmoura que derrete o gelo rapidamente, o que reduz o ponto de congelamento da água e acelera o processo de derretimento. Considerando a massa molecular do átomo de cloro (Cl) e cálcio (Ca), respectivamente, 35,5 g/mol e 40,1 g/mol.
A massa do cálcio necessária para preparar uma solução de cloreto de cálcio, tendo 41,5 gramas de Cloro é
Provas
Um laboratório realizando um teste para diabetes, analisa a concentração de glicose no sangue do paciente em função do tempo. Considerando que, t horas após uma injeção de glicose sua concentração no sangue é dada por \( f (t) = 1,8 + {\large 3,6 \over \sqrt t} \), que representa o número de miligramas (mg) de glicose por cm3 de sangue.
A concentração de glicose no sangue, 4 horas após a injeção
Provas
Estudos realizados para avaliar a velocidade de reação da luz de freio de acionamento rápido como dispositivo de prevenção de colisões, verificaram que o tempo de reação de uma resposta no trânsito a um sinal de frenagem com luzes de freio convencionais pode ser modelado com uma distribuição normal de média 1,25 segundo e desvio padrão de 0,46 segundo. Com o auxílio de alguns dados da área sob a curva normal padronizada
| Z | 0,00 | 0,01 | 0,02 | 0,03 | 0,04 | 0,05 | 0,06 | 0,07 | 0,08 | 0,09 |
|---|---|---|---|---|---|---|---|---|---|---|
| 0,0 | 0,5000 | 0,5040 | 0,5080 | 0,5120 | 0,5160 | 0,5199 | 0,5239 | 0,5279 | 0,5319 | 0,5359 |
| 1,0 | 0,8413 | 0,8438 | 0,8461 | 0,8485 | 0,8508 | 0,8531 | 0,8554 | 0,8577 | 0,8599 | 0,8621 |
| -0,5 | 0,3085 | 0,3050 | 0,3015 | 0,2981 | 0,2946 | 0,2912 | 0,2877 | 0,2843 | 0,2810 | 0,2776 |
A probabilidade de que o tempo de reação esteja entre 1,00 e 1,75 segundo é de
Provas
O composto sulfato de ferro (II) hidratado é utilizado na fabricação de produtos de borracha e como agente redutor em sistema de tratamento de água. Após fazer a análise química, foram encontrados: 20,2% de ferro; 11,5% de enxofre; 23,0% de oxigênio; e 45,3% de água de cristalização.
Dadas as massas molares (g/mol): Fe=56; S = 32; O=16; H2O =18, calcule a fórmula química desse composto, considerando sua massa molecular de 556 g.
Provas
Sabendo-se que o Enxofre (Z=16) e o Oxigênio (Z=16), ambos nãometais pertencentes à família dos calcogênios. Sabendo que o elemento Berílio (Z=4) é um metal alcalino-terroso, o Cloro (Z=17) é da família dos halogênios e o Hidrogênio (Z=1) é posicionado no início do Grupo 1, considere as geometrias moleculares a seguir:
I. Linear;
II. Trigonal Plana;
III. Angular;
IV. Piramidal;
É correto afirmar que SO3, H2S e BeCl2 apresentam, respectivamente, as geometrias moleculares
Provas
Caderno Container