Foram encontradas 1.633 questões.
Em um estudo, analisou-se o momento dipolar das seguintes moléculas: HF, CO2, NF3 e H2O. Dessas moléculas, aquela que apresenta momento dipolar nulo corresponde a:
Provas
Fosfina é a substância de fórmula molecular PH3. A geometria molecular da fosfina é nomeada por:
Provas
O efeito Tyndall pode ser usado para diferenciar uma solução coloidal de uma solução verdadeira. A luz que incidente sobre o sistema coloidal é espalhada pelas partículas em suspensão enquanto, na solução verdadeira, a luz não desvia de sua trajetória. Esse fenômeno visual deve-se:
Provas
Apresentam-se a seguir diagramas de fase de três compostos moleculares:
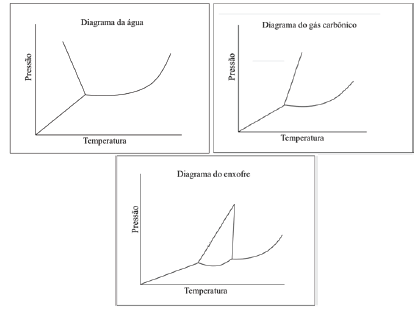
A água é um composto que apresenta um equilíbrio da fase líquido-sólido anômalo, conforme visto nos diagramas. Essa singularidade, em relação aos demais compostos, deve-se:
Provas
Uma solução aquosa de iodo apresentou o seguinte espectro no UV-vis, com as absorvâncias máximas de cada banda indicada sobre a curva:
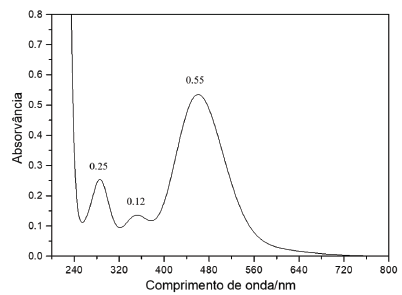
Esse espectro está relacionado com a seguinte tabela:
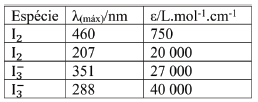
É sabido que uma solução aquosa de iodo apresenta equilíbrio químico com uma impureza de iodeto e forma o íon tri-iodeto, assim a pesagem direta não fornece informações suficientes para encontrar a concentração dessa espécie. Conhecendo as absortividades molares e a absorvância do experimento, a concentração de iodo é: (Dados: caminho óptico da cubeta = 1 cm)
Provas
Para planejar a destilação da mistura de um terço de tolueno com dois terços de benzeno, deseja-se construir um diagrama de temperaturacomposição e, para tal, é necessário conhecer a fração molar dos componentes. Considerando que o sistema foi mantido sob 25.°C a fração molar aproximada do tolueno e do benzeno são respectivamente: (Pvapor (tolueno) = 29,1 mm Hg; Pvapor (benzeno) = 94,5 mm Hg)
Provas
A cromatografia em camada delgada pode ser usada para separar os seguintes compostos:
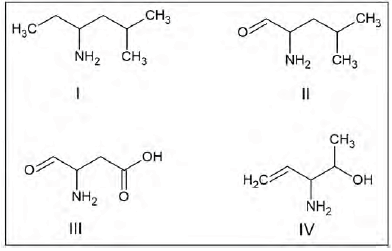
O tempo de retenção desses compostos com a fase estacionária está relacionado com as forças intermoleculares, ou seja, polaridades semelhantes serão fortemente atraídas. Sabendo que a fase estacionária está saturada de água, o composto retido por mais tempo é o:
Provas
Apresenta-se, a seguir, o ciclo de Born-Haber no cloreto de sódio e suas respectivas energias:
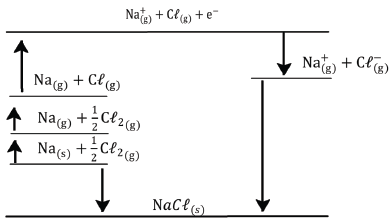
- energia de ionização do Na = + 496 kJ.mol– 1
- afinidade eletrônica do Cℓ = + 349 kJ.mol– 1
- entalpia de atomização Na = + 107 kJ.mol– 1
- entalpia de atomização Cℓ = + 122 kJ.mol-1
- entalpia padrão de formação do NaCℓ = – 411kJ.mol – 1
A entalpia de rede do cloreto de sódio é
Provas
Desde o séc. XVII, com os trabalhos de Robert Boyle, a via úmida dos laboratórios usa água régia para abertura de amostras. Recentemente, trabalhos acadêmicos buscam traduzir os experimentos originais de Boyle, o que permitiu a elaboração da seguinte equação química:
!$ Cu+HCl+HNO_3 \rightarrow [CuCl_4]^{2-} + NO + H_2O + H^+ !$
A soma dos menores coeficientes inteiros que balanceiam a equação é:
Provas
A partir da 2ª Lei da Termodinâmica o conceito de entropia foi criado, a fim de explicar a direção de um processo ou transformação. Sendo assim, a entropia total é uma medida de desordem que:
Provas
Caderno Container