Foram encontradas 60 questões.
Gás metano pode ser convertido em gás hidrogênio a partir do seguinte equilíbrio:
CH4(g) + H2O(g) \( \rightleftharpoons \) CO(g) + 3 H2(g); Kp, 500 ºC = 0,01 atm2
À temperatura de 500 ºC, para as pressões parciais de CH4(g) de 4 atm, H2O(g) de 4 atm e de H2(g) de 2 atm, em um sistema com volume de 100 L e considerando a constante geral dos gases R = 0,0831 atm.L.mol – 1.K – 1, a massa de CO(g) no equilíbrio é aproximadamente:
Provas
Considere a seguinte representação de uma pilha.
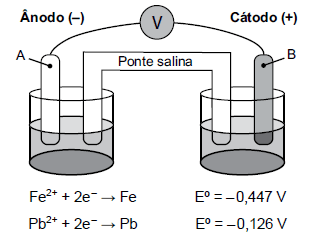
A partir dos potenciais padrões de eletrodo fornecidos, o diagrama de célula que representa a pilha e seu potencial são:
Provas
Algumas soluções, como a solução de KC\( \ell \) a 10% (m/v) e de NaC\( \ell \) a 0,9% (m/v), são utilizadas para reposição hidroeletrolítica. Sabendo que o sangue tem pressão osmótica 7,7 atm, a 25 ºC, e considerando R = 0,083 atm.L.mol – 1.K – 1, essas soluções, em relação ao sangue, a essa temperatura, são
Provas
Considere as configurações eletrônicas para os átomos a seguir.
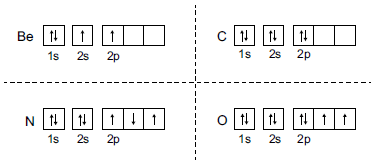
O elétron que apresenta os números quânticos \( m_{\ell} \) = – 1 e ms = – 1/2 está no átomo do elemento , no estado fundamental, e no átomo do elemento no estado excitado.
Assinale a alternativa que preenche, correta e respectivamente, as lacunas.
Provas
O sulfato de alumínio, A\( \ell \)2(SO4)3, é um sal que pode ser obtido por reação de neutralização do hidróxido de alumínio, A\( \ell \)(OH)3, com o ácido sulfúrico, H2SO4. Usando 50,0 mL de uma solução a 30% (v/v) de ácido sulfúrico, preparada a partir do ácido concentrado (98% em massa; d = 1,80 g.cm3), é possível obter a massa máxima, em gramas, de sulfato de alumínio, de
Provas
Analise o diagrama a seguir.
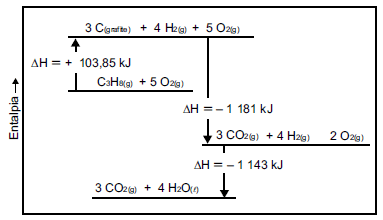
(AIO | Diagrama De Entalpia Segundo A Lei De Hess A Variacao. Adaptado)
A entalpia da reação C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O(\( \ell \)) é:
Provas
Para o preparo de uma solução, foi realizado o seguinte procedimento:
Em um tubo de polipropileno com capacidade volumétrica de 50 mL foram adicionados 0,10 g de uma amostra de uma certa substância que foi solubilizada em 20 mL de uma solução de HC\( \ell \) 1:1. Essa solução foi transferida para um balão volumétrico com capacidade de 25 mL e o volume foi completado com água destilada a 20 ºC, até o traço de aferição. Essa solução foi denominada solução I.
Foram transferidos, quantitativamente, 5,0 mL da solução I para um balão volumétrico de 50 mL,e o volume foi completado com água destilada a 20 ºC até o traço de aferição. Essa solução foi denominada solução II.
Posteriormente, foram transferidos, quantitativamente, 5,0 mL da solução II para um balão volumétrico de 100 mL, e o volume foi completado com água destilada a 20 ºC até o traço de aferição. Essa solução foi denominada solução III.
Ao final desse procedimento, o fator de diluição da solução I é igual a
Provas
Em um cilindro com capacidade volumétrica invariável de 10,0 L, estão confinados 10,0 mol de gás nitrogênio a 10 ºC. Sabendo que as constantes de van der Waals para esse gás são a = 1,39 L2.atm.mol – 2 e b = 0,0391 L.mol – 1, e a constante geral dos gases R = 0,0831 atm.L.K – 1.mol – 1, a pressão para esse gás, calculada pela equação do gás ideal, em comparação com aquela calculada pela equação de van der Waals é em, aproximadamente, .
\( (P + \dfrac{n^2 a}{V^2})(V - nb) = nRT \)
Assinale a alternativa que preenche, correta e respectivamente, as lacunas.
Provas
Analise o diagrama a seguir.
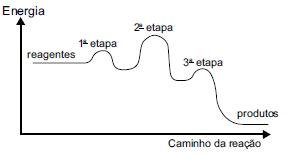
O diagrama está representando uma reação
Provas
Dentre as moléculas a seguir, aquela que se comporta como ácido de Lewis, em presença de água, é:
Provas
Caderno Container