Foram encontradas 100 questões.
As células voltaicas são baseadas nas reações de oxirredução espontâneas. Contrariamente, é possível usar a energia elétrica para fazer com que as reações redox não espontâneas ocorram. Tais processos, produzidos por uma fonte externa de energia elétrica, são chamados reações de eletrólise e ocorrem em células eletrolíticas. Por exemplo, a eletricidade pode ser usada para decompor o cloreto de sódio fundido em seus elementos componentes:
2 NaC\( \ell \) (\( \ell \)) → 2 Na (\( \ell \)) + C\( \ell \)2 (g)
Fonte: BROWN, T.L. et al. Química, a ciência central. 9. ed. São Paulo: Ed. Pearson, 2005, p.754.
O gás cloro produzido nessa reação é extremamente tóxico. Foi inclusive utilizado como agente químico de guerra em diversos conflitos. Considerando-se uma eletrólise ígnea de cloreto de sódio fundido durante 1 h 04 m 20 s (3860 s), sob uma corrente elétrica constante de 10 A, o volume de gás cloro formado nas CNTP será de, aproximadamente
Dados: volume molar gasoso nas Condições Normais de Temperatura e Pressão (CNTP) = 22,4 L mol-1 constante de Faraday: 1 F = 96500 C / mol de elétrons
Provas
Um material usado como componente de equipamentos de proteção balística é o polímero poliparafenileno de tereftalamida (aramida), cujo nome comercial é Kevlar®. A unidade polimérica é formada a partir de dois monômeros diferentes, conforme representado na figura abaixo.

Avalie as seguintes afirmativas acerca da reação, das estruturas e das propriedades dos monômeros e da unidade polimérica da aramida:
I – A estrutura da aramida apresenta somente ligações covalentes do tipo sigma (\( \sigma \)).
II – A unidade polimérica apresenta em sua estrutura o grupo funcional amida.
III – Os carbonos da estrutura do benzeno-1,4-diamina possuem hibridização do tipo sp3.
IV – A fórmula molecular do ácido benzeno-1,4-dioico é C8H6O4.
V – A aramida é obtida por meio de uma reação de polimerização por condensação.
Das afirmativas feitas, estão corretas apenas
Provas
Uma viatura da EsPCEx está equipada com pneus de uma determinada marca. Por recomendação do fabricante, deve-se observar a calibragem de segurança de rodagem dos pneus. A calibragem da pressão é indicada em psi (libras por polegada quadrada). Um pneu dessa viatura possui volume de 44,82 L, e foi abastecido com 140 g de nitrogênio (N2) gasoso. Considerando o nitrogênio como gás ideal e a temperatura de 25 ºC, a pressão desse pneu, em psi, será de aproximadamente
Dados: constante universal do gases = 0,082 L atm mol-1 K-1
relação de pressão: 1 atm = 14,696 psi
relação de temperatura: T Kelvin (K) = T Celsius (ºC) + 273
Provas
O Prêmio Nobel de Química de 2022 foi concedido pela Real Academia Sueca de Ciências aos pesquisadores Carolyn R. Bertozzi, Morten Meldal e K. Barry Sharpless, pelo desenvolvimento da “química do click” e da química bio-ortogonal. O termo “química do click” refere-se a reações rápidas e eficientes entre moléculas que ocorrem por meio de rotas relativamente simples. Meldal e Sharpless desenvolveram, simultânea e independentemente, a reação de cicloadição azida-alcino (representada na figura abaixo em 3 etapas sequenciais). Já Bertozzi aplicou a “química do click” no desenvolvimento de reações, em sistemas biológicos, que tivessem elevada seletividade e não prejudicassem a complexa estrutura dos organismos vivos – reações bio-ortogonais –, que vêm sendo utilizadas na produção de fármacos e no rastreamento de processos biológicos.
Fonte: www.nobelprize.org. Acessado em 1 MAR 23.
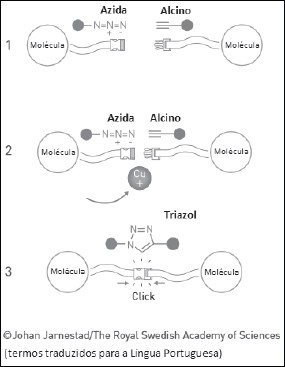
Com base nas estruturas representadas na figura, analise as seguintes afirmativas:
I – A união do grupo azida com os carbonos insaturados do alcino forma um anel benzênico.
II – Na reação representada, os carbonos insaturados do alcino sofrem alteração da geometria linear, no reagente, para a trigonal plana, no produto.
III – Os sinais + e - conferidos aos átomos de nitrogênio do grupo azida evidenciam uma ligação iônica.
IV – A reação envolve a quebra de uma ligação pi (\( \pi \)) e a formação de duas novas ligações sigma (\( \sigma \)).
V – A reação representada mostra a eliminação de uma molécula de amônia (NH3) como subproduto de reação.
Das afirmativas feitas, estão corretas apenas
Provas
Em uma aula no Laboratório de Química da EsPCEx, o professor solicitou aos alunos que identificassem a composição química de uma determinada substância pura, dentre uma lista de possibilidades, por meio da solubilidade em água. Para tanto, foram fornecidos 40 g de uma amostra pura da substância. Os resultados dos dois testes de solubilidade em água realizados pelos alunos, a 20 ºC, estão representados abaixo. Com base nos resultados obtidos e nos dados fornecidos a seguir, a alternativa que indica a correta composição química da substância é

| Lista de possibilidades: NaOH ; NaNO3 ; KNO3 ; K2SO4 ; Ca(OH)2. |
| Soluto (s) |
Solubilidade a 20 ºC |
| NaOH |
109,0 |
| NaNO3 |
87,4 |
| KNO3 |
31,6 |
| K2SO4 |
11,1 |
| Ca(OH)2 |
0,165 |
Provas
Exercícios físicos prolongados podem levar o organismo ao limiar anaeróbico: ponto limite de divisão entre o metabolismo aeróbico (com participação de oxigênio) e o metabolismo anaeróbico (sem participação de oxigênio). Quando o metabolismo anaeróbico entra em ação após certo tempo, pode ocorrer a formação de ácido lático. O ácido lático é capaz de formar, junto com o íon lactato, uma solução-tampão. Soluções-tampão são soluções que resistem à mudança no pH quando pequenas quantidades de ácidos ou bases são adicionados ou quando ocorre diluição. Essas soluções são, geralmente, formadas por uma mistura de um ácido fraco com o sal desse ácido, ou uma base fraca com o sal dessa base. Considere uma solução-tampão de ácido lático e lactato de sódio, em uma determinada condição experimental, na qual se estabelece o equilíbrio descrito na equação abaixo:
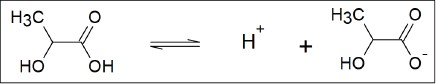
Dado: pKa do ácido = 4,0
Baseado nas informações acima, são apresentadas as seguintes afirmativas:
I - Segundo a União Internacional de Química Pura e Aplicada (IUPAC), a nomenclatura do ácido lático é ácido 2-hidroxipropanoico.
II - No equilíbrio, o pH de um tampão de 0,1 mol L-1 de ácido lático e 0,010 mol L-1 de lactato de sódio é de, aproximadamente, 1,6.
III - A adição de uma pequena quantidade de uma base forte deslocará o equilíbrio da reação no sentido da formação de mais ácido lático.
IV - O ácido lático apresenta dois isômeros opticamente ativos.
V - A adição de um ácido forte ao sistema causaria uma diminuição do valor do pKa.
Das afirmativas feitas, estão corretas apenas
Provas
Durante o curso de formação, um dos experimentos de investigação realizados pelos alunos da EsPCEx, utilizando o conceito de proteção por meio de ânodo de sacrifício, consiste em polir quatro pregos de ferro, envolver cada um deles com uma fita metálica de diferentes metais e mergulhá-los em uma solução aquosa de ferricianeto de potássio com oxigênio dissolvido. O ferricianeto de potássio é um sal que, em meio aquoso, atua como um indicador de corrosão do ferro, pois adquire coloração azul na presença de íons de ferro. O experimento está representado na imagem abaixo:
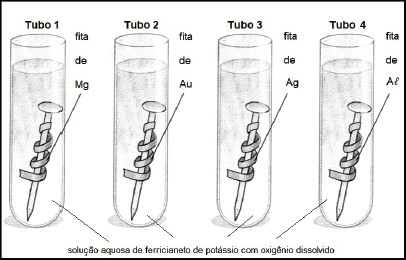
Adaptado de: USBERCO, João; SALVADOR, Edgard. Química. 12. ed. São Paulo: Editora Saraiva, 2009, v. 2, p. 296.
Dados:
| Potenciais padrão de redução |
E0 (T = 298,18 K) |
Potenciais padrão de redução |
E0 (T = 298,18 K) |
| Mg2+ (aq) + 2 e- → Mg (s) |
E0 = – 2,37 V |
A\( \ell \)3+(aq) + 3 e- → A\( \ell \) (s) | E0 = – 1,67 V |
| Au3+ (aq) + 3 e- → Au (s) |
E0 = + 1,50 V |
Fe2+ (aq) + 2 e- → Fe (s) |
E0 = – 0,44 V |
| Ag+ (aq) + 1 e- → Ag (s) |
E0 = + 0,80 V |
2H2O (l) + O2 (g) + 4 e- → 4 OH- (ag) |
E0 = + 0,40 V |
Considerando as informações apresentadas, após certo tempo, surgirá coloração azul apenas nos tubos
Provas
Algumas granadas incendiárias, como as do modelo AN-M14 TH3, possuem em sua composição alumínio metálico em pó e óxido de ferro III. Quando acionadas, elas produzem uma reação extremamente exotérmica, que pode atingir temperaturas da ordem de 3000 ºC. Por essa característica, são utilizadas para destruir ou inutilizar equipamentos. A reação aluminotérmica que ocorre na granada é representada pela seguinte equação química:
2 A\( \ell \) + Fe2O3 → A\( \ell \)2O3 + 2 Fe
Dados: \( \Delta \)Hºf Fe2O3 = – 823 kJ mol-1
\( \Delta \)Hºt A\( \ell \)2O3 = – 1671 kJ mol-1
Considerando-se a reação de 352 g de óxido de ferro III com 135 g de alumínio, sob condições-padrão, são feitas as seguintes afirmativas:
I – Nessas condições, o reagente limitante é o alumínio metálico.
II – O número de oxidação do alumínio passa de 0 (zero) para 3+.
III – O óxido formado como produto da reação possui os seus átomos ligados entre si por meio de ligações iônicas.
IV – A quantidade de calor liberado, considerando 100 % de rendimento na reação, é de aproximadamente 2450 kJ.
V – Nesta reação ocorre a oxidação do ferro.
Das afirmativas feitas, estão corretas apenas
Provas
- Química InorgânicaSubstância e mistura: substância simples, substância composta e mistura. Alotropia
A alternativa que apresenta corretamente os conceitos químicos sobre as características de substâncias simples e compostas e de elementos químicos é:
Provas
Considere a seguinte descrição de um experimento de laboratório:
Materiais e reagentes
- duas porções de zinco em pó com massa de 0,3 g cada uma
- uma placa de zinco laminado com 0,3 g
- solução de ácido clorídrico concentrado (12,0 mol L-1)
- solução de ácido clorídrico diluído (0,05 mol L-1)
- 3 copos de béquer identificados pelas letras A, B e C
- cronômetro
Procedimento
Coloque 30,0 mL da solução de ácido clorídrico concentrado nos copos de béquer A e B, e coloque 30,0 mL da solução de ácido clorídrico diluído no copo de béquer C. Em seguida, coloque simultaneamente a placa de zinco no copo de béquer A e uma porção de 0,3 g de zinco em pó no copo de béquer B. Meça o tempo decorrido até o consumo total do zinco em cada copo de béquer. Posteriormente, coloque uma porção de 0,3 g de zinco em pó no copo de béquer C. Meça o tempo decorrido até o consumo total do zinco nesse copo de béquer. Observe o que ocorre e anote os dados. Considerando-se que os sistemas estavam inicialmente em iguais condições e que foi observada a ocorrência de reação nos três experimentos realizados nos copos de béquer, são feitas as seguintes afirmativas acerca do experimento e das reações ocorridas:
I - Em todos os copos de béquer ocorreu a formação de clorato de zinco e gás carbônico como produtos de reação.
II - Devido à maior superfície de contato do reagente metálico em pó em relação à lâmina, a velocidade da reação observada no copo de béquer B será maior do que no copo de béquer A.
III - As reações ocorridas nos experimentos podem ser classificadas como reações de oxidorredução.
IV - Devido à maior concentração da solução ácida 12,0 mol L-1 em relação à solução 0,05 mol L-1, a velocidade da reação observada no copo de béquer B será menor do que no copo de béquer C.
V - Segundo a teoria de Br\( \varnothing \)nsted-Lowry, na reação entre o ácido clorídrico e a água, o íon cloreto é a base conjugada do ácido.
Das afirmativas feitas, estão corretas apenas
Provas
Caderno Container