Foram encontradas 460 questões.
O processo de cristalização pode ser utilizado como um processo de purificação ou de separação de substâncias. O método é realizado a partir da evaporação do solvente até que os componentes se cristalizem gradualmente. Sobre esse método, analise as proposições a seguir.
I. Cristalização fracionada é um método de purificação de substâncias baseado em diferenças de solubilidade.
II. Cristais formados de forma rápida tendem a ser puros, enquanto que cristais que se formam lentamente tendem a ser impuros.
III. Pode-se utilizar a cristalização para separar o sal (NaCl) da água do mar.
IV. No processo de cristalização fracionada, será cristalizada primeiro aquela substância que for mais solúvel.
V. Em uma solução contendo AgNO3 e CuNO3, após a adição de HCl, quem precipitará primeiro é o AgCl.
Dado: Kps(AgCl) = 1,6 x 10-10 e Kps(CuCl) = 1,0 x 10-6
Estão CORRETAS, apenas, as proposições
Provas
A análise de cátions é comumente realizada a partir da marcha analítica, que é uma sequência de adição de reagentes específicos, sendo esses denominados de reagentes de grupo, que têm por finalidade separar os cátions nos grupos analíticos a partir de reações de precipitação. Após a separação dos cátions, normalmente também é realizada a análise dos reagentes conforme ume série de procedimentos. Com base na separação de cátions dos grupos analíticos, responda à questão abaixo.
Quais os reagentes de grupo dos cátions dos grupos I, II, III, IV e V, na respectiva sequência?
Provas
A cromatografia é um método físico-químico de separação. Ela está fundamentada na migração diferencial dos componentes de uma mistura, que ocorre devido a diferentes interações, entre duas fases imiscíveis, a fase móvel e a fase estacionária. A grande variedade de combinações entre fases móveis e estacionárias a torna uma técnica extremamente versátil e de grande aplicação. O termo cromatografia foi primeiramente empregado em 1906 e sua utilização é atribuída a um botânico russo ao descrever suas experiências na separação dos componentes de extratos de folhas. Diversas são as técnicas de cromatografia, podendo variar a exemplo da cromatografia de papel, a cromatografia líquida de alta eficiência (CLAE; em inglês: High performance liquid chromatography - HPLC) e a cromatografia gasosa (CG).
DAGANI, A. L G. Cromatografia um breve ensaio. Revista Química Nova na Escola, no 7, maio de 1998, p. 21. (adaptado)
Com base nessa técnica de purificação, marque a alternativa CORRETA.
Provas
Ricardo, aluno do último ano do Curso Técnico em Química do IFPE, queria retirar a prata de uma solução de nitrato de prata entregue a ele por seu professor. Para isso, estudante procurou no laboratório algum reagente que lhe permitisse realizar a separação da prata na solução. Encontrou, então, 100 g de cloreto de magnésio, contendo 4,7 % de impureza. Qual será a máxima quantidade de prata que Ricardo conseguirá precipitar da solução aquosa do seu professor, utilizando o cloreto de magnésio encontrado? (dados de massas molares em g/mol: Mg = 24,3; Cl = 35,5; Ag = 107,9; N = 14; O = 16).
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A titulação é um dos métodos analíticos mais utilizados em laboratórios de química. Esse procedimento se baseia na adição do titulante ao titulado. O titulante, a depender do tipo de titulação realizada, pode ser uma base (com uma concentração bem definida), a qual, a partir do volume adicionado ao titulado, poderá ter seu ponto de equivalência identificado por uma mudança de cor da solução ocasionada por um indicador. Alberto realizou uma titulação com 50 mL de um titulado de HCl que apresentou o ponto de equivalência com a adição de 25 mL de uma titulante de NaOH 0,002 M. O potencial hidrogeniônico da solução titulada é
Provas
. A solubilização é a capacidade que uma substância tem de se dissolver em outra. Um conceito muito importante adotado no processo de solubilidade é o de “semelhante dissolve semelhante”. Diversos sais apresentam solubilidade em água, enquanto que outros não. A solubilização é um processo acompanhado de dois fenômenos, um de dissociação iônica e outro de solvatação. Consideremos um sal pouco solúvel de fórmula AB2 e constante de equilíbrio (Kps) igual a 4 x 10-6. Podemos afirmar que a concentração molar de íons B- no equilíbrio será
Provas
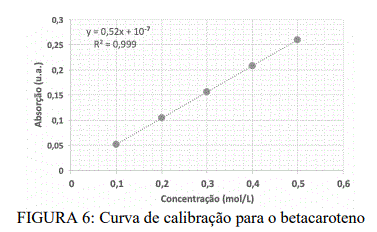
Provas
Os espectrômetros são equipamentos que nos permitem obter informações ópticas acerca da matéria. Para distinguirmos quais propriedades estamos querendo observar, devemos utilizar o equipamento adequado à necessidade. Sobre as representações esquemáticas dos equipamentos mostrados na FIGURA 5, podemos afirmar que
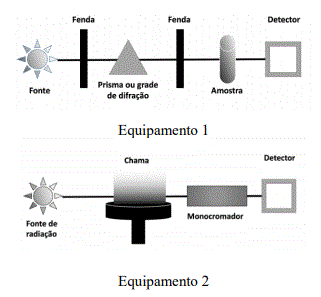
FIGURA 5: Esquemas de dois diferentes equipamentos para medidas ópticas.
Provas
Em um laboratório de química, é muito comum utilizar as balanças como instrumentos de medidas. Diferentes tipos de balanças podem ser utilizadas, a depender do tipo de medida a qual se deseja realizar. Algumas vezes é importante realizar apresentações de química ao público, como se faz, por exemplo, em atividades do tipo Show da Química. Nesses casos, faz-se necessária a utilização das balanças portáteis. Porém, em um laboratório, os tipos mais comuns de balanças encontradas são aquelas denominadas de analítica e semianalítica. Em um laboratório de química do IFPE, dois estudantes do Curso Médio Técnico Integrado de Química realizaram uma série de pesagem de uma mesma massa de glicose. O estudante 1 utilizou, para isso, uma balança semianalítica, e o estudante 2 utilizou uma balança analítica. Os dados das pesagens foram apresentados sob a forma de um gráfico, como mostrado na FIGURA 4.

Sobre a análise dos resultados e sabendo que o valor real da massa é igual a 1,0000 + 0,0001g, podemos afirmar que
Provas
Uma amostra contendo íons de Fe+2(aq) foi submetida a uma análise pelo método de titulação potenciométrica utilizando uma célula que consiste de um eletrodo de calomelano saturado e um eletrodo indicador de platina. A amostra líquida contendo íons de Fe+2(aq) foi preparada conforme protocolo de análise e diluída para 100 mL com água deionizada. Em seguida, uma alíquota de 20 mL foi retirada e foi submetida à titulação com solução de K2Cr2O7 0,0166 M. O GRÁFICO 3 representa a variação do potencial por unidade de titulante ( Δ E/V; mV/mL) em função do volume da solução de K2Cr2O7 adicionada
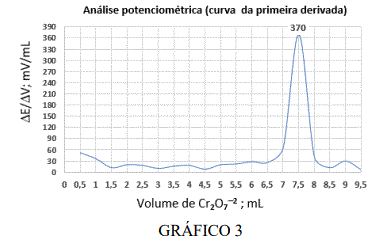
A equação iônica está representada a seguir:
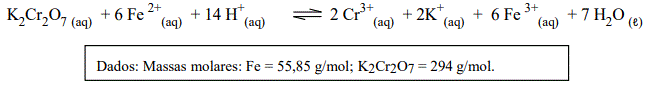
Assinale a alternativa que apresenta a massa do íon Fe+2(aq) presente na amostra inicial.
Provas
Caderno Container