Foram encontradas 200 questões.
- FundamentosPropriedades das Substâncias
- FundamentosTransformações: Estados Físicos e Fenômenos
- Transformações Químicas e EnergiaTermoquímica
A figura 1 apresenta a curva de aquecimento da água pura. Nela são mostradas as quantidades de energia fornecida para a ocorrência das mudanças de fases.
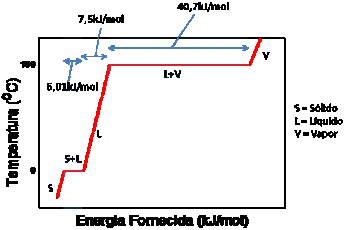
Figura 1 – Questão 12: Curva de aquecimento da água pura. (Adaptado). Fonte: Atkins, P. Jones, L. Chemistry, Molecules, Matter and Change. 4th ed. W. H. Freeman and Company. New York, 1999.
O mínimo de energia necessário para passar 1g de água do estado sólido para o estado vapor é: Dados: H= 1 g mol -1; O = 16 g mol -1

Figura 1 – Questão 12: Curva de aquecimento da água pura. (Adaptado). Fonte: Atkins, P. Jones, L. Chemistry, Molecules, Matter and Change. 4th ed. W. H. Freeman and Company. New York, 1999.
O mínimo de energia necessário para passar 1g de água do estado sólido para o estado vapor é: Dados: H= 1 g mol -1; O = 16 g mol -1
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um estudante necessita produzir gás hidrogênio a partir de raspas de zinco metálico. Há na bancada do laboratório dois reagentes líquidos concentrados:
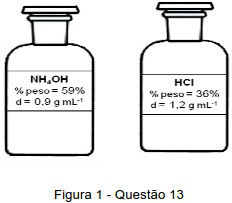
De acordo com as previsões do estudante, para produzir a quantidade de gás hidrogênio desejada ele deverá utilizar 500 mL de uma solução 6 mol L-1 preparada a partir de um dos reagentes acima. Indique a alternativa onde são apresentados, respectivamente, a identidade e o volume do reagente concentrado que o estudante deverá utilizar.
Dados: H = 1 g mol -1 ; N = 14 g mol -1 ; O = 16 g mol -1 ; Cl = 35,5 g mol -1 ; Zn = 65,4 g mol -1 .

De acordo com as previsões do estudante, para produzir a quantidade de gás hidrogênio desejada ele deverá utilizar 500 mL de uma solução 6 mol L-1 preparada a partir de um dos reagentes acima. Indique a alternativa onde são apresentados, respectivamente, a identidade e o volume do reagente concentrado que o estudante deverá utilizar.
Dados: H = 1 g mol -1 ; N = 14 g mol -1 ; O = 16 g mol -1 ; Cl = 35,5 g mol -1 ; Zn = 65,4 g mol -1 .
Provas
Questão presente nas seguintes provas
Num calorímetro misturam-se 50,0 g de uma solução HNO3 1mol.L-1 com 55,0 g de uma solução de KOH 1 mol .L-1 . A temperatura inicial de ambas as soluções era de 18º C. Após a reação de neutralização a temperatura medida foi 23o C. O calorímetro utilizado no experimento foi calibrado utilizando 60,0 g de água quente, a 57o C, adicionados a 60,0 g de água fria, a 12o C , que estavam presentes em um béquer dentro do calorímetro. Após a mistura mediu-se a temperatura e o valor encontrado foi de 32º C. Qual a entalpia da reação de neutralização em questão?
Dados:
Capacidade calorífica da água: 1 cal.g-1 . o C-1 .
Capacidade calorífica da solução neutralizada:1 cal.g-1 . o C-1 .
Densidade da água e de todas as soluções envolvidas: 1g.mL-1 .
Dados:
Capacidade calorífica da água: 1 cal.g-1 . o C-1 .
Capacidade calorífica da solução neutralizada:1 cal.g-1 . o C-1 .
Densidade da água e de todas as soluções envolvidas: 1g.mL-1 .
Provas
Questão presente nas seguintes provas
C
(grafite) + O2(g) → CO2(g) ∆H = -394 kJ mol-1 S
(rômbico) + O2(g) → SO2(g) ∆H = -297 kJ mol-1 CS
2(l) + 3 O2(g) → 2 SO2(g) + CO2(g) ∆H = - 1077kJ mol-1
A entalpia de formação do CS 2(l) a partir de seus elementos formadores tem ΔH = _____________ sendo, portanto uma reação _______________. Assinale a alternativa que contém os complementos corretos para a frase acima, respectivamente.
A entalpia de formação do CS 2(l) a partir de seus elementos formadores tem ΔH = _____________ sendo, portanto uma reação _______________. Assinale a alternativa que contém os complementos corretos para a frase acima, respectivamente.
Provas
Questão presente nas seguintes provas
A decomposição do N2O5 é uma reação de primeira ordem.
N2O5 (g) → 2 NO2(g) + 1/2 O2(g)
A constante de velocidade desta reação é igual a 1,38 x 10-5 s-1 a uma dada temperatura. Se a concentração inicial do N2O5 for 4,0 x 10-3 mol L-1,em quanto tempo aproximadamente a concentração cai até 1,0 x 10-3 mol L-1 ?
Dados: ln 2,5 = 0,916; ln 10-1 = -2,302
N2O5 (g) → 2 NO2(g) + 1/2 O2(g)
A constante de velocidade desta reação é igual a 1,38 x 10-5 s-1 a uma dada temperatura. Se a concentração inicial do N2O5 for 4,0 x 10-3 mol L-1,em quanto tempo aproximadamente a concentração cai até 1,0 x 10-3 mol L-1 ?
Dados: ln 2,5 = 0,916; ln 10-1 = -2,302
Provas
Questão presente nas seguintes provas
- Interações com Tecnologia, Sociedade e Meio Ambiente
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
O etilenoglicol CH2(OH)CH2(OH) é uma substância bastante utilizada como anticongelante. Pergunta-se: qual o volume mínimo de etilenoglicol que deve ser adicionado a 6,5L de água presentes no radiador de um carro, para prevenir o congelamento da água, num dia de inverno em que a temperatura atinge -20º C?
Dados: Densidade do etilenoglicol: 1,1 g cm-3 .
Densidade da água: 1,0 g cm-3
Kf = 1,9 K mol -1 Kg
H = 1 g mol -1 ; O = 16 g mol -1 ; C = 12 g mol -1
Dados: Densidade do etilenoglicol: 1,1 g cm-3 .
Densidade da água: 1,0 g cm-3
Kf = 1,9 K mol -1 Kg
H = 1 g mol -1 ; O = 16 g mol -1 ; C = 12 g mol -1
Provas
Questão presente nas seguintes provas
Fósforo branco, que possui fórmula molecular P4, queima na presença do ar atmosférico para dar o composto A, no qual a porcentagem em massa de oxigênio é de 56,4%. O espectro de massa fornece a massa de A igual a 284 g mol -1 . Assinale a alternativa que contém a correta fórmula molecular de A. Dados: P = 31 g mol -1 ; O = 16 g mol -1 .
Provas
Questão presente nas seguintes provas
O tálio é um metal macio e maleável; quando imediatamente cortado por uma espátula, apresenta brilho metálico característico dos metais. O tálio, massa atômica 204,4 u, apresenta como isótopos mais estáveis o Tl-203 e o Tl-205. O isótopo Tl-205 apresenta abundância isotópica, em percentual inteiro, mais próximo de
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- FundamentosSubstâncias, Misturas e Processos de Separação
- FundamentosTransformações: Estados Físicos e Fenômenos
O níquel metálico cristaliza numa estrutura do tipo cúbica de faces centradas (cfc). Na figura são mostradas duas representações para célula unitária cfc: (a) utilizando esferas rígidas e (b) utilizando esferas reduzidas.
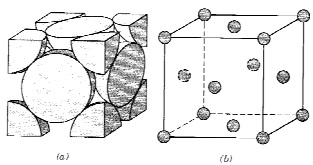 Fonte: CALLISTER, W.D. Ciência de Engenharia de Materiais: uma Introdução, 5ª edição, Rio de Janeiro: LTC,
Fonte: CALLISTER, W.D. Ciência de Engenharia de Materiais: uma Introdução, 5ª edição, Rio de Janeiro: LTC,
O número de coordenação do níquel e o número de átomos de níquel por célula unitária são, respectivamente,
 Fonte: CALLISTER, W.D. Ciência de Engenharia de Materiais: uma Introdução, 5ª edição, Rio de Janeiro: LTC,
Fonte: CALLISTER, W.D. Ciência de Engenharia de Materiais: uma Introdução, 5ª edição, Rio de Janeiro: LTC, O número de coordenação do níquel e o número de átomos de níquel por célula unitária são, respectivamente,
Provas
Questão presente nas seguintes provas
O permanganato de potássio é bastante utilizado em titulações redox em análise química quantitativa, por se tratar de um forte reagente oxidante. Na equação, não balanceada, é representada a reação de uma das aplicações analíticas das titulações do permanganato.
MnO4 - + H2C2O4 + H+ → Mn2+ + CO2 + H2O
Após o correto balanceamento da reação redox descrita, a soma dos coeficientes estequiométricos na equação será igual a
MnO4 - + H2C2O4 + H+ → Mn2+ + CO2 + H2O
Após o correto balanceamento da reação redox descrita, a soma dos coeficientes estequiométricos na equação será igual a
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container