Foram encontradas 200 questões.
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
- Química InorgânicaSoluções e Substâncias Inorgânicas
Considere os íons indicados na tabela.
íons identificação nitrito I nitrato II sulfito III sulfato IV
O íon em que o átomo central apresenta conjunto de orbitais híbridos sp2 e o íon que apresenta geometria pirâmide trigonal são identificados na tabela, respectivamente, com os números
íons identificação nitrito I nitrato II sulfito III sulfato IV
O íon em que o átomo central apresenta conjunto de orbitais híbridos sp2 e o íon que apresenta geometria pirâmide trigonal são identificados na tabela, respectivamente, com os números
Provas
Questão presente nas seguintes provas
Considere o diagrama de Frost para o manganês em solução ácida com pH = 0.
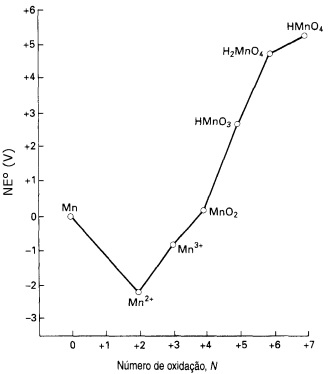
Fonte: SHRIVER, D. F.; ATKINS, P.W, C.H. Química Inorgânica, 3ª edição, Porto Alegre:
A partir da análise do diagrama, pode-se afirmar que a espécie de manganês que se apresenta com o estado de oxidação mais estável em meio ácido, e uma das espécies de manganês que sofre desproporcionamento espontaneamente são, respectivamente,

Fonte: SHRIVER, D. F.; ATKINS, P.W, C.H. Química Inorgânica, 3ª edição, Porto Alegre:
A partir da análise do diagrama, pode-se afirmar que a espécie de manganês que se apresenta com o estado de oxidação mais estável em meio ácido, e uma das espécies de manganês que sofre desproporcionamento espontaneamente são, respectivamente,
Provas
Questão presente nas seguintes provas
No efeito fotoelétrico, quando um feixe de luz atinge uma superfície metálica provoca a emissão de elétrons. Para cada metal há uma frequência mínima da luz abaixo da qual não ocorre emissão de elétrons. Para explicar o efeito fotoelétrico _____________ admitiu que a energia radiante que atingia a superfície metálica era constituída por minúsculos pacotes de energia, chamados atualmente de fótons. No texto a lacuna pode ser corretamente substituída por:
Provas
Questão presente nas seguintes provas
Para abordar o tema equilíbrio químico, um professor nas aulas de química analítica apresentou dois sistemas em equilíbrio químico para discussão do princípio de Le Châtelier. O sistema A, em solução aquosa, refere-se ao equilíbrio dos íons dicromato (laranja) e cromato (amarelo). O sistema B, em fase gasosa, envolve os gases NO2 (castanho) e N2O4 (incolor).
sistema A: Cr2O7 2- (aq) + H2O (l) ⇄2 CrO42-(aq) + 2 H+ (aq)
sistema B: 2 NO2 (g) ⇄ N2O4 (g) ΔHº = -58 kJ
Cada sistema em equilíbrio foi submetido, separadamente, a duas perturbações, descritas a seguir:
I – Foram adicionadas gotas de solução de NaOH no sistema A.
II – Foram adicionadas gotas de solução de HCl no sistema A.
III – Foi aumentada a pressão do sistema B por meio de redução de volume.
IV – O sistema B foi aquecido.
Pode-se afirmar que as cores predominantes dos sistemas A e B após as perturbações I, II, III e V, foram, respectivamente,
sistema A: Cr2O7 2- (aq) + H2O (l) ⇄2 CrO42-(aq) + 2 H+ (aq)
sistema B: 2 NO2 (g) ⇄ N2O4 (g) ΔHº = -58 kJ
Cada sistema em equilíbrio foi submetido, separadamente, a duas perturbações, descritas a seguir:
I – Foram adicionadas gotas de solução de NaOH no sistema A.
II – Foram adicionadas gotas de solução de HCl no sistema A.
III – Foi aumentada a pressão do sistema B por meio de redução de volume.
IV – O sistema B foi aquecido.
Pode-se afirmar que as cores predominantes dos sistemas A e B após as perturbações I, II, III e V, foram, respectivamente,
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Na análise gravimétrica, diversas etapas sucessivas, ou operações unitárias, são empregadas durante a análise, tais como preparo da solução, precipitação, digestão, filtração, lavagem, calcinação e pesagem. Na etapa de preparo de soluções, para abertura de três diferentes amostras: calcário, paládio e materiais silicosos, recomenda-se o uso, respectivamente, de
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
A análise volumétrica é muito utilizada nos laboratórios químicos, especialmente na padronização de soluções. Na figura é representada uma curva de titulação.
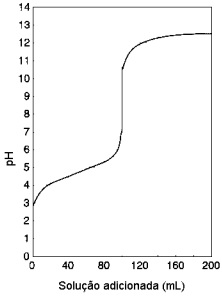
Considerando as soluções 0,1 mol/L de ácido acético, de ácido clorídrico, de hidróxido de sódio e de amônia, pode-se afirmar que a curva refere-se à adição da solução de

Considerando as soluções 0,1 mol/L de ácido acético, de ácido clorídrico, de hidróxido de sódio e de amônia, pode-se afirmar que a curva refere-se à adição da solução de
Provas
Questão presente nas seguintes provas
No tratamento e diagnóstico de tumores na glândula tireoide, o radionuclídeo 131I é frequentemente utilizado. Para certa amostra deste radionuclídeo, o gráfico apresenta sua atividade ao longo do tempo, bem como a atividade presente na amostra em diferentes números de dias após sua preparação. 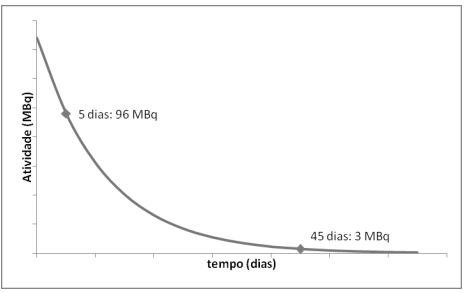
A partir do gráfico, pode-se concluir que a meia-vida do 131 I é, em dias, aproximadamente:

A partir do gráfico, pode-se concluir que a meia-vida do 131 I é, em dias, aproximadamente:
Provas
Questão presente nas seguintes provas
Considere as seguintes reações orgânicas:
I - tolueno com ácidos nítrico e sulfúrico
II - ácido benzoico com ácidos nítrico e sulfúrico
s principais produtos orgânicos obtidos nas reações I e II são, respectivamente,
I - tolueno com ácidos nítrico e sulfúrico
II - ácido benzoico com ácidos nítrico e sulfúrico
s principais produtos orgânicos obtidos nas reações I e II são, respectivamente,
Provas
Questão presente nas seguintes provas
- Química CinéticaTransformações Químicas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
A análise qualitativa é empregada na identificação das espécies presentes em uma amostra. Quanto aos fundamentes da química analítica qualitativa, assinale a alternativa correta.
Provas
Questão presente nas seguintes provas
Os alcoóis: (I) butílico, (II) sec-butílico e (III) isobutílico apresentam propriedades físicas diferentes. Dentre esses alcoóis, aquele que apresenta maior temperatura de ebulição e aquele que apresenta maior solubilidade em água, medidas nas mesmas condições experimentais são, respectivamente, os alcoóis:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container