Foram encontradas 200 questões.
Uma amostra de 0,486g de magnésio metálico é adicionada a 500mL de uma solução de ácido clorídrico cujo pH é 1. Qual o pH da solução resultante após todo magnésio ser consumido? Considere que não há variação no volume total da solução.
Dados: Mg = 24,3 g mol -1 ; H = 1,0 g mol -1 ;Cl = 35,5 g mol -1 ; log 2=0,30.
Dados: Mg = 24,3 g mol -1 ; H = 1,0 g mol -1 ;Cl = 35,5 g mol -1 ; log 2=0,30.
Provas
Questão presente nas seguintes provas
- Interações com Tecnologia, Sociedade e Meio Ambiente
- Química CinéticaTransformações Químicas
- Química InorgânicaSoluções e Substâncias Inorgânicas
A chuva ácida é formada ao atravessar uma atmosfera poluída por óxidos. A precipitação é formada por ácido sulfúrico e ácido nítrico. Quais são esses óxidos?
Provas
Questão presente nas seguintes provas
- Gases
- Química CinéticaTransformações Químicas
- Sistemas de EquilíbrioSistemas Homogêneos: Constantes: Kc e Kp. Deslocamento do Equilíbrio: Fatores
Em fase gasosa o PCl5 (pentacloreto de fósforo) está em equilíbrio com o PCl3 (tricloreto de fósforo) e Cl2(cloro gasoso):
PCl5(g) ⇌ PCl 3(g)+ Cl 2(g)
A 250ºC a referida reação apresenta Kρ = 1,8. Para que a reação apresente um fator de conversão em PCl3 e Cl2 de 30%, qual a pressão aproximada que deve ser aplicada ao sistema?
PCl5(g) ⇌ PCl 3(g)+ Cl 2(g)
A 250ºC a referida reação apresenta Kρ = 1,8. Para que a reação apresente um fator de conversão em PCl3 e Cl2 de 30%, qual a pressão aproximada que deve ser aplicada ao sistema?
Provas
Questão presente nas seguintes provas
Uma célula eletroquímica é definida pelo seguinte arranjo:
Ag | AgBr(s)| Br – (c=0,10) || Cl – (c=0,01) | AgCl(s)| Ag
Qual o potencial fornecido pela célula representada acima?
Dados:
AgBr(s) + 1e- → Ag(s)+ Br – E0 = +0,0713V
AgCl(s) + 1e- → Ag(s)+ Cl – E0 = +0,22V
a 25º C: 2,303 RT/F = 59mV
Ag | AgBr(s)| Br – (c=0,10) || Cl – (c=0,01) | AgCl(s)| Ag
Qual o potencial fornecido pela célula representada acima?
Dados:
AgBr(s) + 1e- → Ag(s)+ Br – E0 = +0,0713V
AgCl(s) + 1e- → Ag(s)+ Cl – E0 = +0,22V
a 25º C: 2,303 RT/F = 59mV
Provas
Questão presente nas seguintes provas
O poliestireno é um polímero termoplástico com ampla utilização na fabricação de embalagens, recipientes descartáveis para alimentos, etc. Uma amostra de poliestireno tem massa molecular média de 52000 u. Qual o grau de polimerização desta amostra? Dados: C = 12u; H = 1u.
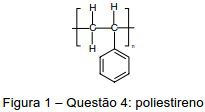

Provas
Questão presente nas seguintes provas
O smog fotoquímico é um problema ambiental resultante das diversas reações entre poluentes induzidas pela luz. Os reagentes originais mais importantes nas ocorrências de smog fotoquímico são os derivados do óxido nítrico (NOx) e os compostos orgânicos voláteis (COVs). A figura abaixo mostra a relação existente entre a presença desses dois poluentes e a produção de ozônio através do smog fotoquímico.
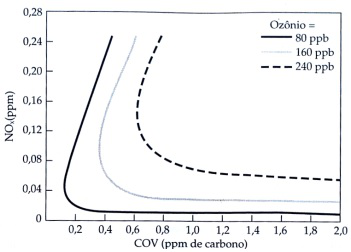
Figura 1 – Questão 5: Relação entre as concentrações de NOx e COV no ar e a concentração resultante de ozônio produzido por sua reação. (Adaptado). Fonte: BAIRD, C. Química Ambiental, 2ª ed. Porto Alegre: Bookman, 2002. p.116.
A partir do conhecimento envolvido no fenômeno do smog fotoquímico e de acordo com os dados apresentados na figura acima, pode-se afirmar que:

Figura 1 – Questão 5: Relação entre as concentrações de NOx e COV no ar e a concentração resultante de ozônio produzido por sua reação. (Adaptado). Fonte: BAIRD, C. Química Ambiental, 2ª ed. Porto Alegre: Bookman, 2002. p.116.
A partir do conhecimento envolvido no fenômeno do smog fotoquímico e de acordo com os dados apresentados na figura acima, pode-se afirmar que:
Provas
Questão presente nas seguintes provas
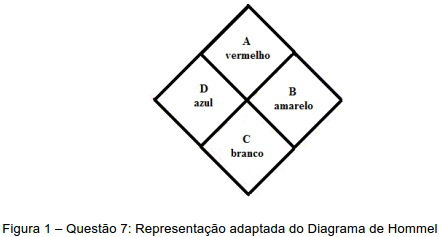
As letras A, B, C, e D presentes na representação do diagrama de Hommel (figura 1) estão associadas aos seguintes riscos, respectivamente:
Provas
Questão presente nas seguintes provas
Um programa de gerenciamento de resíduos deve contemplar dois tipos de resíduos: o ativo (gerado continuamente fruto das atividades rotineiras dentro da unidade geradora), e o passivo, que compreende todo aquele resíduo estocado. Em uma determinada Instituição de Ensino foram analisadas três diferentes amostras de resíduos sem identificação. A tabela abaixo apresenta os resultados encontrados em cada um dos testes:
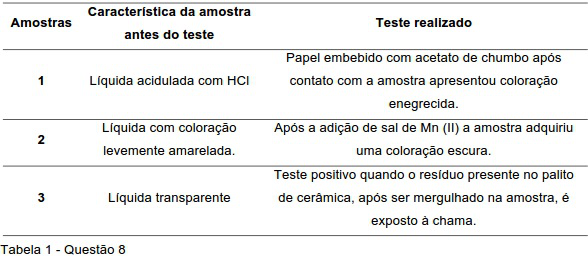
Com bases nos resultados dos testes, as amostras podem ser caracterizadas como:

Com bases nos resultados dos testes, as amostras podem ser caracterizadas como:
Provas
Questão presente nas seguintes provas
A análise coulométrica é uma aplicação da primeira lei de Faraday que pode ser expressa da seguinte forma: a extensão da reação química num eletrodo é diretamente proporcional à quantidade de eletricidade que passa através do eletrodo. Numa célula eletroquímica apropriada foi realizada a seguinte reação:
I3- + 2e- ⇌ 3 I -
Considerando as informações fornecidas acima, qual a quantidade de matéria de I3 - consumida após a passagem de 0,193 A durante 500 s ?
Dado: Constante de Faraday = 96500 C mol -1
I3- + 2e- ⇌ 3 I -
Considerando as informações fornecidas acima, qual a quantidade de matéria de I3 - consumida após a passagem de 0,193 A durante 500 s ?
Dado: Constante de Faraday = 96500 C mol -1
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A figura 1 apresenta a variação da pressão de vapor de quatro diferentes substâncias puras.
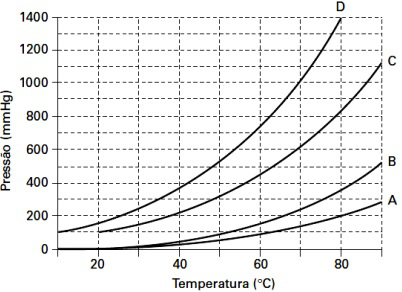
Figura 1 – Questão 11: Variação da pressão de vapor em função da temperatura para quatro diferentes substâncias puras.
Substância Massa Molar g mol-1 CHCl3 (Clorofórmio) 119,5
H2O (água) 18 CH3CH2OH (etanol) 46 CH2(OH)COOH (ácido glicólico) 76
As curvas apresentadas no gráfico foram obtidas em experimentos utilizando as substâncias listadas na Tabela 1. Identifique a alternativa que associa corretamente as curvas do gráfico às suas respectivas substâncias.
As curvas apresentadas no gráfico foram obtidas em experimentos utilizando as substâncias listadas na Tabela 1. Identifique a alternativa que associa corretamente as curvas do gráfico às suas respectivas substâncias.

Figura 1 – Questão 11: Variação da pressão de vapor em função da temperatura para quatro diferentes substâncias puras.
Substância Massa Molar g mol-1 CHCl3 (Clorofórmio) 119,5
H2O (água) 18 CH3CH2OH (etanol) 46 CH2(OH)COOH (ácido glicólico) 76
As curvas apresentadas no gráfico foram obtidas em experimentos utilizando as substâncias listadas na Tabela 1. Identifique a alternativa que associa corretamente as curvas do gráfico às suas respectivas substâncias.
As curvas apresentadas no gráfico foram obtidas em experimentos utilizando as substâncias listadas na Tabela 1. Identifique a alternativa que associa corretamente as curvas do gráfico às suas respectivas substâncias.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container