Foram encontradas 80 questões.
Em 1911, dois alunos do Prof. Ernest Rutherford realizaram o seguinte experimento para testar o modelo atômico de Thomson: bombardearam uma lâmina de ouro com um feixe de radiação alfa, como mostra a Figura 1.
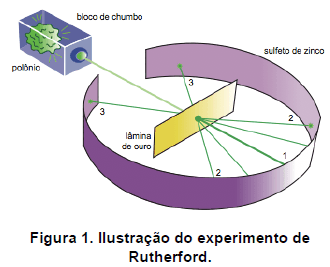
Apenas uma a cada 20 mil partículas alfa (núcleos de hélio) era ricocheteada com ângulos maiores de 90 graus. Nesse experimento, foi utilizada uma lâmina de ouro que é um metal representado por !$ ^{197}_{79} Au !$ . Porém, Rutherford usou também lâminas de outros metais como platina !$ (^{195}_{78} Pt) !$ e alumínio !$ (^{27}_{13} Al) !$. A lâmina de platina apresentou o mesmo resultado observado para a lâmina de ouro. No entanto, não foi possível observar tal fenômeno de deflexão usando uma lâmina de alumínio. Isso se deve ao fato de que:
Provas
Soluções aquosas dos seguintes sais foram preparadas separadamente: Fe2(SO4)3, NaF, Ca(CH3CO2)2 e NH4Cl. O pH de cada solução será, respectivamente:
Provas
Um gás pode apresentar dois comportamentos dependendo das condições de temperatura e pressão, ou seja, ele pode se comportar como um gás ideal ou como um gás real. Esses comportamentos estão relacionados a diferentes modelos utilizados para explicar observações experimentais, e são importantes na indústria para estimar corretamente a pressão que um gás irá exercer dentro do reator. Suponha, como exemplo, o uso de 1500 mols de gás nitrogênio (N2) a 800 K na produção da amônia pelo processo Haber-Bosch. O reator apresenta um volume de 600 L, e suporta uma pressão de até 175 atm. Adotando o modelo do gás real, a pressão exercida no reator pelo gás será de aproximadamente 173 atm. Se o modelo do gás ideal fosse adotado, a pressão exercida seria maior ou menor e com qual diferença numérica em relação à pressão real?
(Dado: R = 0,082 atm.L.mol-1.K-1)
Provas
Os íons Mn2+ reagem em meio aquoso ácido com os íons BiO3− formando íons permanganato, íons Bi3+ e água. A soma dos menores valores inteiros dos coeficientes estequiométricos da equação corretamente balanceada dessa reação é:
Provas
O biodiesel pode ser obtido por reação de transesterificação de óleos vegetais ou de gordura animal (trialcilglicerol). Esta reação se processa com o aquecimento do trialcilglicerol e um álcool de cadeia curta, empregando-se um ácido forte como catalisador. Forma-se como produtos o éster, que é o biodiesel, e um triálcool, o glicerol. Cuidados são tomados para que a reação se processe na ausência de água para evitar a hidrólise do biodiesel no meio reacional.
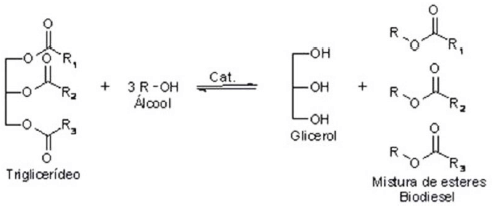
Considerando-se a síntese do biodiesel a partir do óleo de coco (R1 = R2 = R3 = C11H23) com metanol, a reação indesejada de hidrólise do biodiesel geraria com um dos produtos um composto com fórmula molecular
Provas
Atendendo às regras de segurança no laboratório químico, todos os frascos devem possuir rótulos que indiquem claramente seu conteúdo. Uma forma de representar os perigos associados ao conteúdo do frasco é a inclusão no rótulo do diamante de Hommel.
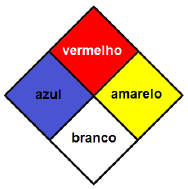
Risco para a saúde, perigo de incêndio e perigo de instabilidade são classificados em uma escala que abrange valores de 0 (mínimo) a 4 (máximo) e são correta e respectivamente representados no Diamante de Hommel nos campos de cores:
Provas
Um estudo cinético da reação de síntese do composto Z foi feito a partir da reação dos compostos X e T.
X(g) + T (g) → Z(g)
Três experimentos, I, II e III, de medida de velocidade de reação foram feitos em condições de temperatura e pressão controladas e constantes. Os resultados são expressos na tabela a seguir.
|
Experimento |
[X] mol.L-1 | [T] mol.L-1 |
Velocidade de formação de Z mol.L-1s-1. |
| I | x | t | v |
| II | x | 3t | v |
| III | 9x | t | 3v |
Com base nos resultados dos experimentos é possível concluir corretamente que os valores de ordem de reação para consumo das substâncias X e T são, respectivamente:
Provas
Um composto orgânico formado apenas por carbono, hidrogênio e oxigênio foi analisado por combustão. Uma amostra de 90 mg desse composto foi queimada adequadamente em um equipamento apropriado e como resultado da combustão completa formaram-se 176 mg de CO2 e 90 mg de H2O. A fórmula mínima do composto orgânico analisado é corretamente representada por
Provas
As ligações químicas nos compostos !$ C \ell F_3 !$ e !$ IF_5 !$ são corretamente representadas empregando-se para os átomos centrais dessas moléculas, respectivamente, os conjuntos de orbitais híbridos
Provas
Considere a teoria cinético-molecular dos gases para analisar as informações a seguir:
I – Os gases são constituídos por moléculas ou átomos que estão em movimento constante e aleatório.
II – Quando as moléculas de um gás colidem entre si, não há perda energia individual.
III – Há uma relação entre a energia cinética média das moléculas do gás e a temperatura absoluta.
IV – A colisão entre as moléculas de um gás dentro de um recipiente isolado não causa alteração na energia total.
São corretas somente as afirmações:
Provas
Caderno Container