Foram encontradas 50 questões.
Em novembro de 1952 a cidade de Londres enfrentou uma grande frente fria, fazendo com que as pessoas utilizassem mais carvão que o habitual para manterem-se aquecidas. Devido às dificuldades econômicas enfrentadas no pós-guerra, o carvão de melhor qualidade foi exportado, levando os londrinos a usarem carvão de baixa qualidade, rico em enxofre, para aquecerem-se. Como resultado, formou-se um nevoeiro muito denso chamado de smog, termo cunhado a partir das palavras fog - névoa e smoke - fumaça, que chegou a impedir o trânsito de automóveis nas ruas, e causar a morte de mais de 4000 pessoas.
Fonte: O mistério do nevoeiro mortífero de Londres foi resolvido. Matou 4 mil pessoas. Disponível em: https://observador.pt/2016/11/17/0-misterio-do-nevoeiro-mortifero-de-londres-foi-resolvido/>. Acesso em: 02 jun. 2019.
Considerando que a queima de enxofre leve à formação exclusivamente de trióxido de enxofre e que o carvão contém 1,62% de enxofre, responda:
Qual a massa de óxido produzida a partir da queima de 10 toneladas de carvão?
Provas
Um professor procurou o técnico de seu campus a fim de ajudá-lo a preparar uma aula prática para o Ensino Médio sobre as propriedades dos materiais. José pretende escolher objetos que possam demonstrar, simultaneamente, as características de maleabilidade, ductilidade, e condutividade térmica. Dessa forma, o conjunto que melhor representa essas propriedades seria:
Provas
O metano é um gás incolor, sua molécula é tetraédrica e apolar, de pouca solubilidade na água e, quando adicionado ao ar se transforma em mistura de alto teor inflamável. As entalpias molares do CH4(g), O2(g), H2O(l) e CO2(g) valem, respectivamente: - 1650kJ/mol, - 497kJ/mol e -924kJ/mol, e -1604kJ/mol dessa forma o módulo do calor liberado na combustão de 1 mol de metano é:
Provas
O terpineol é um álcool do tipo monoterpeno que podem existir na forma de três isômeros, alfa, beta, e gama-terpineol, os últimos dois diferindo somente pela localização da ligação dupla. O terpineol é geralmente obtido por uma mistura destes três isômeros, sendo o alfa-terpineol como o principal constituinte, como mostrado na figura a seguir:
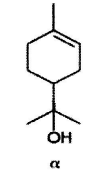
Dessa forma, a formula molecular do a terpineol é:
Provas
A análise do teor de ácido acético (CH3COOH) no vinagre comercial seguiu o seguinte procedimento: 20,0 mL de uma amostra de vinagre foi transferida para um balão volumétrico de 100,0 mL e o volume completado com água destilada. Após a homogeneização, retirou-se uma alíquota de 10,0 mL e titulou-se com uma solução padronizada de NaOH 0,2 mol/L. Na titulação foram consumidos 15,0 mL de NaOH. Assinale a alternativa que contenha o título (m/v) em porcentagem de ácido acético na amostra de vinagre.
Dados: massa molar do CH3COOH = 60,0 g/mol
Provas
Alguns elementos químicos apresentam-se na forma de isótopos, que são átomos de mesmo número atômico que apresentam massas diferentes. As massas atômicas e a abundância dos isótopos podem ser determinadas por espectrometria de massas. À figura abaixo corresponde ao espectro de massas da molécula de cloro, Cl2. No eixo das abcissas encontra-se a relação entre a massa e a carga do íon, sendo que os íons gerados possuem carga igual a 1. No eixo das ordenadas, a intensidade corresponde a quantidade de íons que foram produzidos com determinada relação entre a massa e a carga. Essa figura apresenta dois conjuntos de sinais. O conjunto de maior massa apresenta 3 sinais e correspondem a massa da molécula Cl2, chamados de íon molecular. O conjunto de menor massa é composto de dois sinais, que correspondem à massa dos dois isótopos do cloro.
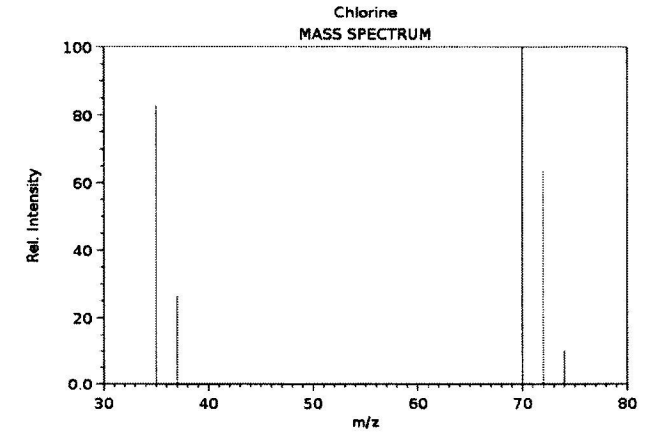
Fonte: National Institute of Standards and Technology. Disponível em: <https://webbook.nist.gov/chemistry>. Acesso em: 06 jun. 2019.
A respeito do espectro de massas da molécula de cloro, são feitas as seguintes afirmações:
I. Na natureza são encontrados dois isótopos do cloro, de massas 35 e 36.
II. A abundância relativa entre os dois isótopos é aproximadamente 1:3.
III. Os íons moleculares apresentam 3 valores de massas, pois as combinações possíveis são: 35CI-35Cl; 35CI-37Cl e 37Cl-37Cl.
Estão corretas as afirmativas:
Provas
“Salinização de áreas irrigadas degrada terras do Nordeste”
Um sítio, em Ibimirim, no sertão de Pernambuco, foi abandonado. O agricultor, que já plantou tomate, milho e cebola no lote irrigado, não se conforma. “Não dá para plantar mais nada. Aqui está inutilizado pra gente”, observa Marlos Robson Dávila.
A ameaça que degrada os solos e avança pelas terras secas do semiárido é a salinização. O resultado é devastador. A primeira impressão que a gente tem é que todo esse terreno foi coberto por uma fina camada de areia, mas olhando de perto, a gente observa que a mancha branca no chão é formada por uma concentração de sais.
Fonte: Globo, 2013. Disponível em: <http://gl.globo.com/jornal-nacional/noticia/2013/07/salinizacao-de-areas-irrigadas-degrada-terras-do-nordeste.htmi>. Acesso em: 03 jul. 2019.
Sobre a salinização, analise as sentenças a seguir.
I. A salinização é um processo de acúmulo excessivo de sais minerais, estes geralmente provenientes das águas pluviais, oceânicas ou aquelas utilizadas pela irrigação na agricultura.
II. A salinização é um problema que tem se intensificado nos últimos anos. Ela pode agravar processos de infertilidade dos solos e até causar a desertificação de muitas áreas pelo mundo.
III. Em regiões de climas subtropical ou tropical, a ocorrência de salinização é muito comum. À taxa de evaporação é muito elevada e existe pouca quantidade de chuvas. As taxas de desertificação são acentuadas em regiões com esses tipos climáticos.
IV. Os recursos hídricos (exceto as águas das chuvas) apresentam sais minerais presentes na forma de diferentes íons. Normalmente, nas regiões mais frias, o índice de evaporação é muito elevado e a água passa para o estado gasoso, enquanto os sais minerais não, o que provoca o seu acúmulo excessivo nos solos e causa o problema da salinização.
Sobre as sentenças acima, assinale a alternativa CORRETA:
Provas
Em 1981 a agência americana FDA Food and Drug Administration aprovou o adoçante chamado aspartame. Essa substância é 160 vezes mais doce que a sucrose. Estruturalmente, o aspartame é um éster metílico de um dipeptídeo formado a partir de dois aminoácidos essenciais, o ácido aspártico e a fenilalanina.
Fonte: Hart, H., Hart, D., Craine, L. E. Organic Chemistry: A Short Course. Houghton Mifflin Co., 1995.
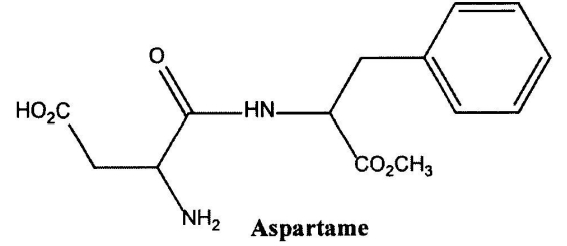
O número de carbonos assimétricos encontrados na fórmula do aspartame é (são):
Provas
“O hidróxido de sódio, cuja fórmula molecular é o NaOH, pertence à classe das bases, sendo classificada como forte, e é também comumente chamado de soda cáustica. É um sólido (temperatura ambiente) branco cristalino, higroscópico (absorve águ(A), é bastante solúvel em água e se ficar exposto ao ambiente por algum tempo, absorve a umidade do ar e vai se tornando um líquido incolor. (...)
O NaOH não existe na natureza, ele é preparado industrialmente pela eletrólise de um solução aquosa de cloreto de sódio (NaCl). No processo são utilizados eletrodos inertes, sendo produzidos gás cloro(Cl2) no eletrodo positivo e gás hidrogênio (H2) no eletrodo negativo.”
Fonte: INFO ESCOLA. Disponível em:<https://www infoescola.com/compostos-quimicos/soda-caustica/>. Acesso em: 03 jul. 2019.(adaptado).
Uma determinada indústria precisou misturar duas soluções de NaOH com molaridades diferentes para atender um cliente. Nesse processo, misturou-se 65ml, de solução a 5mol/L com 350mL de solução a 2mol/L. Qual a molaridade da nova solução?
Provas
Em uma aula prática, um aluno fez uma titulação de volumetria de neutralização em triplicata e os resultados experimentais de consumo de NaOH foram: 24,60 mL, 24,50 mL e 24, 70 mL. Sabendo que o valor teórico de volume de NaOH consumido deveria ser 22,00 mL, assinale a alternativa correta.
Provas
Caderno Container