Foram encontradas 240 questões.
Sobre preparo de amostras para análises espectroscópicas são realizadas as seguintes afirmações:
I – Substâncias que não se dissolvem em ácidos geralmente podem ser dissolvidas em um fundente inorgânico, suficientemente quente para estar fundido.
II – Os ácidos não oxidantes (HCl, HBr, HF, H3PO4, H2SO4 diluído e HClO4 diluído) dissolvem muitos metais por meio de uma reação redox.
III – As substâncias que não se dissolvem em ácidos não oxidantes podem ser dissolvidas em ácidos oxidantes como o HNO3, o H2SO4 concentrado a quente ou o HClO4 concentrado a quente.
IV – O ácido fluorídrico quente é especialmente útil na dissolução de silicatos.
É correto afirmar que:
Provas
São equipamentos indicados para coletar amostras de águas superficiais e sedimentos, respectivamente:
Provas
A reação entre o Nitrogênio (N2) e Hidrogênio (H2), ambos no estado gasoso, formando a amônia gasosa e liberando energia !$ (\Delta H < 0) !$. As variáveis inerentes ao sistema como pressão, temperatura, concentração e outros podem ser controladas. Considerando que a mistura destes gases estejam no estado de equilíbrio é incorreto afirmar que:
Provas
O pH de uma solução de ácido acético de concentração igual 0,015 mol.L-1 será de:
Provas
A massa de sulfato de bário, em microgramas, que pode ser solubilizada em 500mL de solução de nitrato de bário 0,01 mol.L-1, à 25ºC, é de:
Provas
Deseja-se preparar uma solução tampão com pH = 9,00 a partir de 50mL de solução de NH4Cl (cloreto de amônio) 0,1 mol.L-1. Para isso deve-se adicionar um volume adequado de uma solução de NaOH 0,10 mol.L-1. O volume de NaOH que deve ser adicionado aos 50mL da solução de !$ NH_4C\ell !$ esta expresso na alternativa:
Provas
O padrão primário é uma substância extremamente importante em química analítica e é usada como material de referência em titulações. Assinale a alternativa incorreta em relação ao padrão primário:
Provas
Uma amostra pesando 5,00g foi previamente diluída em água e submetida a um ensaio volumétrico para determinação do teor de carbonato de sódio e bicarbonato de sódio. A titulação foi basicamente “dividida” em duas etapas, de modo que primeira etapa utilizou-se o indicador de fenolftaleína e na segunda etapa utilizou-se o indicador de alaranjado de metila. Na primeira etapa foram gastos 15,80mL de ácido clorídrico padronizado de concentração igual a 0,1 mol.L-1. Na segunda etapa gastou-se 25,20mL do mesmo ácido para determinação do ponto final da titulação (considere que toda a amostra foi usada para esta titulação). Suponha que o ácido reagiu apenas com os sais citados anteriormente. A alternativa que representa, respectivamente, o teor de carbonato de sódio e bicarbonato de sódio em %m/m é:
Provas
Considere o rótulo do reagente abaixo para calcular qual será o volume de ácido clorídrico concentrado que deverá ser usado para preparar 250,0mL de solução de ácido clorídrico na concentração de 0,5 mol.L-1.
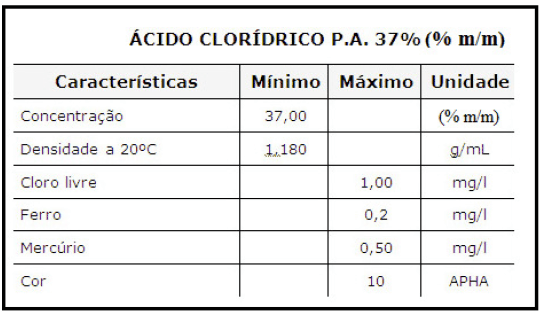
O volume necessário é de:
Provas
Analise o espectro abaixo:
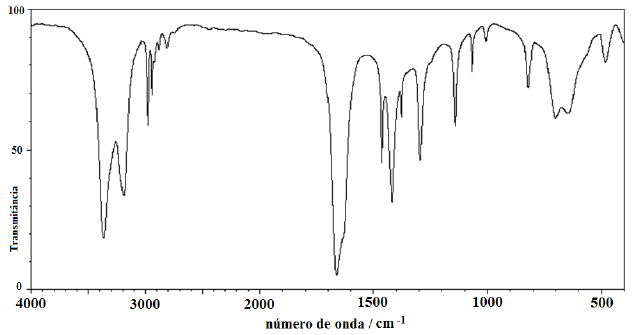
Pode-se afirmar que o espectro acima se refere a uma:
Provas
Caderno Container