Foram encontradas 240 questões.
As enzimas catalisam reações biológicas importantes para o correto funcionamento do organismo e a maioria delas possui em seu centro ativo um metal. Em relação ao mecanismo de catálise enzimática determine a afirmativa correta:
Provas
Na figura abaixo é apresentado o diagrama de orbitais moleculares para a molécula de NO.
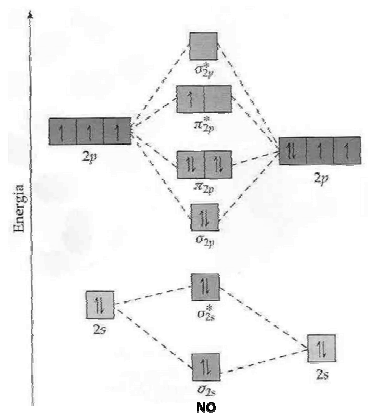
De acordo com a teoria de Lewis essa molécula seria formada por uma ligação dupla, mas na verdade seu comprimento de ligação experimental sugere uma ordem de ligação maior do que uma ligação dupla e menor do que a tripla. Este fato é explicado :
Provas
A série espectroquímica foi determinada experimentalmente e serve como ferramenta para a teoria do campo cristalino:
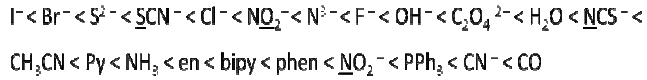
O monóxido de carbono está no final da série espectroquímica e a explicação para isso é fornecida pela teoria dos orbitais moleculares, pois:
Provas
O Mecanismo desta reação ainda não é totalmente conhecido e por isso é extensivamente estudado por pesquisadores com o objetivo de desvendá-lo. A figura abaixo apresenta uma proposta de ciclo catalítico para a sMMO.
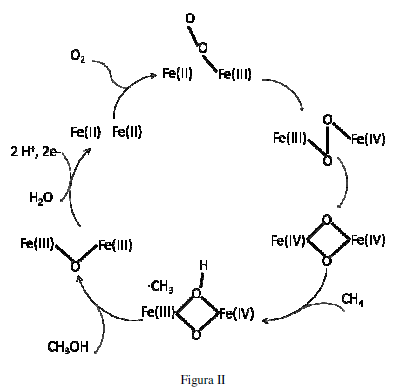
De acordo com o ciclo catalítico apresentado na Figura II, determine a alternativa correta:
Provas
A enzima metano monooxigenase (MMO) é capaz de oxidar a ligação C-H no metano e pertence à classe das enzimas oxidoredutases. A MMO tem sido bastante estudada por converter metano em metanol. O Sítio ativo da enzima MMO solúvel (sMMO) está representado na figura abaixo:
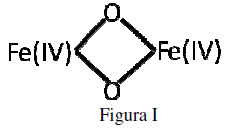
Determine a alternativa correta em relação à Figura I.
Provas
A reação abaixo descreve uma hidrogenação de alcenos catalisada por platina metálica.
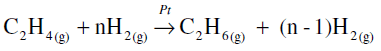
Para esta reação o mecanismo geral é:
Provas
A energia de rede !$ ( E_{Rede} ) !$ mede a estabilidade de compostos iônicos como por exemplo, NaCl, (NH4)2SO4 e [Pt(NH3)4Cl2]Br2. A equação para a energia de rede é relativamente simples: !$ E_{Rede} = k { \large |q_cq_a| \over d} !$ , na qual !$ k !$ é uma constante, !$ q_c !$ é a carga do cátion e !$ q_a !$ a carga do ânion e d a distância da ligação iônica formada.
O Cloreto de cromo hidratado disponível comercialmente apresenta fórmula molecular igual a CrCl3·6H2O no estado sólido. Uma solução aquosa deste sólido é levada a aquecimento para total solubilização, tornando-se assim de coloração violeta. O composto 1, formado nesta solução violeta, apresenta energia de rede igual a !$ E_{Rede}^1 = { \large 9k \over d} !$ . Iniciando-se do Cloreto de cromo pentahidratado sólido, CrCl3·5H2O, outra solução aquosa é feita e a solução do composto 2 apresenta coloração esverdeada à temperatura ambiente, pela formação de um composto iônico com !$ E_{Rede}^2 = { \large 4k \over d} !$ .
Considerando o texto acima responda a questão.
Porque é necessário aquecer a solução para formar uma solução aquosa do composto 1 e não é necessário para o composto 2?
Provas
A energia de rede !$ ( E_{Rede} ) !$ mede a estabilidade de compostos iônicos como por exemplo, NaCl, (NH4)2SO4 e [Pt(NH3)4Cl2]Br2. A equação para a energia de rede é relativamente simples: !$ E_{Rede} = k { \large |q_cq_a| \over d} !$ , na qual !$ k !$ é uma constante, !$ q_c !$ é a carga do cátion e !$ q_a !$ a carga do ânion e d a distância da ligação iônica formada.
O Cloreto de cromo hidratado disponível comercialmente apresenta fórmula molecular igual a CrCl3·6H2O no estado sólido. Uma solução aquosa deste sólido é levada a aquecimento para total solubilização, tornando-se assim de coloração violeta. O composto 1, formado nesta solução violeta, apresenta energia de rede igual a !$ E_{Rede}^1 = { \large 9k \over d} !$ . Iniciando-se do Cloreto de cromo pentahidratado sólido, CrCl3·5H2O, outra solução aquosa é feita e a solução do composto 2 apresenta coloração esverdeada à temperatura ambiente, pela formação de um composto iônico com !$ E_{Rede}^2 = { \large 4k \over d} !$ .
Considerando o texto acima responda a questão.
As reações químicas envolvidas na formação dos compostos 1 e 2. São, respectivamente:
Provas
A hemoglobina é uma molécula biológica cujo centro ativo, normalmente chamado de grupo heme, pode ser representado pelo complexo de coordenação da figura abaixo.
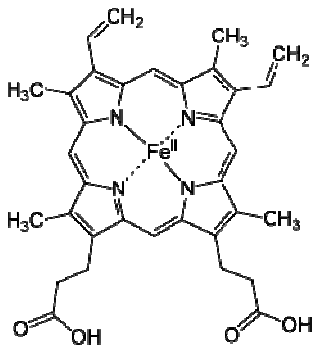
Uma das funções principais da hemoglobina é se ligar à molécula de oxigênio (O2) e transportá-lo até os pulmões. Já o monóxido de carbono presente na atmosfera e sub-produto da combustão completa de combustíveis orgânicos pode também se ligar à hemoglobina tendo efeito fatal em consequência de asfixia. Em relação ao texto acima responda a questão:
O Grupo heme pode ser caracterizado como um ligante:
Provas
A hemoglobina é uma molécula biológica cujo centro ativo, normalmente chamado de grupo heme, pode ser representado pelo complexo de coordenação da figura abaixo.

Uma das funções principais da hemoglobina é se ligar à molécula de oxigênio (O2) e transportá-lo até os pulmões. Já o monóxido de carbono presente na atmosfera e sub-produto da combustão completa de combustíveis orgânicos pode também se ligar à hemoglobina tendo efeito fatal em consequência de asfixia. Em relação ao texto acima responda a questão:
Determine a alternativa correta:
Provas
Caderno Container