Foram encontradas 60 questões.
Observe a figura a seguir.
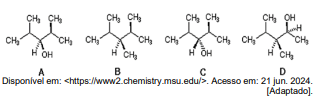
Compostos quirais possuem isômeros que, apesar de terem exatamente os mesmos elementos e ligações, não podem ser sobrepostos por causa da disposição espacial. Qual das estruturas acima representa um composto quiral?
Provas
Observe a figura a seguir.

Reações de substituição em aromáticos são ferramentas versáteis para o planejamento e execução de rotas sintéticas e processos industriais. Qual é o catalisador que deve ser empregado para promover a seguinte a reação de substituição no benzeno?
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
- Sistemas de EquilíbrioSistemas Homogêneos: Constantes: Kc e Kp. Deslocamento do Equilíbrio: Fatores
Um sistema químico reacional em equilíbrio pode ser perturbado, de forma que a reação é deslocada no sentido direto (formação de produtos a partir dos reagentes) ou inverso (decomposição dos produtos nos reagentes). Sabe-se que a reação: \( CH_4 (g) \, + \, H_20 \, (g) \, \rightleftharpoons \, CO (g) \, + \, 3H_2 \, (g) \) é endotérmica.
Após o sistema reacional atingir o equilíbrio, pode-se afirmar que
Provas
Reações em fases gasosas podem ter sua constante de equilíbrio definida em termos das pressões parciais. Esse parâmetro pode ser usado para determinar qual a composição final do sistema quando atingir o equilíbrio. A constante de equilíbrio da reação \( Cl_2 \, (g) \, + \, Br \, _2(g) \, \rightleftharpoons \, 2 \, BrCl \, (g) \) é \( K \, = \, 0,01. \) No equilíbrio, um sistema apresentou pressões parciais para o Cl2 em 10 bar e para o BrCl em 5 bar.
Qual era a pressão parcial do Br2, em bar, no equilíbrio?
Provas
O calor liberado ou consumido em uma reação química é dado pela sua entalpia de reação \( (\Delta_r \, H). \) Duas etapas consecutivas da preparação industrial de ácido sulfúrico são dadas pelas equações químicas 1 e 2 descritas abaixo, juntamente com suas respectivas entalpias de reação.
Com base nesses dados, qual é o valor da entalpia da reação 3, em kJ mol-1?
Dados:
\( Equação \, 1: \, S \, (s) \, + \, 0_2 \, (s) \, \rightarrow \, SO_2 \, (g) \, \Delta_r \, H \, = \, -300 \, KJ \, mol^{-1} \)
\( Equação \, 2: \, 2 \, S \, (s) \, + \, 3 \, 0_2 \, (g) \, \rightarrow \, 2 \, SO_3 \, (g) \, \Delta_r \, H \, = \, -800 \, KJ \, mol^{-1} \)
\( Equação \, 3: \, 2 \, SO_2 \, (g) \, + \, 0_2 \, (g) \, \rightarrow \, 2 \, SO_3 \, (g) \, \Delta_r \, H \, = \, ? \)
Provas
Observe a equação química não balanceada apresentada a seguir.
m H2S + n HNO3 \( \rightarrow \) o H2SO4 + p NO + q H2O
Elaborado pelo(a) autor(a).
A partir do balanceamento estequiométrico dessa equação, empregando-se algarismos inteiros, a soma dos coeficientes m, n, o, p e q é igual a
Provas
Observe a figura a seguir.
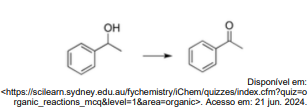
Reações orgânicas são comumente classificadas de acordo com as transformações que ocorrem nas moléculas participantes. Como pode ser classificada a reação acima?
Provas
Metanol pode ser oxidado para ácido fórmico, por meio de rotas metabólicas com as enzimas ADH e FDH. A oxidação pode ser verificada pela variação no número de oxidação de elementos.
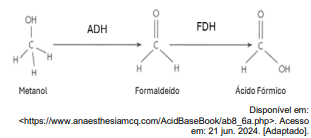
Qual é o número de oxidação do carbono no metanol e no ácido fórmico, respectivamente?
Provas
O potencial padrão de uma célula eletroquímica (as vezes chamado de força eletromotriz) é um parâmetro importante para avaliar a espontaneidade da reação redox associada a célula. Qual o potencial padrão, em volts, de uma célula eletroquímica que tem os metais Zn(s) e Bi(s) como eletrodos e opera com a reação global redox \( 3 \, Zn \, (s) \, + \, 2Bi^{3+} \, (aq) \, \rightarrow \, 3 \, Zn^{2+} \, (aq) \, + \, 2 \, Bi \, (s)? \)
Dados: potenciais padrão de redução das semirreações:
\( Zn^{2+} \, (aq) \, + \, 2 \, e^- \, \rightarrow \, Zn \, (s) \, Eº \, = \, -0,76 \, V \)
\( Bi^{3+} \, (aq) \, + \, 3 \, e^- \, \rightarrow \, Bi \, (s) \, Eº \, = \, +0,20 \, V \)
Provas
Moléculas polares, quando colocadas em um campo elétrico, experimentam uma força que tende a alinhá-las com o campo. A extensão com que as moléculas se alinham com o mesmo depende do seu momento dipolar, representado pela letra grega µ (mi), que é definido como o produto entre a magnitude das cargas parciais e a distância que as separa. A partir dessas informações, determina-se que a ordem decrescente de polaridade de moléculas contendo átomos de C, H e Cl e, por consequência, de seus alinhamentos com um campo elétrico é dada,
Provas
Caderno Container