Foram encontradas 1.316 questões.
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química OrgânicaPropriedades Físicas dos Compostos Orgânicos
Analise a tabela de pontos de ebulição para diversos cloretos a seguir.
| PE (ºC) | composto | PE (ºC) | composto | PE (ºC) | composto |
| 1380 | LiCl | 12,5 | BCl3 | 76 | CCl4 |
| 1440 | NaCl | 183 | AlCl3 | 57 | SiCl4 |
| 1380 | KCl | 1000 | ScCl3 | 136 | TiCl4 |
Elaborado pelo(a) autor(a).
O caráter das ligações químicas nas substâncias tem grande influência nas suas propriedades químicas. As substâncias da tabela que apresentam os maiores pontos de ebulição apresentam, predominantemente, ligações de caráter
Provas
- Química OrgânicaCadeias Carbônicas
- Química OrgânicaFunções Nitrogenadas: Amina, Amida, Nitrila, Isonitrila e Nitro Composto
- Química OrgânicaIsomeria Plana e Espacial
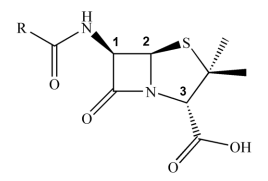
Elaborado pelo(a) autor(a).
A molécula de penicilina apresenta três centros assimétricos. As configurações absolutas dos carbonos assinalados com 1, 2 e 3 na figura são, respectivamente:
Provas
Uma solução tampão é uma mistura de um ácido fraco e sua base conjugada, ou de uma base fraca e seu ácido conjugado, que resiste a variações de pH quando pequenas quantidades de ácido ou base são adicionadas. Este efeito estabilizador ocorre porque os componentes da solução tampão neutralizam os íons H+ ou OH− adicionados, mantendo o pH da solução relativamente constante.
Quando se misturam as soluções de ácido fórmico e formiato de sódio estabelecem-se os seguintes equilíbrios:
HCOOH(aq) + H2O(l) ⇌ H3O+(aq) + HCOO-(aq) Ka = 1,8 x 10-4
HCOO-(aq) + H2O(l) ⇌ HCOOH+(aq) + OH-(aq) Kb = Kw.Ka-1 = 5,56 x 10-11
Calcule a concentração de íons hidrônio de uma solução tampão obtida pela mistura das soluções ácido fórmico 0,25 mol L-1 e formiato de sódio 0,9 mol L-1.
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Massas Molares: O = 16,0 g mol-1; C = 12 g mol-1; H = 1 g mol-
Provas
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Quando um composto iônico solúvel é adicionado à água, ocorre um processo chamado de hidratação, onde as moléculas de água envolvem os íons da superfície do sólido, separando-os dos outros íons e dissolvendo-os, gradativamente. Este processo ocorre pelas interações íon-dipolo entre as moléculas da água e os íons devido ao caráter polar da molécula de H2O, onde a carga parcial negativa do átomo de O é atraída pelos cátions e as cargas parciais positivas dos átomos de H são repelidas por eles.
ATKINS, Peter; LAVERMAN, Leroy; JONES, Loretta. Princípios de química: questionando a vida moderna e o meio ambiente. 7. Porto Alegre: Bookman, 2018.[Adaptado].
Baseado no texto acima, para qual dos cátions listados abaixo espera-se a maior energia de interação íon-dipolo?.
Provas
Leia o texto a seguir.
“Em química, entretanto, a maior parte das reações químicas ocorre em recipientes abertos para a atmosfera e, portanto, em pressão constante de cerca de 1 atm. Esses sistemas podem se expandir ou contrair livremente. Se um gás se forma, ele trabalha contra a atmosfera para ocupar espaço. Embora nenhum pistão esteja envolvido, trabalho é realizado. Nesse sentido, uma função de estado que medisse as variações de energia em pressão constante considerando automaticamente as perdas de energia como trabalho de expansão durante a transferência de calor seria muito útil.”
ATKINS, Peter; LAVERMAN, Leroy; JONES, Loretta. Princípios de química: questionando a vida moderna e o meio ambiente. 7. Porto Alegre: Bookman, 2018. [Adaptado].
A função de estado à qual o trecho grifado no texto faz referência é a
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Provas
A extração líquido-líquido é um processo aplicado que envolve misturas líquidas. Em um dado processo de produção do composto A (soluto), o soluto que se deseja extrair está inicialmente presente em uma solução binária rica em composto B (diluente). Observou-se que através da adição de um solvente puro (S), haverá formação de duas fases líquidas parcialmente imiscíveis. Para que a separação seja efetiva, uma das fases formadas deve conter grandes quantidades do composto A e do solvente (S): essa fase é chamada de extrato. Além disso, a outra fase formada deve conter grande quantidade do composto B (e pouca quantidade do composto A), sendo chamada de rafinado. O coeficiente de partição do componente A \( (K_A) \) é um parâmetro frequentemente utilizado para medir a eficiência de um processo de separação baseado em extração líquido-líquido, e pode ser calculado como dado pela equação a seguir:
\( K_A \, = \, \dfrac {[concentração \,\, do \,\, componente \,\, A \,\, na \,\, fase \,\, extrato]} {[concentração \,\, do \,\, componente \,\, A \,\, na \,\, fase \,\, rafinado]} \)
No processo que visa extrair, através de extração líquido-líquido, o soluto (A) utilizando o solvente S,
Provas
Caderno Container