Foram encontradas 50 questões.
“A maioria das enzimas são proteínas que apresentam atividade catalítica. A região da estrutura terciária de uma enzima, responsável pela atividade catalítica, denomina-se sítio ativo ou sítio catalítico. De forma geral, o sítio catalítico ocupa cerca de 10 a 20% do volume total da enzima e é nesta região que o substrato se liga para ser transformado em produto. Para o substrato se ligar ao sítio ativo é necessário força entre as duas moléculas que ajude a estabilizar e ajustar o complexo formado entre a enzima e o substrato.” Diante do exposto, marque V para as afirmativas verdadeiras e F para as falsas.
( ) O substrato pode se ligar às enzimas por meio de interações eletrostáticas. Essas interações são formadas pelos grupos funcionais ionizáveis do substrato e estão carregados em solução aquosa (ou próxima ao pH 7) que se ligam, via complexo de cargas, com grupos ionizáveis de cargas opostas do sítio ativo da enzima. Do ponto de vista energético, a energia típica deste tipo de interação está na faixa de 25 a 50 kJ/mol e a sua força é inversamente proporcional à distância entre estas duas cargas.
( ) O substrato pode se ligar às enzimas por meio das interações (ou ligações) de hidrogênio. Este tipo de interação é formado entre pares de elétrons não ligantes de átomos de N (aminas, por exemplo) e O (alcoóis, por exemplo) de um aminoácido com átomos de H ácidos (hidroxilas alcoólicas, por exemplo) de outro aminoácido (ligações de hidrogênio intermoleculares), sendo amplamente utilizado para ligar grupos funcionais polares dos aminoácidos do substrato com a enzima. A força das ligações de hidrogênio depende da natureza química e da geometria do alinhamento dos grupos que interagem entre si. A energia associada a este tipo de interação varia na faixa de 2 a 25 kJ/mol, dependendo da polaridade e cargas dos aminoácidos ligantes.
( ) O substrato pode se ligar às enzimas por meio das interações (ou ligações) de Van der Waals, também chamadas de interações não polares. Este tipo de interação ocorre entre os dipolos momentâneos formados pelo movimento dos elétrons nas nuvens eletrônicas dos aminoácidos do substrato e da enzima. Embora, de forma geral, a soma da energia do conjunto total de interações de Van der Waals seja muito significativa nas interações enzima-substrato (cerca de 50 a 100 kJ/mol), sabe-se que individualmente cada interação de Van der Waals possui baixa energia (5 a 8 kJ/mol).
( ) O substrato pode se ligar às enzimas por meio das interações hidrofóbicas. Se o substrato possui grupos hidrofóbicos em sua estrutura (anel aromático, por exemplo) é possível estabelecer interações ligantes favoráveis às regiões hidrofóbicas do sítio ativo da enzima. Estas interações hidrofóbicas podem ser entendidas como uma tendência das moléculas orgânicas apolares (ou regiões apolares) se agregarem em soluções aquosas.
A sequência está correta em
Provas
Aminoácidos são moléculas orgânicas essenciais à formação das proteínas. Basicamente, as proteínas formadas do organismo humano são construídas por apenas vinte aminoácidos. Os aminoácidos têm características químicas inerentes às suas funções orgânicas. A figura a seguir apresenta a curva de titulação do aminoácido glicina (0,1 M e 25°C) com solução de NaOH (0,1 M e 25°C). Sobre essa curva, é correto afirmar que
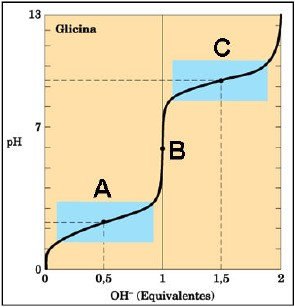
(Nelson e Cox. Princípios de Bioquímica de Lehninger. Ed. Artmed, 2011. – Com adaptações.)
Provas
Se as proteínas são as moléculas biológicas mais versáteis, por outro lado as macromoléculas mais abundantes são os carboidratos (também conhecidos como sacarídeos ou hidratos de carbono). Estima-se que, anualmente, 100 bilhões de toneladas de CO2 e H2O são convertidos em celulose e, outros subprodutos, pelas plantas. Classicamente, e de forma geral, os carboidratos são definidos como um composto derivado de estruturas polihidroxi aldeído ou um polihidroxi cetona. Entretanto, algumas classes de derivados de carboidratos podem apresentar outras funções orgânicas como aminas, amidas e ácidos carboxílicos. As três maiores classes de carboidratos são: monossacarídeos, dissacarídeos e polissacarídeos.
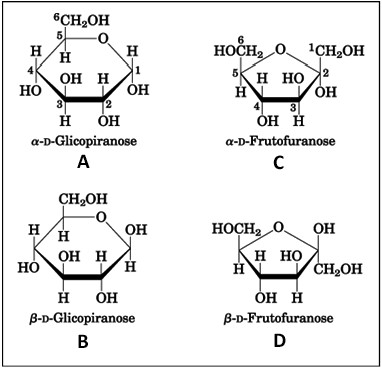
(Nelson e Cox. Princípios de Bioquímica de Lehninger. Ed. Artmed, 2011. – Com adaptações.)
Analise as estruturas químicas anteriores e assinale a alternativa INCORRETA.
Provas
É senso comum entre os cientistas que as proteínas são as macromoléculas mais versáteis dos sistemas vivos e cruciais para o correto funcionamento dos sistemas vivos. Esta classe de moléculas atua nas células desempenhando funções, tais como catalisadores biológicos, transporte de moléculas, suporte mecânico, resistência imunológica e controle do crescimento e diferenciação celular. Assinale a alternativa INCORRETA.
Provas
O desenvolvimento da teoria quimiosmótica foi um dos pontos fundamentais no entendimento sobre a forma como as células animais e vegetais conseguem transformar a energia proveniente de elétrons em moléculas de ATP’s que serão utilizadas em diversas atividades. Sobre a teoria quimiosmótica, assinale a alternativa INCORRETA.
Provas
As enzimas são moléculas essenciais ao correto funcionamento celular. Em relação às enzimas, marque V para as afirmativas verdadeiras e F para as falsas.
( ) As enzimas designadas constitutivas são aquelas produzidas em pequenas quantidades e, quando as células crescem em condições de indução específicas, em grandes quantidades.
( ) As enzimas denominadas indutíveis são aquelas formadas de forma independente do ambiente de crescimento onde a célula se encontra.
( ) A modificação covalente reversível de aminoácidos nas enzimas pode alterar a atividade das enzimas. A fosforilação de enzimas é a modificação covalente melhor estudada. Neste tipo de modificação, ocorre a transferência de grupos fosfatos do ATP (ou outros doadores) para certos grupos funcionais das cadeias laterais dos aminoácidos das enzimas. Esta transferência provoca alterações na estrutura tridimensional das enzimas e modifica suas atividades.
A sequência está correta em
Provas
A função de uma enzima é fornecer um caminho reacional de menor energia de ativação e de maior velocidade. A constante de velocidade de uma reação qualquer está relacionada à sua energia de ativação através da equação k = A .e-Eat/RT, onde A é uma constante determinada experimentalmente, R é a constante dos gases (R = 8,3 J.mol–1.K–1) e T é a temperatura na qual a reação se processa. Considere a reação S \( → \) P, que ocorre tanto na presença, quanto na ausência de enzimas. Na reação catalisada, a presença da enzima fornece uma redução na energia de ativação de 40 kJ/mol em relação à reação não catalisada. Assinale, aproximadamente, quantas vezes a velocidade da reação enzimo-catalisada é maior que a velocidade de reação não catalisada. Considere também, que a reação ocorra numa temperatura de 25°C.
Provas
Dissacarídeos são açúcares formados pela ligação de dois monossacarídeos através de uma reação de condensação com liberação de água. Uma característica reacional marcante dos dissacarídeos são as reações de hidrólise produzindo dois monossacarídeos. Considerando as propriedades fundamentais dos dissacarídeos, assinale a INCORRETA.
Provas
As enzimas são utilizadas na síntese orgânica, de forma isolada ou íntegra, através de células de animais, vegetais e micro-organismos. Devido ao alto custo para se obter enzimas, deve-se, em síntese orgânica, imobilizá-las em suportes físicos para possibilitar a sua recuperação ao final da reação. As reações orgânicas representadas a seguir são processos clássicos em síntese orgânica, como a hidrólise e a transesterificação. Elas podem ser químicocatalisadas ou enzimo-catalisadas. Todas as reações foram catalisadas pelo mesmo grupo de enzimas.
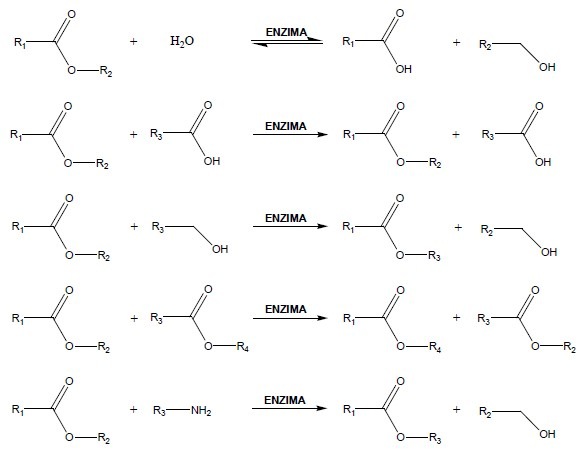
As enzimas que catalisam as reações orgânicas anteriores são as
Provas
Analise as afirmativas a seguir.
I. Na glicólise, uma molécula de glicose é degradada numa série de reações enzimo-catalisadas que produzem duas moléculas de três carbonos (piruvato).
II. Durante a sequência de reações da glicólise, uma parte da energia química disponível na glicose é conservada na forma de ATP e NADH.
III. A quebra da glicose é a única fonte de energia metabólica em alguns tecidos e células de mamíferos, como, por exemplo, os eritrócitos e os neurônios.
IV. Fermentação é um termo geral utilizado para designar a degradação anaeróbica da glicose e outros nutrientes orgânicos para obter energia conservada na forma de ATP.
Está(ão) correta(s) a(s) afirmativa(s)
Provas
Caderno Container